- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Химическая связь. Типы кристаллических решеток
Содержание
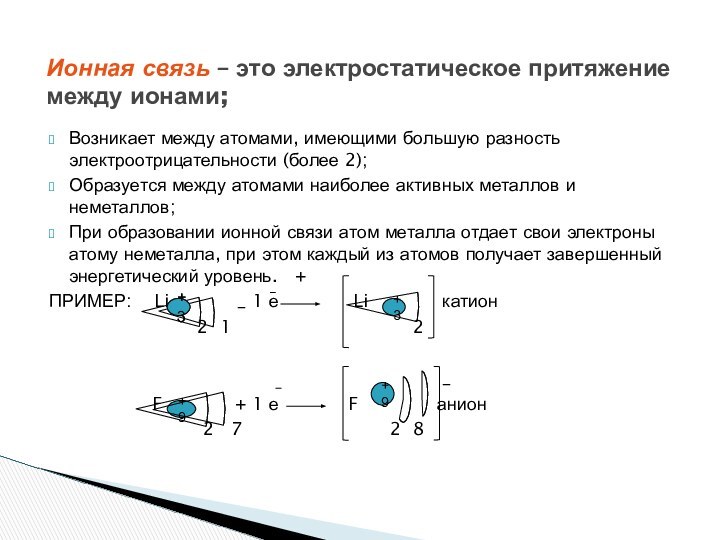
- 2. Химическая связь- взаимодействие между атомами, приводящее к образованию устойчивой системы- молекулы, иона, кристалла.
- 3. Возникает между атомами, имеющими большую разность электроотрицательности
- 4. -ОН , -2SO, - Cl
- 5. Вещества с ионной связью при н.у. находятся
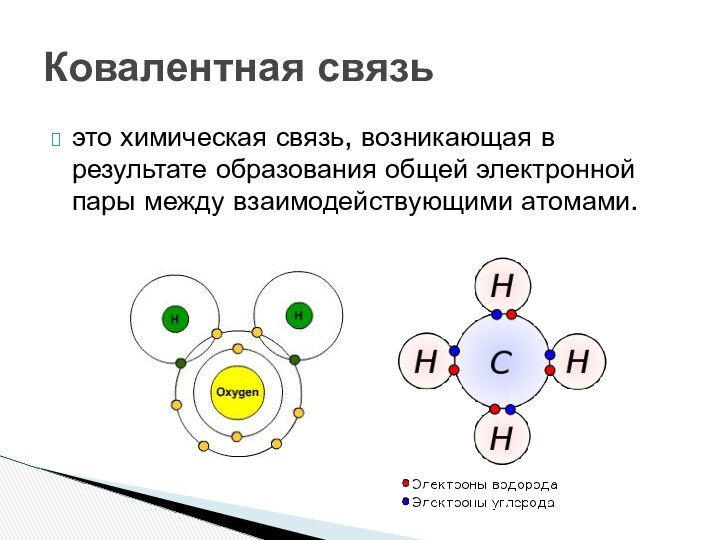
- 6. это химическая связь, возникающая в результате образования общей электронной пары между взаимодействующими атомами. Ковалентная связь
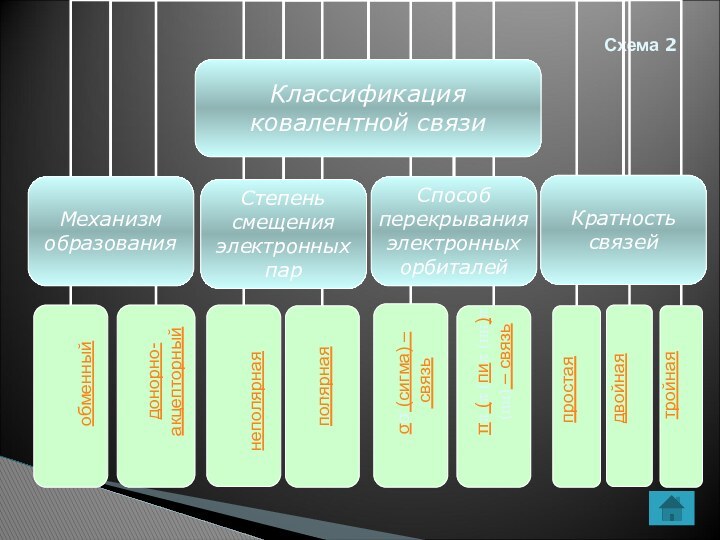
- 7. Схема 2обменныйдонорно-акцепторныйполярнаянеполярнаяσσ (сигма) – связьππ (π (пиπ (пи)π (пи) – связьпростаядвойнаятройная
- 8. Механизмы образования ковалентной связи
- 9. Обменный механизм образования ковалентной связи☼ Действует,
- 10. Донорно-акцепторный механизм образования ковалентной связи
- 11. Степень смещения электронных пар☼Зависит от ЭЛЕКТРООТРИЦАТЕЛЬНОСТИ элементов.Ряд
- 13. Кратность ковалентной связи☼Зависит от числа общих электронных
- 14. Длина связи – расстояние между центрами двух
- 15. насыщаемость – молекулы и ионы имеют определенный
- 16. газамижидкостямитвердыми -- аморфные (расположение частиц в
- 17. При кристаллизации веществ с ковалентной связью образуется
- 18. Металлическая химическая связь осуществляется свободными электронами, общими
- 19. Механизм образования металлической связи:
- 20. ненасыщенная;ненаправленная.Особенности металлической связи: сравнительно небольшое количество электронов
- 21. Водородная химическая связь – это электростатическое притяжение
- 22. Водородная связьМежмолекулярная водородная связь – этосвязь между
- 23. Водородная связьВнутримолекулярная водородная связь – эта связь
- 25. Физическая природа химической связи едина – это
- 26. Резких границ между разными видами химических связей нет, все виды химической связи имеют единую электрическую природу.
- 27. Что представляют собой ионы? Ионы – это
- 28. Выполните упражнение №1Из предложенного списка распределите формулы
- 29. Выполните упражнение №2Покажите образование ионнойсвязи в соединениях:
- 30. Скачать презентацию
- 31. Похожие презентации




















Слайд 2 Химическая связь- взаимодействие между атомами, приводящее к образованию
устойчивой системы- молекулы, иона, кристалла.
Слайд 3 Возникает между атомами, имеющими большую разность электроотрицательности (более
2);
Образуется между атомами наиболее активных металлов и неметаллов;
При образовании
ионной связи атом металла отдает свои электроны атому неметалла, при этом каждый из атомов получает завершенный энергетический уровень. +ПРИМЕР: Li _ 1 е Li катион
2 1 2
_
F + 1 е F анион
2 7 2 8
Ионная связь – это электростатическое притяжение между ионами;
+3
+3
+3
+9
+9
Слайд 5 Вещества с ионной связью при н.у. находятся в
твердом агрегатном состоянии и образуют кристаллы с ионной кристаллической
решеткойВ узлах ионной кристаллической решетки находятся ионы, между которыми присутствует ионная связь
Физические свойства: тугоплавкие, нелетучие, твердые, но хрупкие, многие растворимы, в растворах и расплавах проводят электрический ток (щелочи, соли и др.)
Ионная связь является крайним случаем ковалентной полярной связи
Слайд 6 это химическая связь, возникающая в результате образования общей
электронной пары между взаимодействующими атомами.
Ковалентная связь
Слайд 7
Схема 2
обменный
донорно-
акцепторный
полярная
неполярная
σσ (сигма) –
связь
ππ (π (пиπ (пи)π
(пи) – связь
простая
двойная
тройная
Слайд 9
Обменный механизм образования ковалентной связи
☼ Действует, когда
атомы образуют общие электронные пары за счёт объединения неспаренных
электронов.Например:
Н2 – водород Н• + •Н → Н ׃ Н или Н - Н ;
НCl – хлороводород или соляная кислота
Н• + • Cl → Н Cl или H – Cl ;
3. N2 – азот N • + • N → N N или N N.
••
••
••
••
••
••
••
••
••
•••
•
•
•
•
•••
••
••
Слайд 10
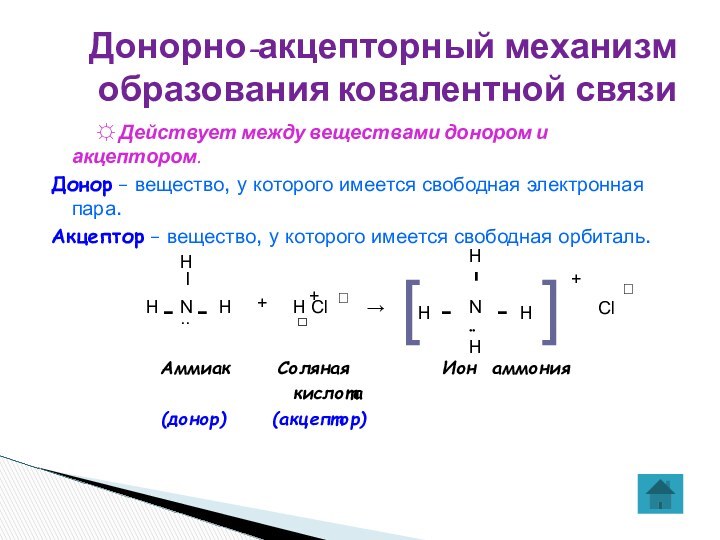
Донорно-акцепторный механизм образования ковалентной связи
☼ Действует между веществами донором и акцептором.
Донор – вещество,
у которого имеется свободная электронная пара.Акцептор – вещество, у которого имеется свободная орбиталь.
Аммиак Соляная Ион аммония
кислота
(донор) (акцептор)
Н
Н
N
H
..
-
-
І
+
H Cl
□
→
+
[ ]
-
-
-
H
H
H
H
N
••
+
Cl
Слайд 11
Степень смещения электронных пар
☼Зависит от ЭЛЕКТРООТРИЦАТЕЛЬНОСТИ элементов.
Ряд электроотрицательности:
F, O, N, C l, Br, S, C,
P, SiНЕПОЛЯРНАЯ ковалентная связь – это связь, образованная между атомами с одинаковой электроотрицательностью.
Например : H – H; Cl – Cl; N N.
ПОЛЯРНАЯ ковалентная связь – это связь, образованная между атомами с разной электроотрицательностью.
Например: H – Cl; H – S – H.
ІІІ
Слайд 13
Кратность ковалентной связи
☼Зависит от числа общих электронных пар,
связывающих атомы.
Бывает:
ПРОСТАЯ « - » - это одна
σ-связь;ДВОЙНАЯ « » - это одна σ-связь и одна π-связь;
3. ТРОЙНАЯ « » - это одна σ-связь и две π- связи.
ІІ
ІІІ
Слайд 14 Длина связи – расстояние между центрами двух соседних
атомов (зависит от радиуса атома и кратности связи);
Энергия связи
– количество энергии, которую нужно затратить на разрыв 1 моля связи;Кратность связи – число общих электронных пар между двумя атомами;
Валентный угол – угол между лучами, выходящими из центра одного атома к центрам двух соседних атомов;
Полярность связи – неравномерное распределение электронной плотности между атомами в молекуле
Параметры ковалентной связи:
Слайд 15 насыщаемость – молекулы и ионы имеют определенный состав,
т.к. образуется определенное и ограниченное число связей;
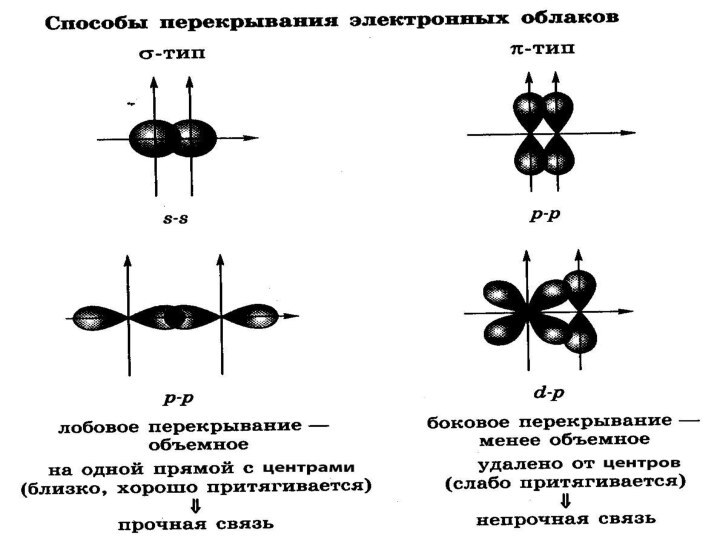
направленность – электронные
облака могут перекрываться в разном направлении и образовывать σ- и π- связи;поляризуемость – изменяется полярность под действием внешнего электрического поля.
Для веществ с ковалентной связью характерны молекулярные и атомные кристаллические решетки.
Свойства ковалентной связи:
Слайд 16
газами
жидкостями
твердыми
-- аморфные (расположение частиц в них
неупорядоченное, например – стекло, смола, полимеры и др.)
-- кристаллические (характеризуются упорядоченной структурой – NaCl, KNO3 ….)Вещества с ковалентной связью бывают при обычных условиях:
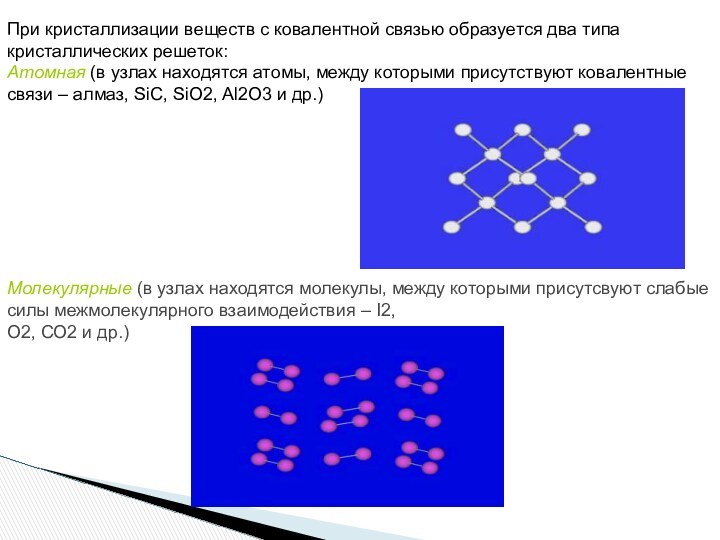
Слайд 17 При кристаллизации веществ с ковалентной связью образуется два
типа кристаллических решеток:
Атомная (в узлах находятся атомы, между
которыми присутствуют ковалентные связи – алмаз, SiC, SiO2, Al2O3 и др.)Молекулярные (в узлах находятся молекулы, между которыми присутсвуют слабые силы межмолекулярного взаимодействия – I2,
О2, СО2 и др.)
Слайд 18 Металлическая химическая связь осуществляется свободными электронами, общими для
всего кристалла.
Металлы образуют металлические кристаллические решетки, в узлах которых
находятся катион-атомы, а между ними «электронный газ», определяющий такие физические свойства металлов, как металлический блеск, тепло и электропроводность.
Слайд 19
Механизм
образования металлической связи:
0 n+
М - nē = М
Например:
для элементов (металлов) Ι группы главной
0 1+
подгруппы М - 1ē = М ;
для элементов (металлов) Ι Ι группы главной
0 2+
подгруппы М - 2ē = М .
Слайд 20
ненасыщенная;
ненаправленная.
Особенности металлической связи: сравнительно небольшое количество электронов одновременно
связывает множество атомных ядер – связь делокализована. Эти электроны
свободно перемещаются по всему кристаллу («электронный газ»), который в целом нейтрален.Характерна металлическая кристаллическая решетка, в узлах которой находятся положительно заряженные ионы и свободные атомы, между ними находятся отрицательно заряженные электроны.
Свойства металлической связи:
Слайд 21
Водородная химическая связь – это электростатическое притяжение между
положительно поляризованными атомами водорода одной молекулы и отрицательно поляризованными
атомами (F, O, N) другой молекулы. Механизм образования водородной связи близок к донорно-акцепторному ( R –Н δ+ …. Э δ- – R)
Слайд 22
Водородная связь
Межмолекулярная водородная связь – это
связь между атомами
водорода одной
молекулы и сильноотрицательными
элементами(O, N, F) другой молекулы.
Н
О - - - - Н О Н Н Н Н - - - - О Н - - - - О Н
|
|
|
|
|
|
|
|
Слайд 23
Водородная связь
Внутримолекулярная водородная связь –
эта связь возможна
при наличии в одной
молекуле и электроноакцепторной
группы и электронодонорного атома.
Например
в молекулеДНК: І І
А-Т
Г-Ц
Г-Ц
Т-А
І І
Слайд 25 Физическая природа химической связи едина – это ядерно-электронное
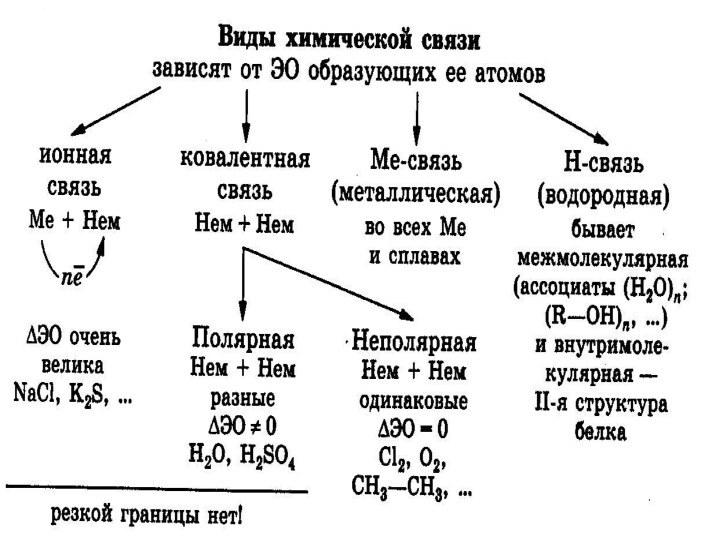
взаимодействие.
Деление химической связи на виды условно и связано с
природой химических элементов:А) металлы (большие размеры атомов, малая электроотрицательность, способны отдавать электроны, превращаясь в катионы);
Б) неметаллы (малые размеры атомов, большая электроотрицательность, способны принимать электроны, превращаясь в анионы).
Природа химической связи едина, и ионную связь можно рассматривать как предельный случай ковалентной связи, поэтому говорят о степени ионной связи. Даже в таком соединении, как CsF, ионная связь выражена только на 89%.
Единство химической связи
Слайд 26 Резких границ между разными видами химических связей нет,
все виды химической связи имеют единую электрическую природу.
Слайд 27
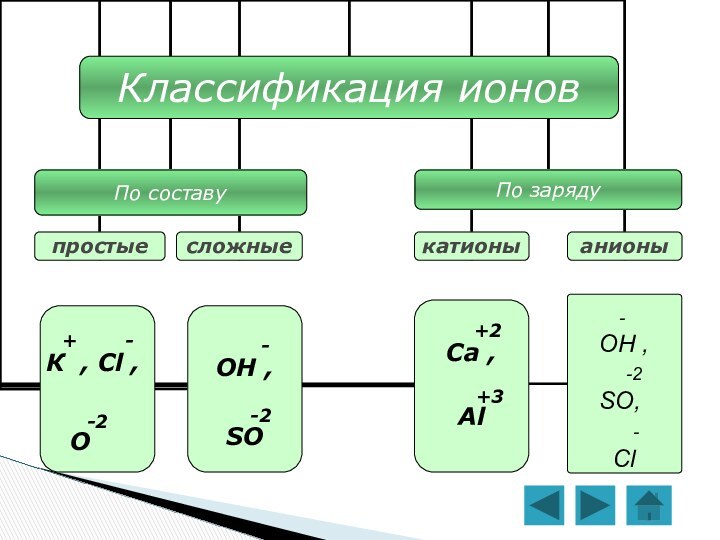
Что представляют собой ионы?
Ионы – это положительно
или отрицательно заряженные частицы, в которые превращаются атомы или
группы атомов в результате отдачи электронов (окисления) или присоединения электронов (восстановления).Какая химическая связь связывает ионы?
Ионная.
Какие частицы связываются ковалентной связью?
Атомы. Синоним ковалентной связи – атомная связь.
Для атомов каких элементов характерна металлическая связь?
Для атомов металлов, имеющих на внешнем уровне в основном 1 – 3 электрона и сравнительно большой радиус атома.
Где встречается водородная связь?
В биополимерах – в двойной спирали молекулы ДНК, между молекулами растворителя и молекулами растворенного вещества (растворение этанола в воде).
Дайте ответы на вопросы: