- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Химия Соли
Содержание
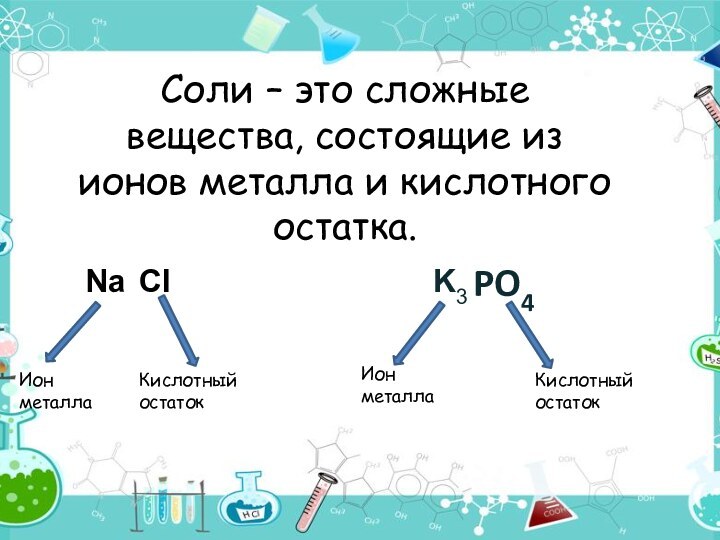
- 2. Соли – это сложные вещества, состоящие из ионов металла и кислотного остатка.PO4Ион металлаКислотный остатокИон металлаКислотный остатокNaClK3
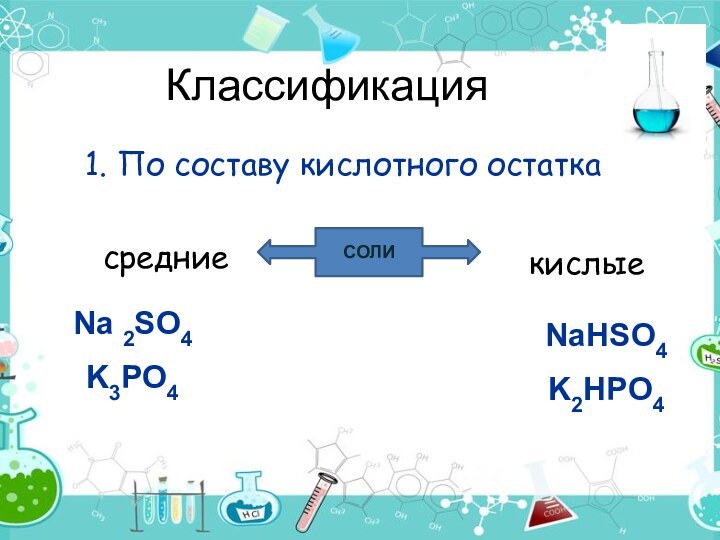
- 3. Классификация 1. По составу кислотного остаткаСОЛИсредниекислыеNa 2SO4K3PO4NaHSO4K2HPO4
- 4. Номенклатура средних солеймагнияНазвание кислотного остаткаНаименование металла в родительном падежеМgСL2 хлорид
- 5. Номенклатура кислых солейУказать название кислотного остаткаК названию кислотного остатка прибавить «гидро-»Наименование металла в родительном падежеNaHSO4сульфатгидронатрия
- 6. Химические свойства1. Взаимодействие с металлами:
- 7. Химические свойства 2. Взаимодействие со щелочами:
- 8. Химические свойства3. Взаимодействие солеймежду собойКСl + AgNO3 → AgCl + KNO3
- 9. Химические свойства4.Взаимодействие с кислотами:Сильные кислоты вытесняют более
- 10. Химические свойства Разложение при нагревании
- 11. Способы получения 1. Кислота + основание
- 12. Скачать презентацию
- 13. Похожие презентации
Соли – это сложные вещества, состоящие из ионов металла и кислотного остатка.PO4Ион металлаКислотный остатокИон металлаКислотный остатокNaClK3









Слайд 4
Номенклатура средних солей
магния
Название кислотного остатка
Наименование металла в родительном
падеже
МgСL2
хлорид
Слайд 5
Номенклатура кислых солей
Указать название кислотного остатка
К названию кислотного
остатка прибавить «гидро-»
Наименование металла в родительном падеже
NaHSO4
сульфат
гидро
натрия
Слайд 9
Химические свойства
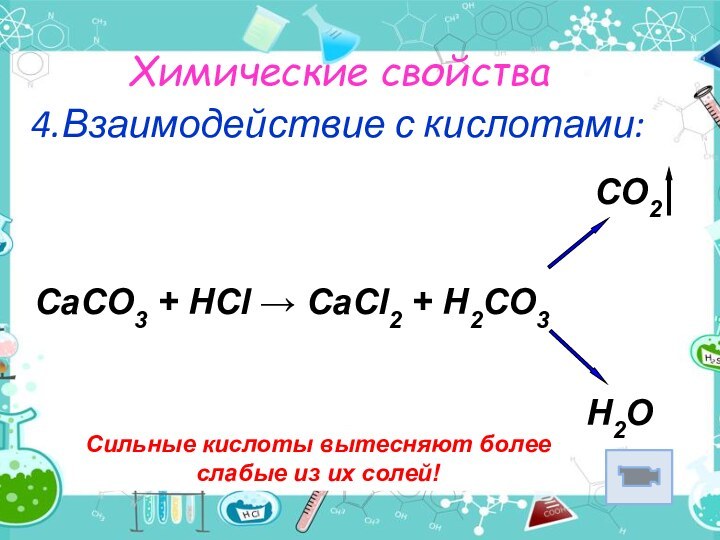
4.Взаимодействие с кислотами:
Сильные кислоты вытесняют более слабые
из их солей!
CO2CaCO3 + HCl → CaCl2 + H2CO3
H2O
Слайд 11
Способы получения
1. Кислота + основание = соль
+ вода
H2SO4 +2NaOH = Na2SO4
+ 2H2O2. Кислота + металл = соль + водород
2HCL +Zn = ZnCL2 + H2
3. Кислота + основный оксид = соль + вода
2HCL + CuO = CuCL2 + H2O
4. Кислота + соль = новая кислота + новая соль
H2SO4 + BaCL2 = 2HCL + BaSO4
Условия: в результате реакции должны получиться газ, осадок или вода.
Основаны на химических свойствах оксидов,
оснований, кислот
10
способов
10
способов
10
способов
10
способов
10
способов





























