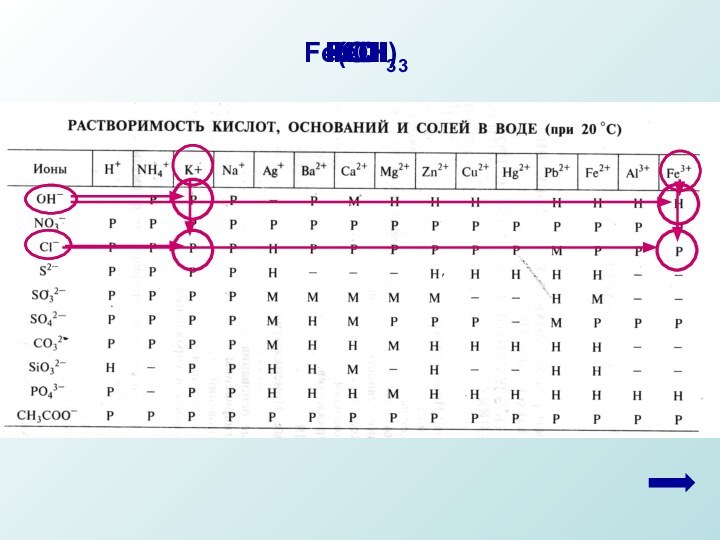
и гидроксида калия. Написать молекулярное и ионные уравнения реакции
между этими растворами.FeCl3
+
+
KOH
KCl
Fe(OH)3
=
3
3
расставить коэффициенты
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть



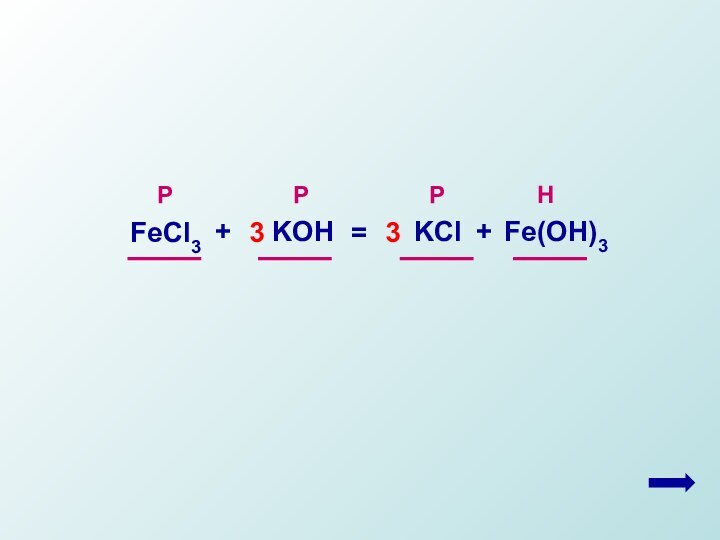


FeCl3
+
+
KOH
KCl
Fe(OH)3
=
3
3
расставить коэффициенты
Fe3+
+
+
K+
K+
Fe(OH)3
=
3
3
Cl-
+
+
OH-
Cl-
3
3
+
3
FeCl
+
+
KOH
KCl
Fe(OH)3
=
3
3
Р
Р
Р
Н
3
Необходимо учитывать индексы у ионов и коэффициенты в уравнении реакции.