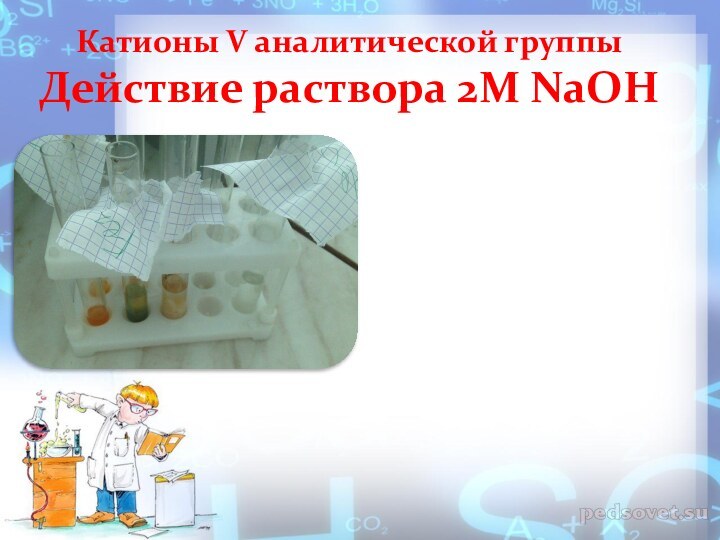
V аналитической группы
Действие раствора 2М Действие раствора 2М
NaOHДействие раствора Действие раствора K3[Fe(CN)6]
Действие раствора Действие раствора KДействие раствора K4Действие раствора K4[Fe(CN)6]
Действие раствора Действие раствора NH4NCS
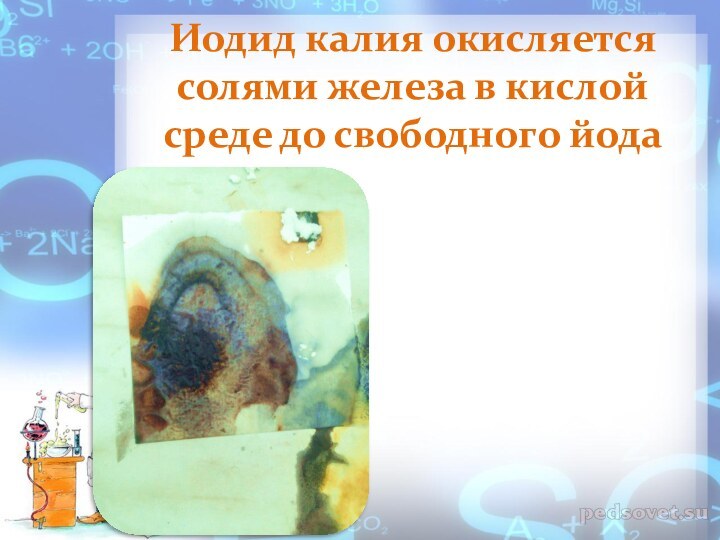
Иодид калия окисляется солями железа в кислой среде до свободного йода
Пероксид водорода
Моно гидрофосфат натрия
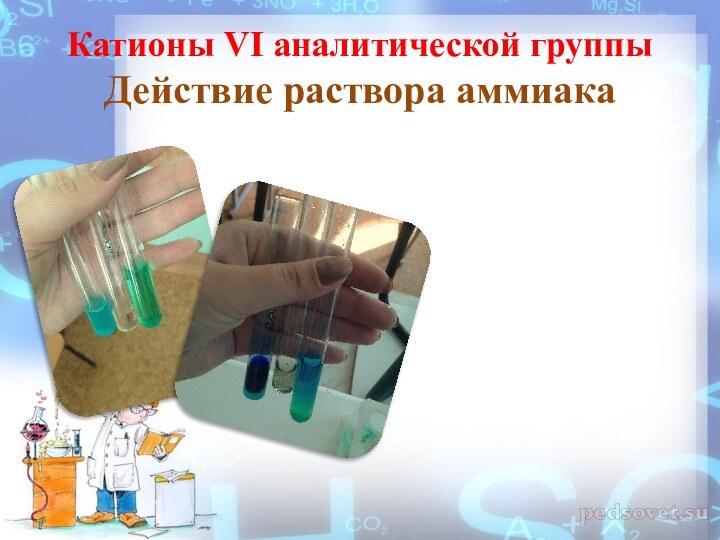
Катионы VI аналитической группы
Действие раствора аммиака
Действие щёлочи
Реакция на катион меди(Реакция на катион меди(IIРеакция на катион меди(II)




![Качественные реакции катионов V и VI аналитической группы Действие раствора K3[Fe(CN)6]К 2-3 каплям раствора железа(II) хлорида прибавляли 2 капли раствора](/img/tmb/12/1164303/c5b3f3a87f9b67874985b23f71510c1b-720x.jpg)
![Качественные реакции катионов V и VI аналитической группы Действие раствора K3[Fe(CN)6]](/img/tmb/12/1164303/d808a1830330a7ea3ef8585f4c7782a6-720x.jpg)
![Качественные реакции катионов V и VI аналитической группы Действие раствора K4[Fe(CN)6]К 2-3 каплям раствора железа(II) хлорида прибавляли 2 капли раствора](/img/tmb/12/1164303/dbdce842d85155770b8b4ef398785896-720x.jpg)