- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Карбонатна кислота
Содержание
- 2. Карбонатна кислотаВугільна кислота — слабка двоосновна кислота з хімічною формулою . У
- 3. Фізичні властивості Молекула вугільної кислоти має плоску
- 4. Розкладання При підвищенні температури розчину і/або пониженні парціального
- 5. Отримання Вугільна кислота утворюється при розчиненні у
- 6. Застосування Вугільна кислота завжди присутня у водних розчинах вуглекислого газу (см. Газована вода).
- 7. В біохімії використовується властивість рівноважної системи змінювати тиск газу
- 8. Органічні похідні Вугільну кислоту формально можна розглядати
- 9. Деякі представники подібних з'єднань перераховані в таблиці.
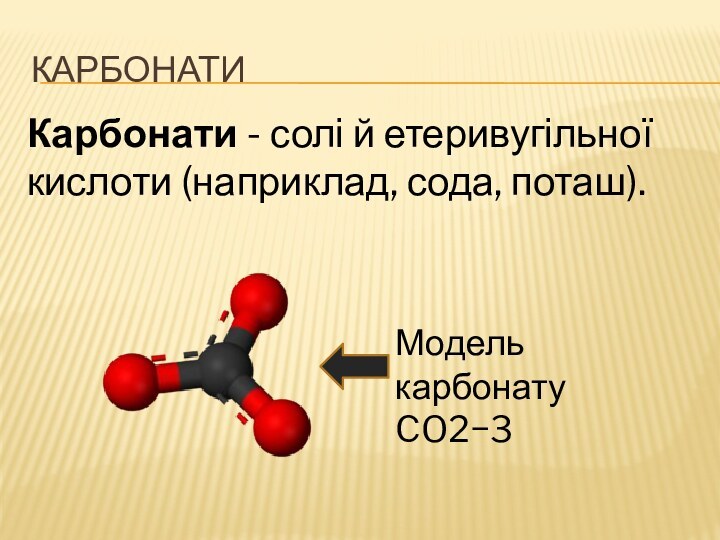
- 10. КарбонатиКарбонати - солі й етеривугільної кислоти (наприклад, сода, поташ).Модель карбонату CO2−3
- 11. Усі карбонати, за винятком карбонатів лужних металів і амонію, у
- 12. Карбонати лужних металів у термічному відношенні значно
- 13. Гідрокарбонати, на відміну від карбонатів, у воді
- 14. У термічному відношенні гідрокарбонати менш стійкі за
- 15. З солей карбонатної кислоти найбільше практичне значення
- 16. Скачать презентацию
- 17. Похожие презентации
Карбонатна кислотаВугільна кислота — слабка двоосновна кислота з хімічною формулою . У чистому вигляді нестійка. Утворюється в малих кількостях при розчиненні вуглекислого газу у воді, в тому числі і вуглекислого газу з повітря. Утворює ряд стійких неорганічних та органічних похідних:солі(карбонати та гідрокарбонати), естери, аміди та інші.















Слайд 2
Карбонатна кислота
Вугільна кислота — слабка двоосновна кислота з хімічною формулою . У чистому
Слайд 3
Фізичні властивості
Молекула вугільної кислоти має плоску будову. Центральний
вуглецевий атом має sp ²-гібридизацію. У гідрокарбонат- карбонат-аніонів відбувається делокалізація π-зв'язку. Довжина
зв'язку C — O в карбонат-іоні становить 129 пм.Структурна формула
Кулестрижнева модель
Слайд 4
Розкладання
При підвищенні температури розчину і/або пониженні парціального тиску діоксиду вуглецю
рівновагу в системі зміщується вліво, що призводить до розкладання частини
вугільної кислоти на воду і діоксид вуглецю. При кипінні розчину вугільна кислота розкладається повністю:
Слайд 5
Отримання
Вугільна кислота утворюється при розчиненні у воді діоксиду вуглецю:
Вміст
вугільної кислоти в розчині збільшується при зниженні температури розчину
та збільшенні тиску вуглекислого газу.
Слайд 6
Застосування
Вугільна кислота завжди присутня у водних розчинах вуглекислого газу (см. Газована
вода).
Слайд 7 В біохімії використовується властивість рівноважної системи змінювати тиск газу пропорційно
зміні змісту іонів оксонія(кислотності) при постійній температурі. Це дозволяє реєструвати
в реальному часі хід ферментативних реакцій, що протікають із зміною pH розчину.
Слайд 8
Органічні похідні
Вугільну кислоту формально можна розглядати як карбонову кислоту з гідроксильної групою
замість вуглеводневої залишку. У цій якості вона може утворювати
всі похідні, характерні для карбонових кислот.Карбонові кислоти – органічні сполуки, що містять одну або декілька карбоксильних груп COOH. За кількістю цих груп розрізняють одноосновні (бензойна, оцтова кислота), двоосновні (щавелева,малонова, фталева, азелаїнова кислота) та багатоосновні (лимонна кислота).
Слайд 10
Карбонати
Карбонати - солі й етеривугільної кислоти (наприклад, сода, поташ).
Модель карбонату CO2−3
Слайд 11 Усі карбонати, за винятком карбонатів лужних металів і амонію, у воді
нерозчинні. Більшість карбонатів при нагріванні розкладаються, не плавлячись, на
оксид відповідного металу і діоксид вуглецю.Наприклад:
MgCO3 = MgO CO2↑
Слайд 12 Карбонати лужних металів у термічному відношенні значно стійкіші
і їх можна нагрівати до плавлення без розкладу.
ГІДРОКСИД БАРІЮ
Слайд 13 Гідрокарбонати, на відміну від карбонатів, у воді розчинні.
Вони можуть утворюватись при сумісній дії CO2 і H2O (H2CO3)
на нормальні карбонати.Наприклад:
CaCO3 + CO2 + H2O = Ca(HCO3)2
Слайд 14 У термічному відношенні гідрокарбонати менш стійкі за карбонати
і вже при незначному нагріванні розкладаються, переходячи в нормальні
солі.При дії на карбонати і гідрокарбонати сильних кислот вони, як солі слабкої і нестійкої кислоти, легко розкладаються з виділенням діоксиду вуглецю.
Слайд 15 З солей карбонатної кислоти найбільше практичне значення мають карбонат
натрію (сода кальцинована) Na2CO3,карбонат калію (поташ) K2CO3, гідрокарбонат натрію (питна сода) NaHCO3 і карбонат кальцію (вапняк, крейда,мармур)
CaCO3.Карбонат натрію
Гідрокарбонат натрію





























