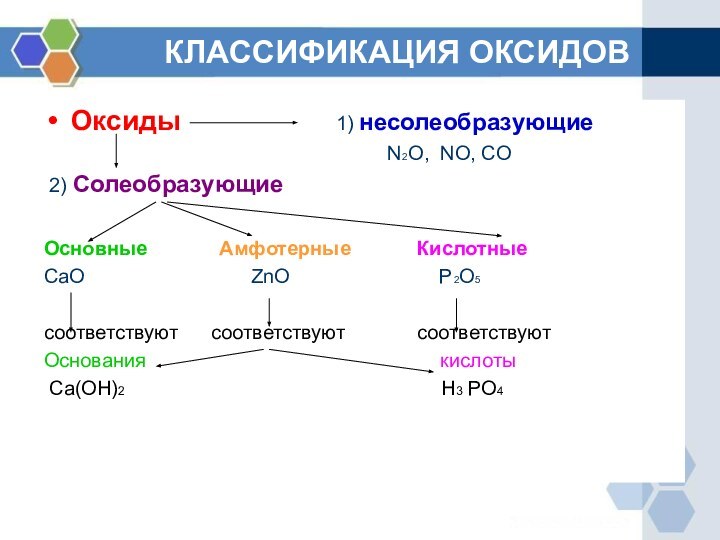
1) несолеобразующие
N2O, NO, CO2) Солеобразующие
Основные Амфотерные Кислотные
CaO ZnO P2O5
соответствуют соответствуют соответствуют
Основания кислоты
Ca(OH)2 H3 PO4
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть