практическое значение водорода?
Где можно использовать знания по
данной теме?Каковы цели урока?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть






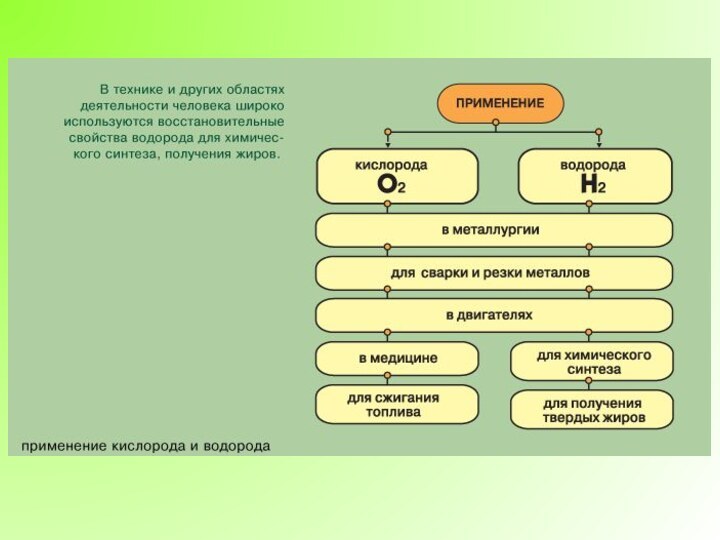






















Применение
Физические свойства