- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Реакции ароматического нуклеофильного замещения
Содержание
- 2. Реакции ароматического нуклеофильного замещения
- 3. Реакции SNArAr-B + C- → ArC + B-
- 4. Ароматические соединения Характерны реакции замещения, в первую
- 5. Нуклеофильное замещение в ароматических и гетероароматических системах
- 6. SNArнуклеофуги - уходящие частицы: Hal-, RO-, NO2-
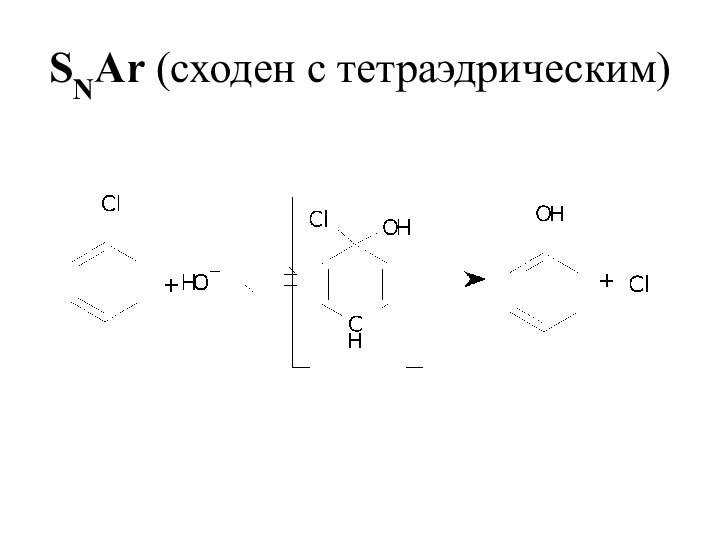
- 7. SNAr (сходен с тетраэдрическим)
- 8. SNArУскоряется в присутствии электроноакцепторных заместителей (особенно в
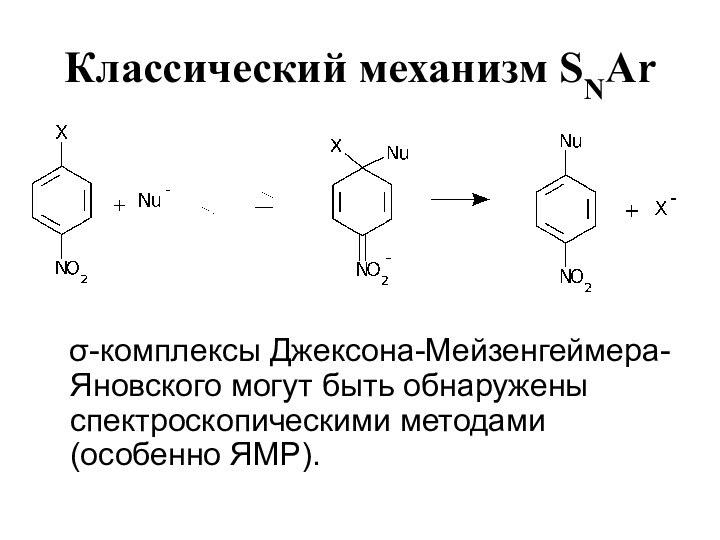
- 9. Классический механизм SNAr σ-комплексы Джексона-Мейзенгеймера-Яновского могут быть обнаружены спектроскопическими методами (особенно ЯМР).
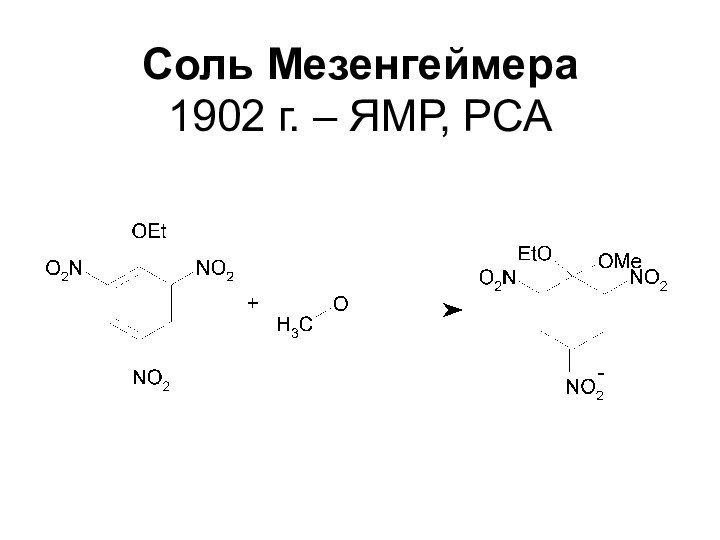
- 10. Соль Мезенгеймера 1902 г. – ЯМР, РСА
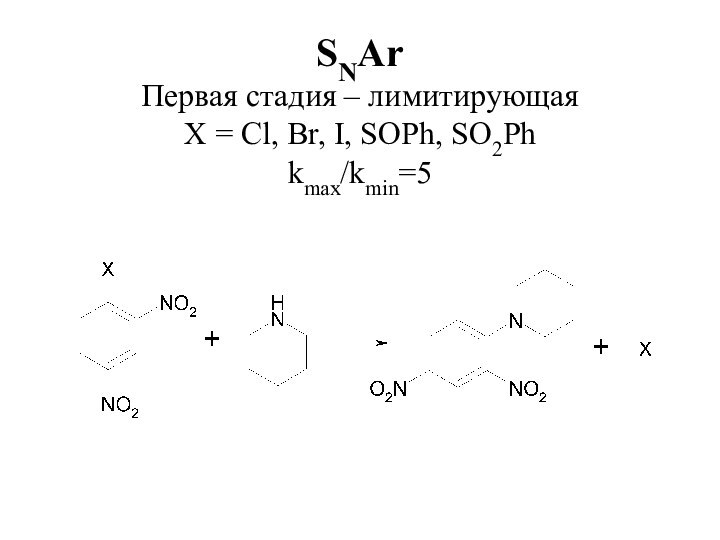
- 11. SNAr Первая стадия – лимитирующая X = Cl, Br, I, SOPh, SO2Ph kmax/kmin=5
- 12. SNAr Реакционная способность уходящих групп F,
- 13. SB-GA (Specific Base - General Acid) Баннет: протекает через образование цвитерионного σ-комплекса (часто депротонирование –лимитирующая стадия)
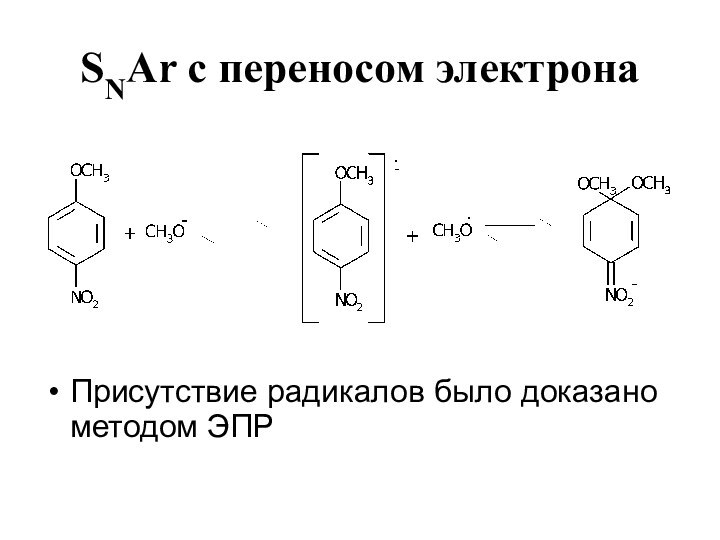
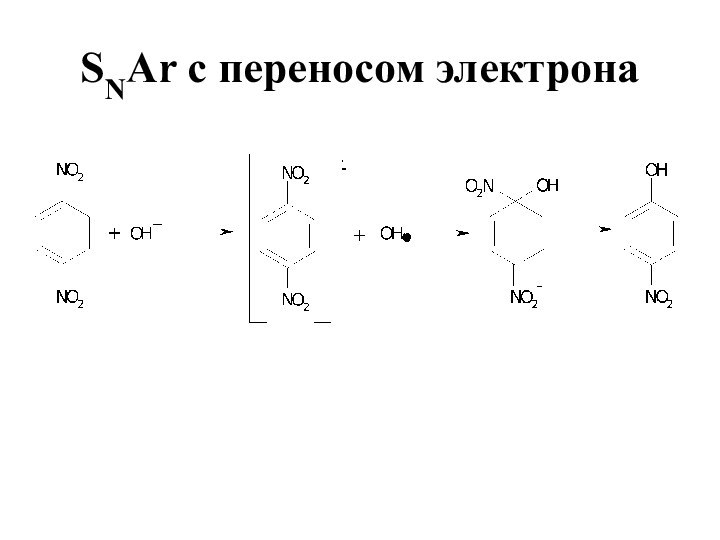
- 14. SNAr с переносом электрона Присутствие радикалов было доказано методом ЭПР
- 15. SNAr с переносом электрона
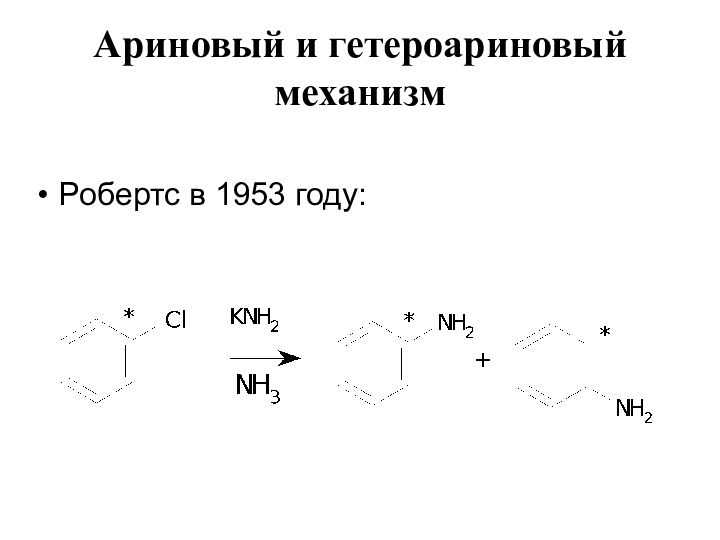
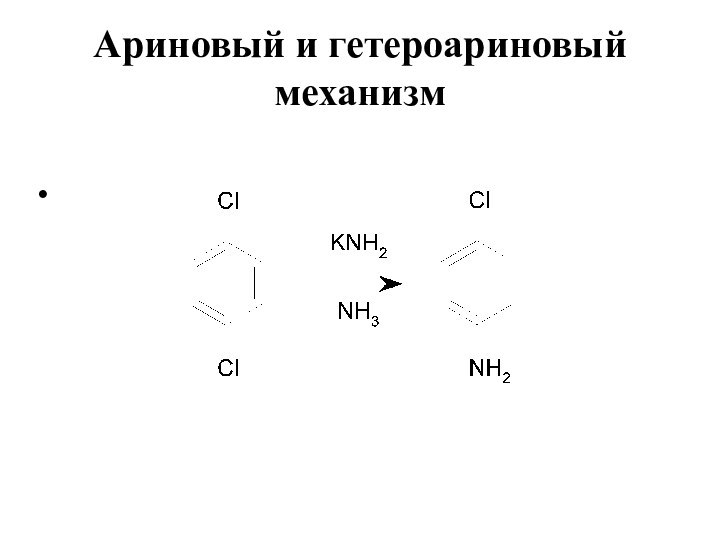
- 16. Ариновый и гетероариновый механизм Робертс в 1953 году:
- 17. Ариновый и гетероариновый механизм побочные реакции циклоприсоединения,
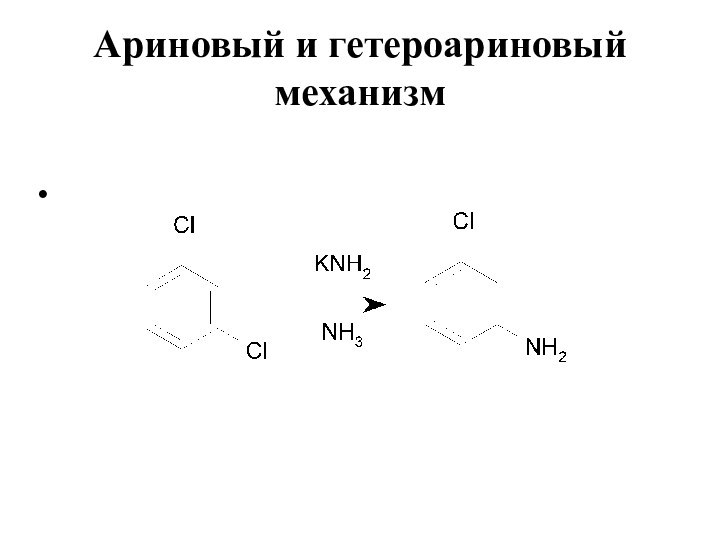
- 18. Ариновый и гетероариновый механизм
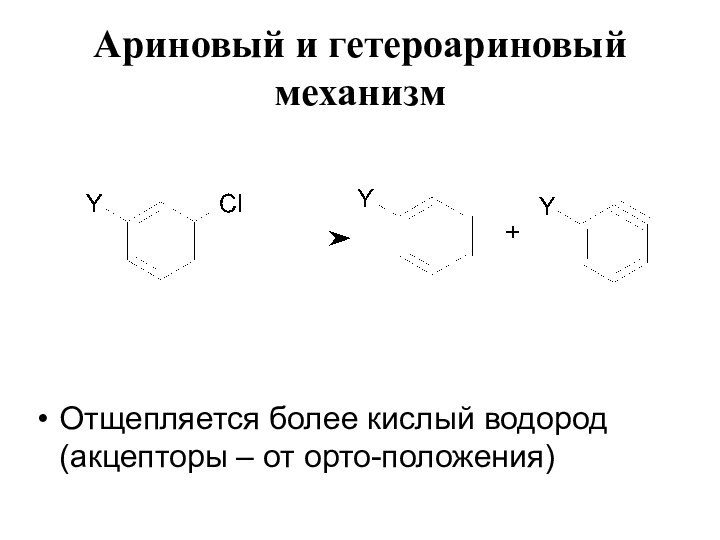
- 19. Ариновый и гетероариновый механизм Отщепляется более кислый водород (акцепторы – от орто-положения)
- 20. Ариновый и гетероариновый механизм
- 21. Ариновый и гетероариновый механизм
- 22. Ариновый и гетероариновый механизм
- 23. Механизм SRN1Баннет и Ким1970 г.
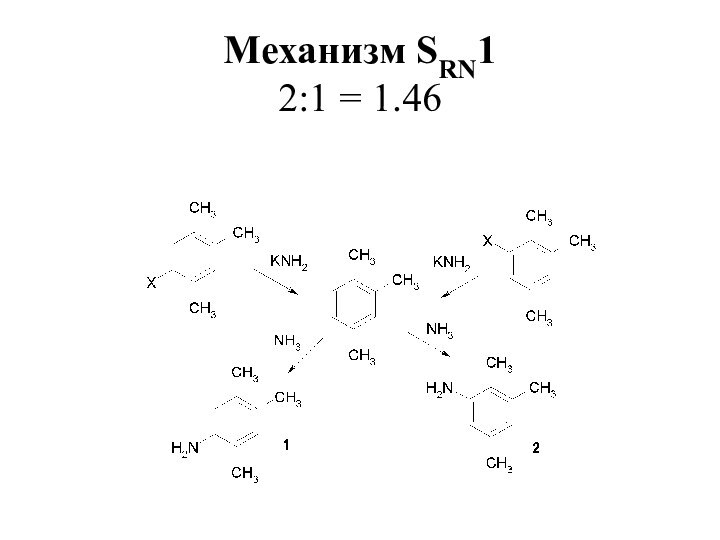
- 24. Механизм SRN1 2:1 = 1.46
- 25. Механизм SRN1Для йода2:1 = 0.63 или 2:1
- 26. SRN1ArX + e → [ArX]-.[ArX]-. → Ar.
- 27. SRN1Не нужна активация сильно электроноакцепторными группамиОтсутствует чувствительность к стерическим препятствиямЭффективно фотостимулирование или электрохимическое инициирование
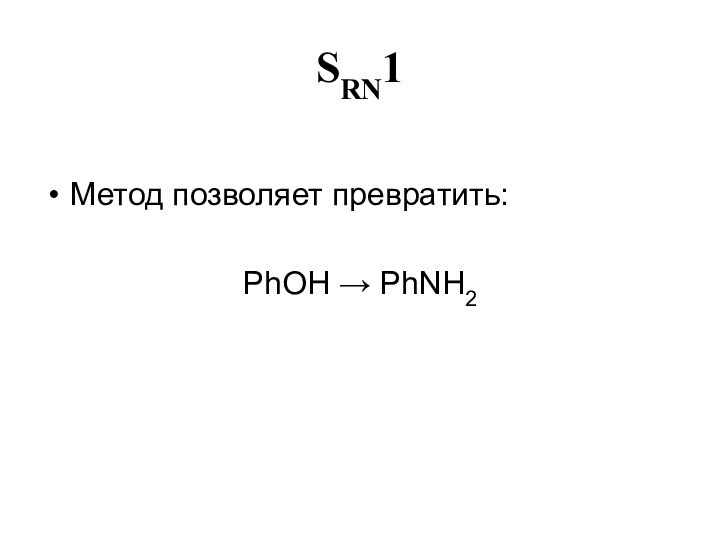
- 28. SRN1Метод позволяет превратить:PhOH → PhNH2
- 29. SN1Ar ArN2+ → N2 +
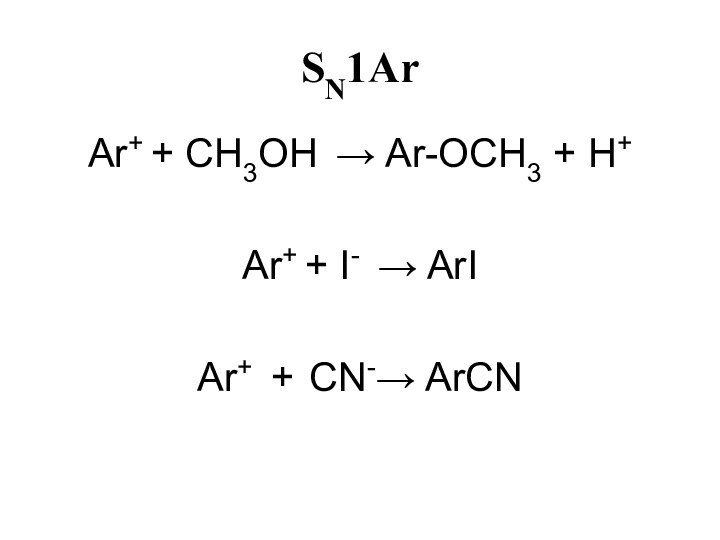
- 30. SN1Ar Ar+ + CH3OH → Ar-OCH3 + H+Ar+ + I- → ArIAr+ + CN-→ ArCN
- 31. SN1Ar1) Скорость не зависит от [Nu]2) Влияние
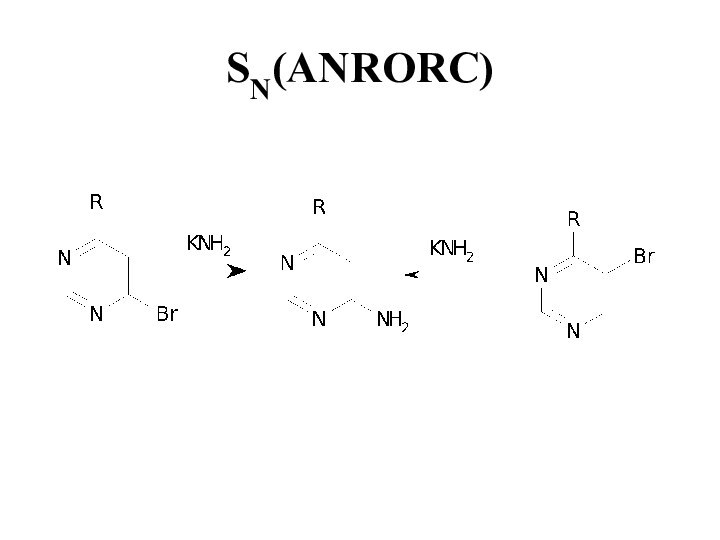
- 32. SN(ANRORC) Этот механизм был открыт Ван-дер-Плассом в
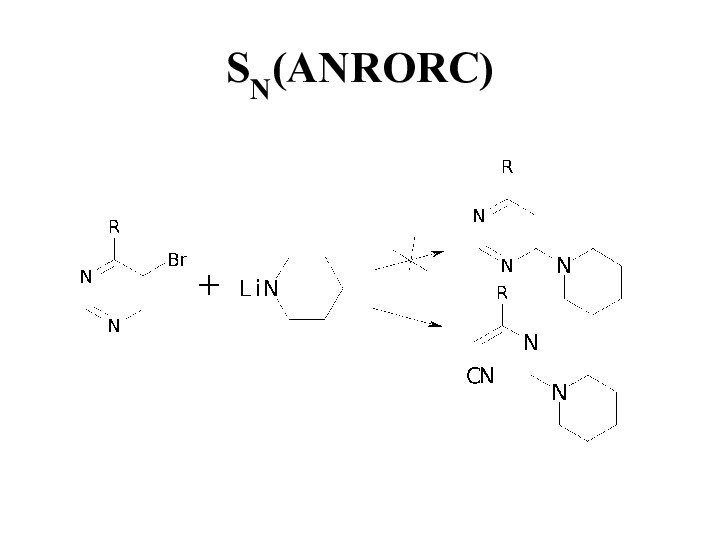
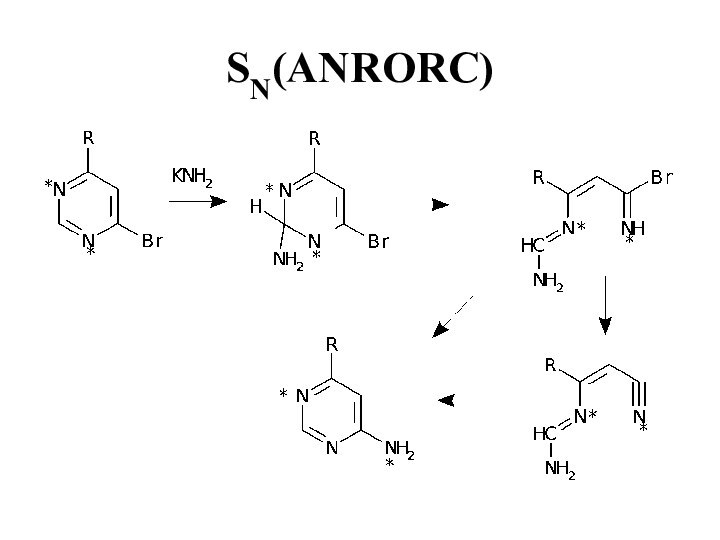
- 33. SN(ANRORC)
- 34. SN(ANRORC)
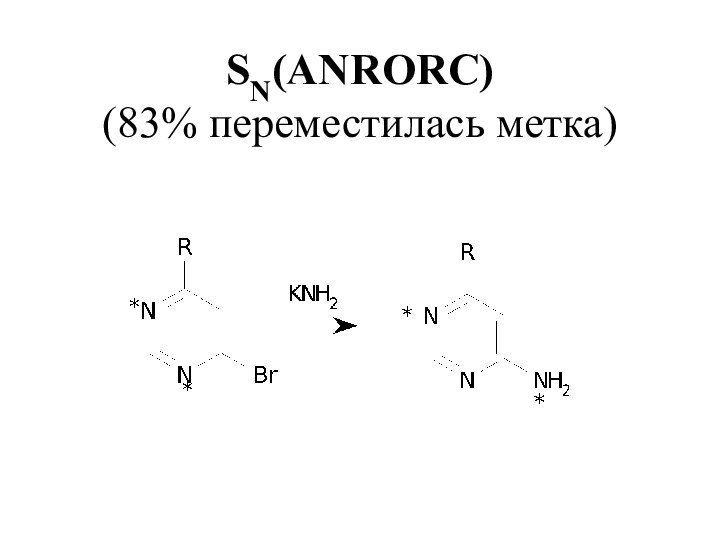
- 35. SN(ANRORC) (83% переместилась метка)
- 36. SN(ANRORC)
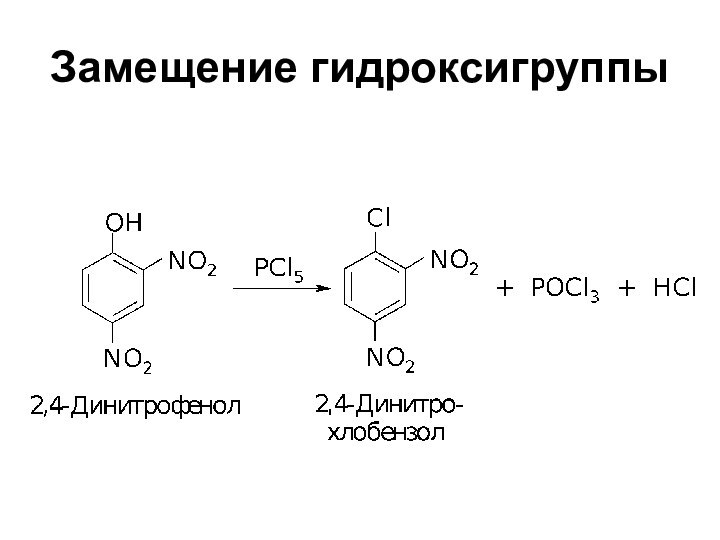
- 37. Замещение гидроксигруппы
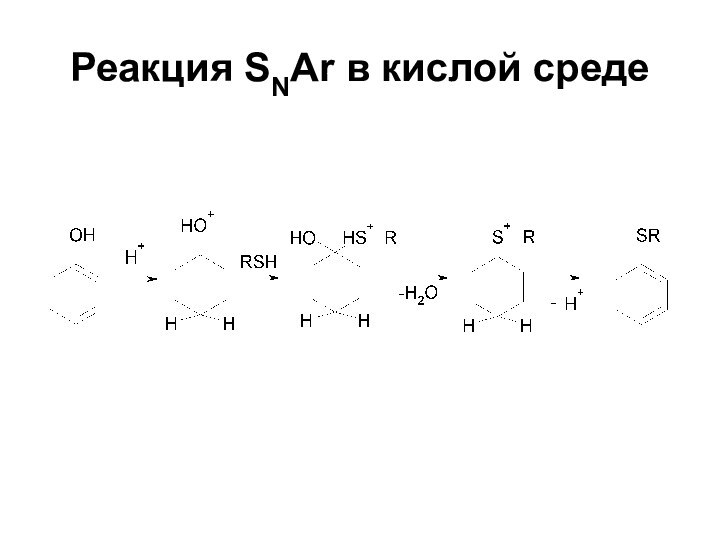
- 38. Реакция SNAr в кислой среде
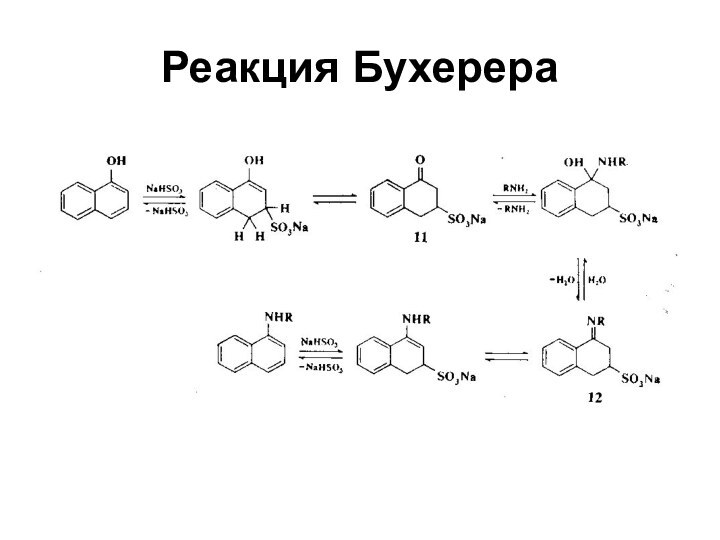
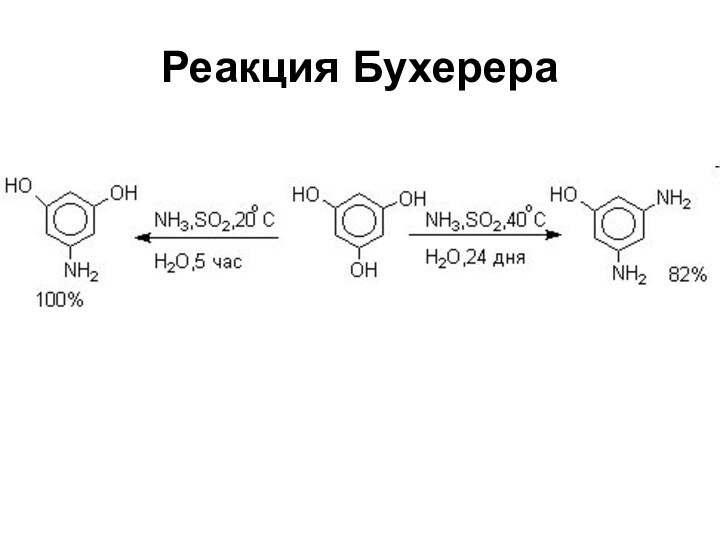
- 39. Реакция Бухерера
- 40. Реакция Бухерера
- 41. Реакция УльманаArI + Cu → ArCuArCu + ArI → ArAr
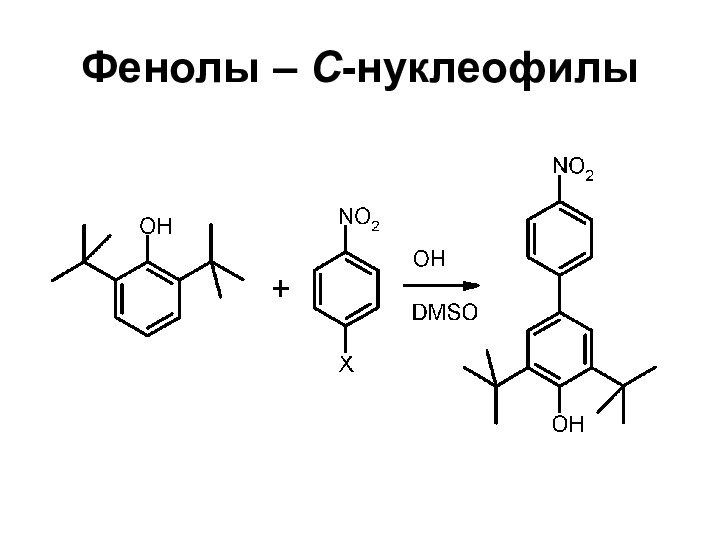
- 42. Фенолы – С-нуклеофилы
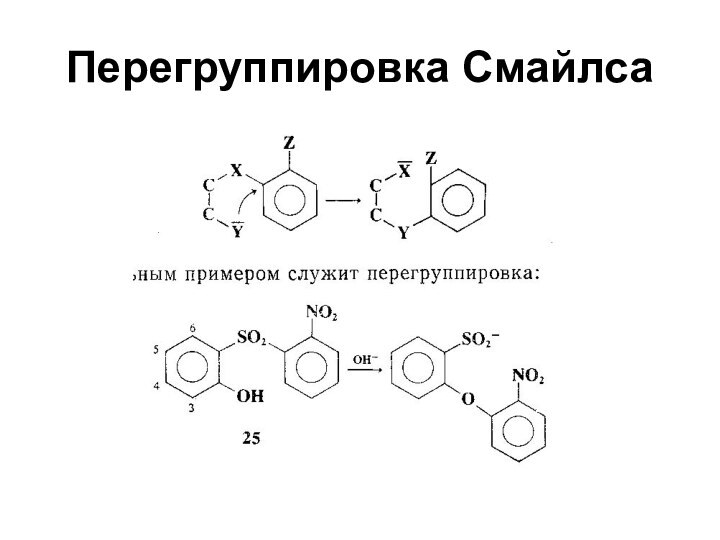
- 43. Перегруппировка Смайлса
- 44. Реакция УльманаAr-I + Cu → ArCuArCu + Ar-I → Ar-Ar
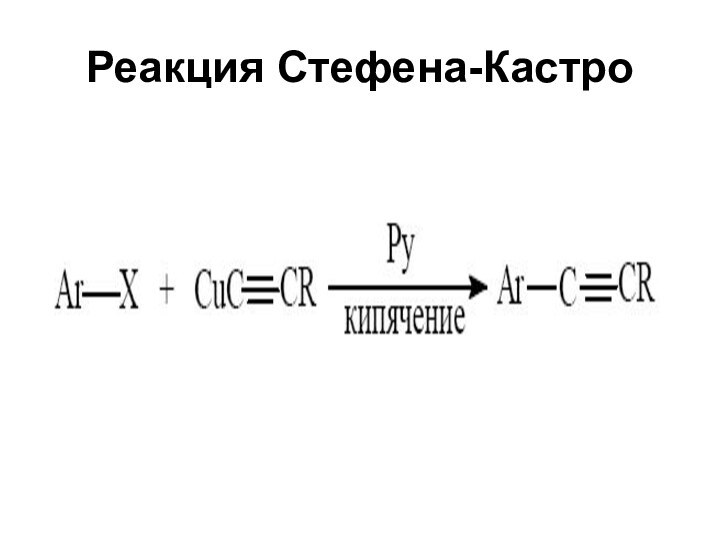
- 45. Реакция Стефена-Кастро
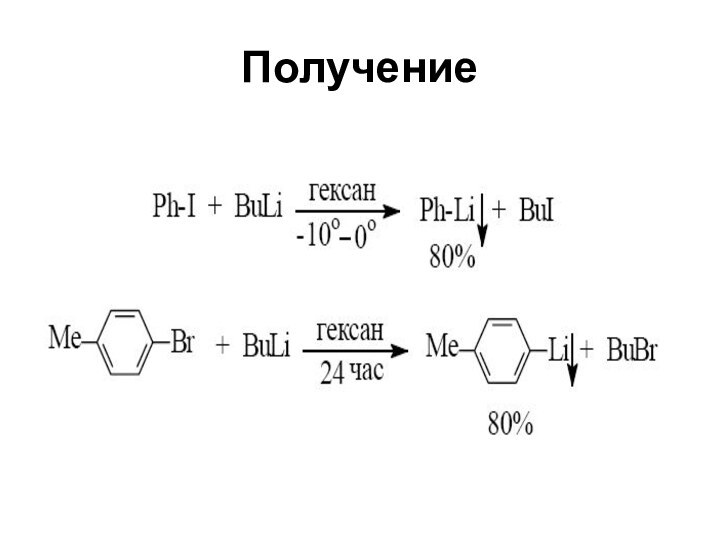
- 46. Получение
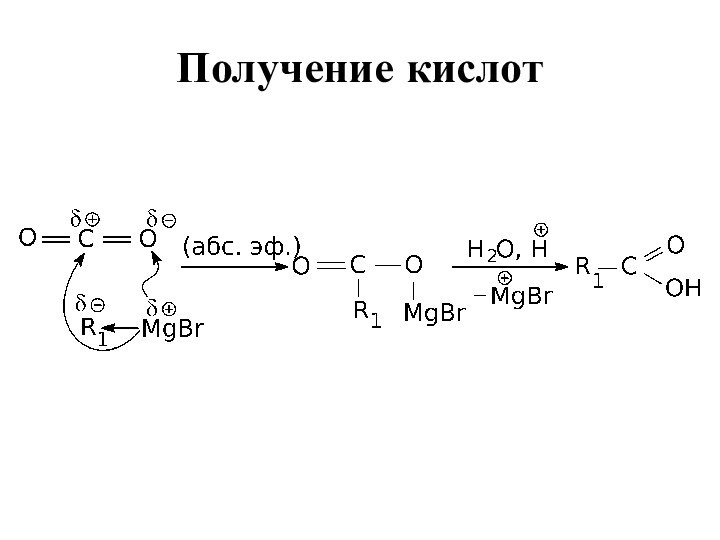
- 47. Получение кислот
- 48. Скачать презентацию
- 49. Похожие презентации
Реакции ароматического нуклеофильного замещения










![Реакции ароматического нуклеофильного замещения SRN1ArX + e → [ArX]-.[ArX]-. → Ar. + X-Ar. + Y- →](/img/tmb/11/1088230/8a713a8246b827c3293b99d443a9620a-720x.jpg)

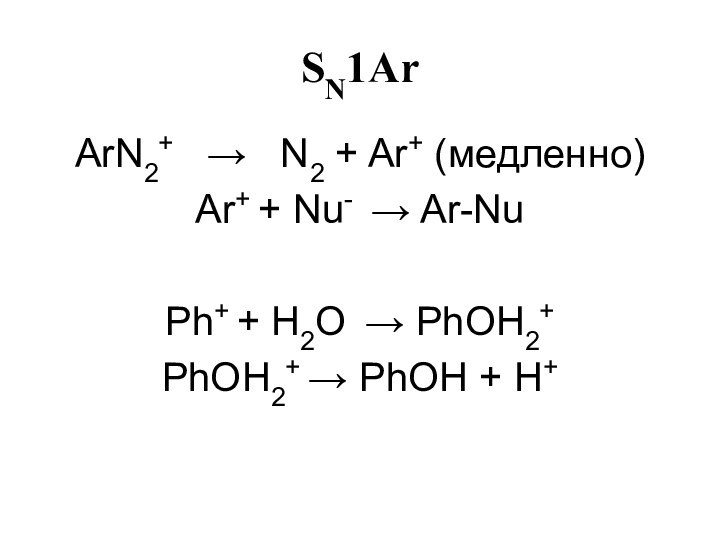
![Реакции ароматического нуклеофильного замещения SN1Ar1) Скорость не зависит от [Nu]2) Влияние заместителей в ароматическом](/img/tmb/11/1088230/f16876ab7a85ac025aae0defdc4e704a-720x.jpg)




Слайд 5
Нуклеофильное замещение в ароматических и гетероароматических системах
1)
реакции, активируемые электроноакцепторными группами в орто- и пара-положениях к
уходящей группе;2) реакции, катализируемые очень сильными основаниями и протекающие через образование ариновых интермедиатов;
3) реакции, инициируемые донорами электронов;
4) реакции, в которых азот в соли диазония замещается нуклеофилом
Слайд 6
SNAr
нуклеофуги - уходящие частицы:
Hal-, RO-, NO2- и
др., в том числе и водород.
Эта область органической
химии в последние десятилетия особенно интенсивно развивается, в ней было открыто несколько новых механизмов.
Слайд 8
SNAr
Ускоряется в присутствии электроноакцепторных заместителей (особенно в орто-
и пара-положениях), катализаторов, π-коплексованием, в гетероциклах атомом азота (α
и γ-положения), N-оксидной функциейТормозится в присутствии электронодонорных заместителей
Слайд 9
Классический механизм SNAr
σ-комплексы Джексона-Мейзенгеймера-Яновского могут быть
обнаружены спектроскопическими методами (особенно ЯМР).
Слайд 12 SNAr Реакционная способность уходящих групп F, NO2, OTs, SOPh,
Cl, Br, I, N3, OAr, OR, SR, SO2R, NH2
Слайд 13
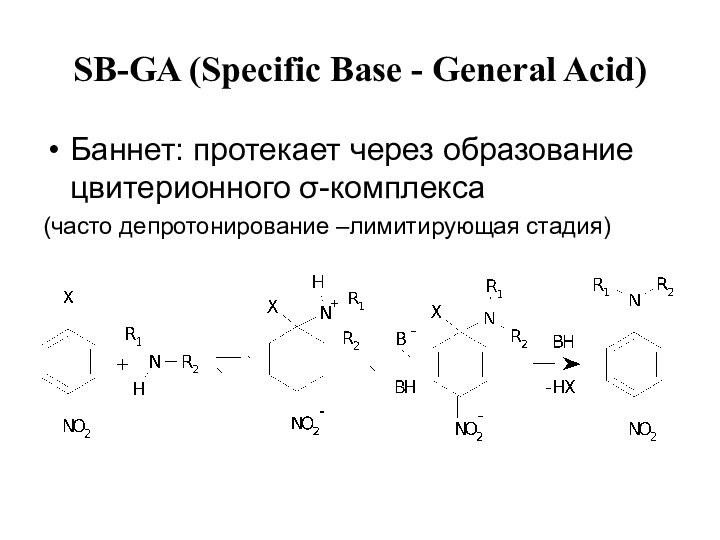
SB-GA (Specific Base - General Acid)
Баннет: протекает
через образование цвитерионного σ-комплекса
(часто депротонирование –лимитирующая стадия)
Слайд 17
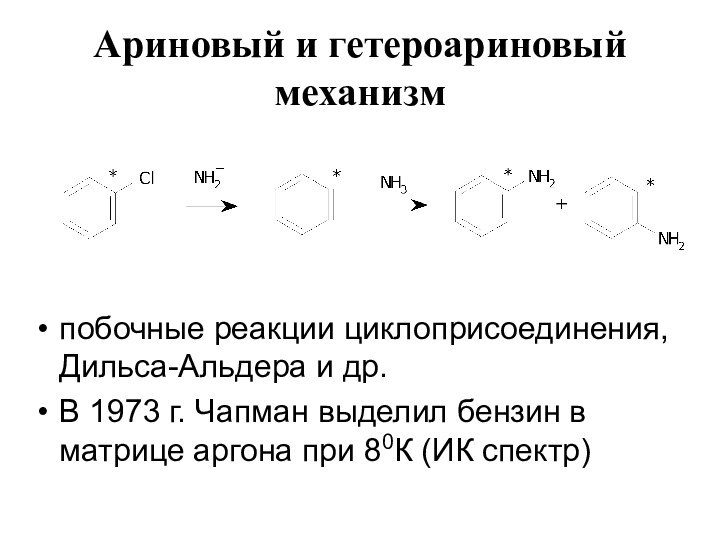
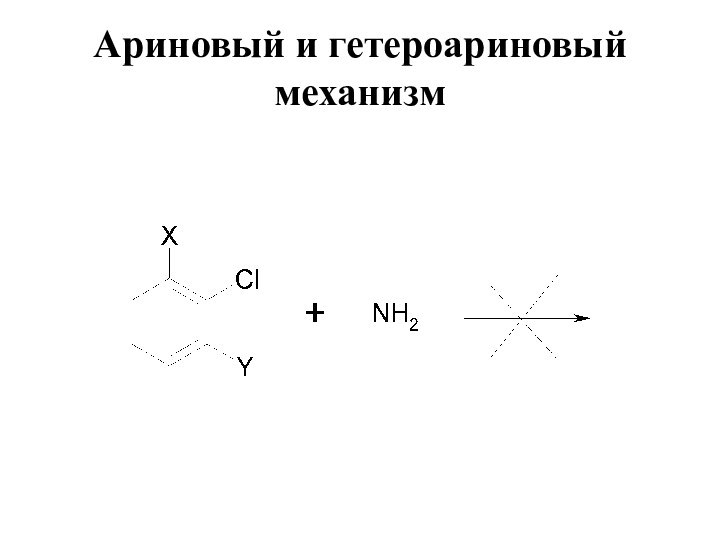
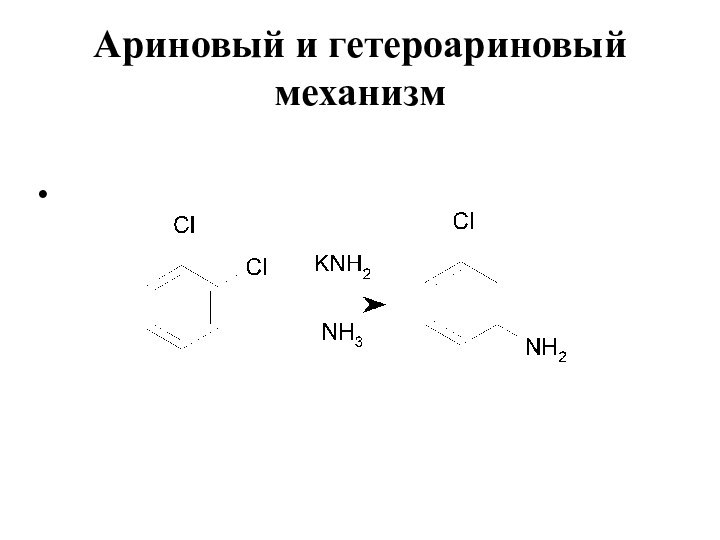
Ариновый и гетероариновый механизм
побочные реакции циклоприсоединения,
Дильса-Альдера и др.
В 1973 г. Чапман выделил бензин
в матрице аргона при 80К (ИК спектр)





























