связи в комплексных соединениях.
2. Изучить реакции
комплексных соединений и факторы, влияющие на устойчивость.3. Рассмотреть применение комплексных соединений в военно-химической практике.
Основная литература:
Н.С. Ахметов. Общая и неорганическая химия. М.: Высшая школа . 2003. С. 206-208.
2. Общая и неорганическая химия. Учебное пособие. СВИРХБЗ.
Ч 3. 2003. C. 83-96.
Дополнительная литература:
Учебная программа по дисциплине «Общая и неорганическая химия». 2001. 19 с.
2. М.И. Сафарова. Общая и неорганическая химия в схемах и таблицах. Ч.1. Теоретические основы неорганической химии. Учебное пособие. Саратов. СВИРХБЗ. 2006. С. 80.





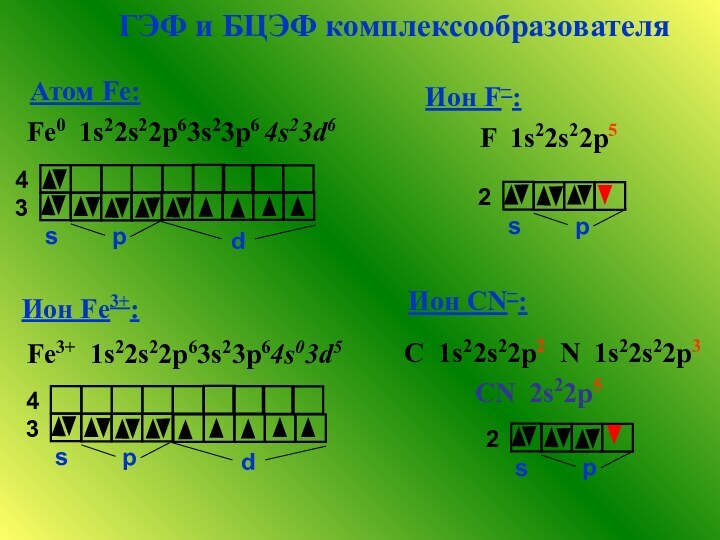
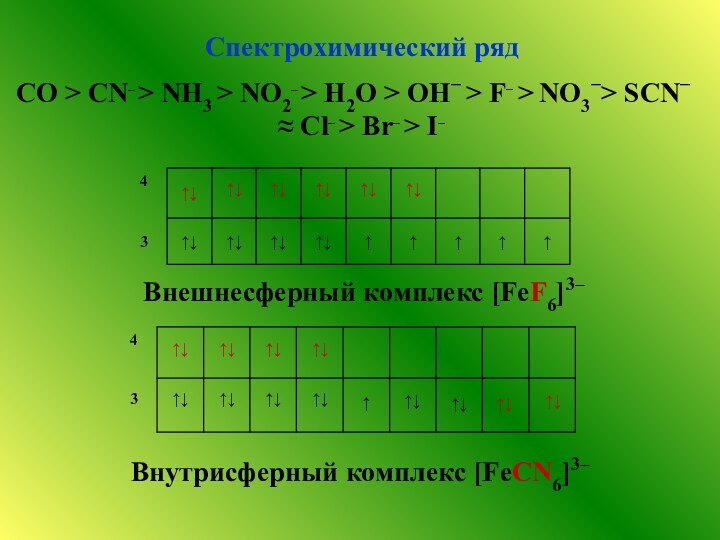
![Свойства комплексных соединений [Co(H2O)6]2+ розовый[Co(CH3COO)2] ярко-розовый [Co(NO2)6]4-](/img/tmb/12/1104411/47df122a02bdf6bcefd873d19e789006-720x.jpg)

![Свойства комплексных соединений K3[Fe(CN)6] 3K+ + [Fe(CN)6]3-](/img/tmb/12/1104411/0e3de21bb42cab6b8b929a56f5a82e62-720x.jpg)
![Свойства комплексных соединений [Ag(NH3)2]+ [Ag(NH3)]+ + NH3[Ag(NH3)2]+](/img/tmb/12/1104411/df2ffb1543cf6eaa0bdb2e401701d3cc-720x.jpg)
![Свойства комплексных соединений Реакции комплексных соединенийпо внешней сфере2K3[Fe(CN)6] + 3FeSO4 =](/img/tmb/12/1104411/39f27ae09c2f1e6ab7f2da76e34d9447-720x.jpg)


![Свойства комплексных соединений 3. Разбавление K[AgCl2] = KCl + AgCl↓ 5. Окислительно-восстановительные](/img/tmb/12/1104411/2da0c13b5208090f6a587df73a1e6a3c-720x.jpg)

![Свойства комплексных соединений При одинаковом координационном числе Сравнение прочности комплексовпо общим константам нестойкости [Fe(SCN)6]3- +](/img/tmb/12/1104411/7150a94492e08bb703cc667f96b9d9c4-720x.jpg)