Слайд 2
Цель: экспериментальное подтверждение пригодности методик количественного
определения ранитидина в таблеках Ранитидин-ЛекТ и эргокальциферола (витамина Д2)
в препарате Эргокальциферол-ЛекТ методом ВЭЖХ.
Задачи:
предварительное тестирование методик количественного определения ранитидина и эргокальциферола методом ВЭЖХ;
подбор условий анализа;
проведение работ по подтверждению пригодности выбранных методик;
статистическая обработка полученных данных и занесение результатов исследования в протокол предприятия.
Слайд 3
Метод анализа
Высокоэффективная жидкостная хроматография — один из эффективных
методов
разделения сложных смесей веществ.
В обращенно-фазовом варианте хроматографии используют неполярные химически модифицированные сорбенты
(например, неполярный алкильный радикал C18) и полярные подвижные фазы (например, метанол, ацетонитрил).
Слайд 4
Подтверждение пригодности аналитической методики количественного определения ранитидина методом
ВЭЖХ в препарате Ранитидин-ЛекТ
4
Слайд 5
Препарат применяется для профилактики и лечения язвенной болезни
желудка и /или двенадцатиперстной кишки, в том числе связанной
с приемом нестероидных противовоспалительных препаратов (НПВП).
Ранитидина гидрохлорид
Слайд 7
Краткое изложение методики анализа
Раствор стандартного образца ранитидина
гидрохлорида
Около 55 мг (точная
навеска) стандартного образца (BP CRS, USP RS) ранитидина гидрохлорида, помещают в мерную колбу вместимостью 50 мл, растворяют в 40 мл метанола, доводят объем раствора метанолом до метки и перемешивают.
Затем 1,0 мл полученного раствора помещают в мерную колбу вместимостью 25 мл, доводят объем раствора подвижной фазой до метки и перемешивают.
Испытуемый раствор
Около 100 мг (точная навеска) порошка растертых таблеток помещают в мерную колбу вместимостью 50 мл, прибавляют 40 мл подвижной фазы, помещают в ультразвуковую ванну на 15 мин, доводят объем суспензии подвижной фазой до метки, перемешивают и фильтруют через мембранный фильтр с диаметром пор не более 0,45 мкм, отбрасывая первые порции фильтра.
Затем 1,0 мл фильтрата переносят в мерную колбу вместимостью 25 мл, доводят объем раствора подвижной фазой до метки и перемешивают.
Слайд 8
Содержание С13Н22N4О3S (ранитидина) должно быть от 142 до
158 мг, считая на среднюю массу таблетки.
Содержание (Х)
вычисляют по формуле:
S – площадь пика ранитидина на хроматограмме испытуемого раствора;
S0 – площадь пика ранитидина на хроматограмме раствора стандартного образца ранитидина гидрохлорида;
а0 – навеска стандартного образца ранитидина гидрохлорида (мг);
а – навеска порошка растертых таблеток (мг);
G – средняя масса одной таблетки (мг);
Р – содержание ранитидина гидрохлорида в стандартном образце (%);
0,896 – коэффициент пересчета ранитидина гидрохлорида на ранитидин
Слайд 9
Проведение проверки методики на соответствие критериям специфичности
Р -
растворитель, не содержащий определяемых компонентов;
С1 - раствор плацебо;
С2 -
раствор ранитидина гидрохлорида концентрацией 0,08 мг/мл
С3 - испытуемый раствор таблеток Ранитидин – ЛекТ 150 мг.
Слайд 10
Проведение проверки методики на соответствие критериям прецизионности (сходимость)
Средняя
масса таблетки 316 мг
Стандартное отклонение для 6 определений (n=6)
SD =0,87
Относительное стандартное отклонение RSD = 0,55 %
Доверительный интервал ∆x = 1,0 (критерий Стьюдента t = 2,57 для f = 5 и P = 95%)
Содержание ранитидина в таблетке x = 156,9 ± 1,0 мг
Слайд 11
Проведение проверки методики на соответствие
критериям прецизионности (воспроизводимость)
Средняя масса таблетки 316 мг
Стандартное отклонение для
6 определений (n=6) SD =0,84
Относительное стандартное отклонение RSD = 0,53 %
Доверительный интервал ∆x = 0,96 (критерий Стьюдента t = 2,57 для f = 5 и P = 95%)
Содержание ранитидина в таблетке x = 156,64 ± 0,96 мг
Слайд 12
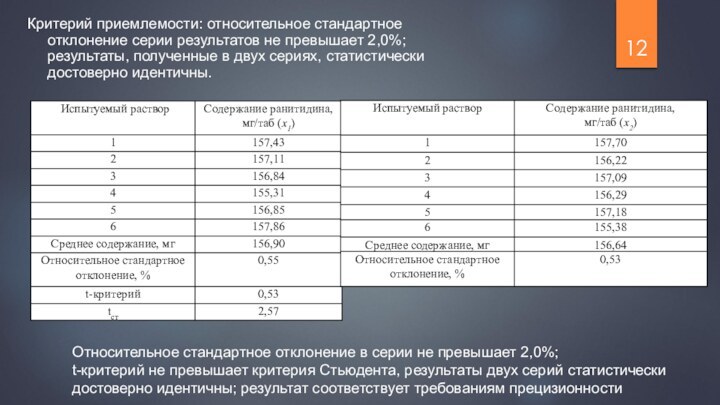
Критерий приемлемости: относительное стандартное отклонение серии результатов не
превышает 2,0%; результаты, полученные в двух сериях, статистически достоверно
идентичны.
Относительное стандартное отклонение в серии не превышает 2,0%;
t-критерий не превышает критерия Стьюдента, результаты двух серий статистически достоверно идентичны; результат соответствует требованиям прецизионности
Слайд 13
Проведение проверки методики на соответствие критериям линейности
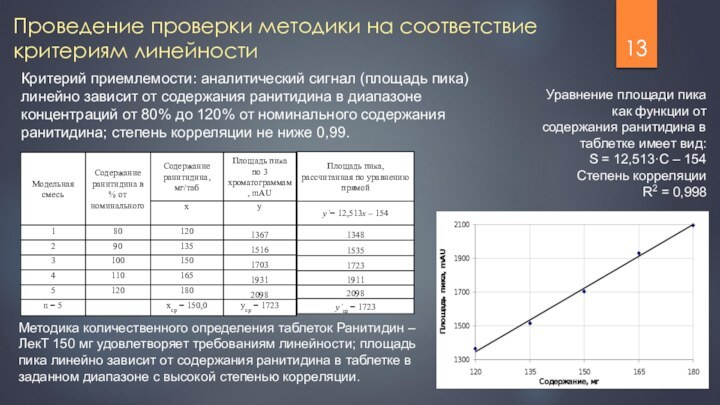
Критерий приемлемости:
аналитический сигнал (площадь пика) линейно зависит от содержания ранитидина
в диапазоне концентраций от 80% до 120% от номинального содержания ранитидина; степень корреляции не ниже 0,99.
Уравнение площади пика как функции от содержания ранитидина в таблетке имеет вид:
S = 12,513·С – 154
Степень корреляции
R2 = 0,998
Методика количественного определения таблеток Ранитидин – ЛекТ 150 мг удовлетворяет требованиям линейности; площадь пика линейно зависит от содержания ранитидина в таблетке в заданном диапазоне с высокой степенью корреляции.
Слайд 14
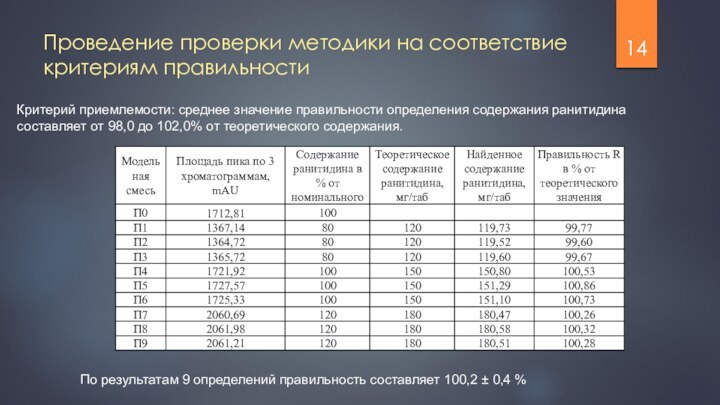
Проведение проверки методики на соответствие критериям правильности
Критерий приемлемости:
среднее значение правильности определения содержания ранитидина составляет от 98,0
до 102,0% от теоретического содержания.
По результатам 9 определений правильность составляет 100,2 ± 0,4 %
Слайд 15
Определение диапазона применения
Критерий приемлемости: в заданном диапазоне выполняются
условия линейности, правильности, прецизионности.
Диапазон применения методики количественного определения таблеток
Ранитидин – ЛекТ 150 мг составляет 120 – 180 мг ранитидина в таблетке
Слайд 16
Опробация методики количественного определения эргокальциферола (витамин Д2) раствор
[в масле] 0,0625 % методом ВЭЖХ
Слайд 17
Эргокальциферол (витамин Д2)
Одна из форм витамина Д, образующаяся
при воздействии ультрафиолета на эргостерол.
Неустойчив к влиянию света,
высоких темпаратур, кислорода воздуха. Регулирует обмен кальция и фосфора в организме.
Слайд 18
Хроматографические условия и условия пригодности системы (исходная методика)
эффективность колонки, рассчитанная по пику эргокальциферола, должна быть не
менее 1500 теоретических тарелок;
относительное стандартное отклонение площади пика не должно превышать 1,5 %;
относительное стандартное отклонение времени удерживания не должно превышать 2 %.
Слайд 19
Краткое изложение методики анализа
Раствор стандартного образца эргокальциферола:
Около 0,006
г (точная навеска) стандартного образца эргокальциферола (ЕР, USP, рабочий
стандарт фирмы) помещают в мерную колбу вместимостью 50 мл, приливают примерно 10 мл спирта изопропилового, растворяют, затем доводят объем раствора спиртом изопропиловым до метки, перемешивают.
Испытуеый раствор:
2,5 мл препарата помещают в мерную колбу вместимостью 50 мл, приливают спирт изопропиловый примерно 10 мл, растворяют, затем доводят объем раствора спиртом изопропиловым до метки, перемешивают.
Слайд 20
Содержания эргокальциферола (Х,мг/мл) вычисляют по формуле:
S - площадь
пика эргокальциферола на хроматограмме испытуемого раствора;
S0 - площадь пика
эргокальциферола на хроматограмме раствора стандартного образца эргокальциферола;
а - навески стандартного образца эргокальциферола, (мг);
Р - содержание эргокальциферола в стандартном образце, %.
Содержание эргокальциферола 1 мл должно составлять от 0,58 до 0,67 мг.
Слайд 21
Подбор хроматографических условий
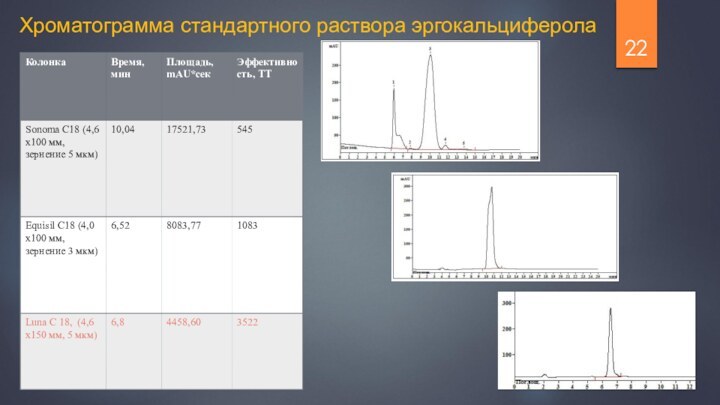
Слайд 22
Хроматограмма стандартного раствора эргокальциферола
Слайд 23
Хроматограмма стандартного раствора эргокальциферола
Колонка Equisil C18 (4,0х100 мм,
зернение 3 мкм)
Времена удерживания основного компонента не совпадают между
вводом проб, также по параметру эффективность колонка не удовлетворяет условиям анализа.
Слайд 24
Колонка Luna C18 (4,6х150 мм, зернение 5 мкм)
Хроматограмма
стандартного раствора эргокальциферола
Относительное стандартное отклонение по площади пиков RSD=0,03%
(не более 1,5%).
Относительное стандартное отклонение по времени удерживания RSD=1,08% (не более 2%)
Выбранная колонка удовлетворяет критериям пригодности хроматографической системы.
Слайд 25
Проведение проверки методики на соответствие критериям специфичности
Р –
раство-ритель
С1 – стандартный раствор эргокальци-
ферола
С2 - раствор плацебо
С3
- испытуемый раствор готового лекарственного средства Эргокальциферол-ЛекТ .
Слайд 26
Проведение проверки методики на соответствие критериям специфичности
Слайд 27
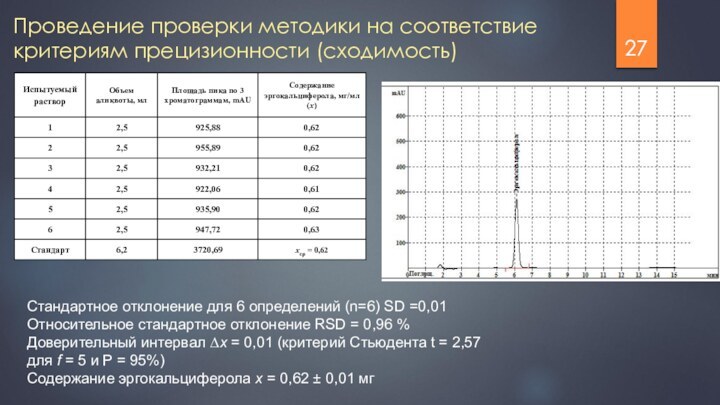
Проведение проверки методики на соответствие критериям прецизионности (сходимость)
Стандартное
отклонение для 6 определений (n=6) SD =0,01
Относительное стандартное
отклонение RSD = 0,96 %
Доверительный интервал ∆x = 0,01 (критерий Стьюдента t = 2,57 для f = 5 и P = 95%)
Содержание эргокальциферола x = 0,62 ± 0,01 мг
Слайд 28
Проведение проверки методики на соответствие
критериям прецизионности (воспроизводимость)
Стандартное отклонение для 6 определений (n=6) SD
=0,003
Относительное стандартное отклонение RSD = 0,51 %
Доверительный интервал ∆x = 0,003 (критерий Стьюдента t = 2,57 для f = 5 и P = 95%)
Содержание эргокальциферола x = 0,62 ± 0,003 мг
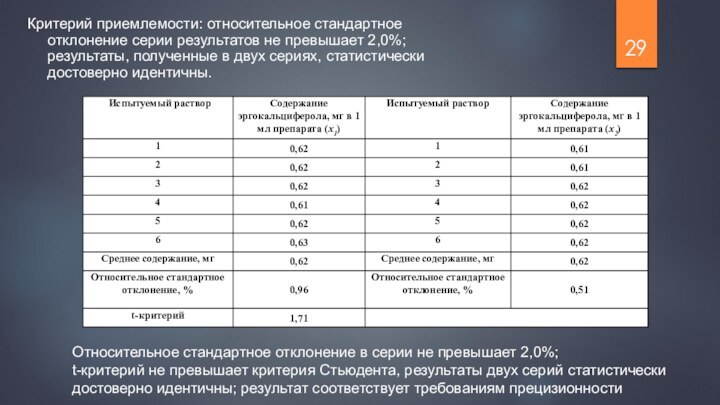
Слайд 29
Критерий приемлемости: относительное стандартное отклонение серии результатов не
превышает 2,0%; результаты, полученные в двух сериях, статистически достоверно
идентичны.
Относительное стандартное отклонение в серии не превышает 2,0%;
t-критерий не превышает критерия Стьюдента, результаты двух серий статистически достоверно идентичны; результат соответствует требованиям прецизионности
Слайд 30
Проведение проверки методики на соответствие критериям линейности
Критерий приемлемости:
аналитический сигнал (площадь пика) линейно зависит от содержания витамина
Д2 в диапазоне концентраций от 80% до 120% от номинального содержания; степень корреляции не ниже 0,99.
Уравнение площади пика как функции от содержания эргокальциферола в таблетке имеет вид:
S = y = 1341⋅С+ 53,866
Степень корреляции
R2 = 0,999
Методика количественного определения Эргокальциферол-ЛекТ удовлетворяет требованиям линейности; площадь пика линейно зависит от содержания эргокальциферола в препарате в заданном диапазоне с высокой степенью корреляции
Слайд 31
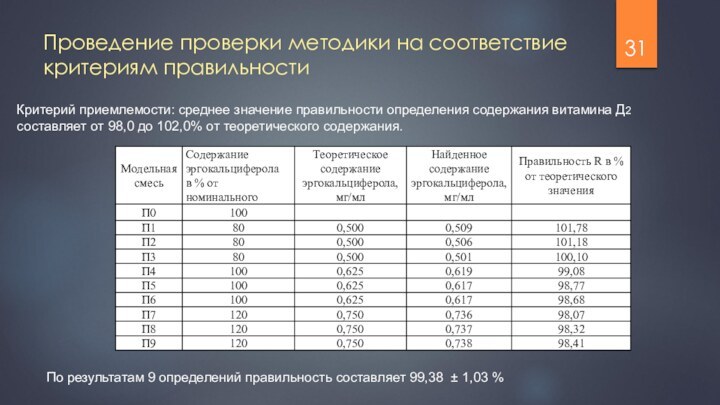
Проведение проверки методики на соответствие критериям правильности
Критерий приемлемости:
среднее значение правильности определения содержания витамина Д2 составляет от
98,0 до 102,0% от теоретического содержания.
По результатам 9 определений правильность составляет 99,38 ± 1,03 %
Слайд 32
Определение диапазона применения
Критерий приемлемости: в заданном диапазоне выполняются
условия линейности, правильности, прецизионности.
диапазон применения методики количественного определения Эргокальциферол-ЛекТ
составляет 0,50-0,75 мг эргокальциферола в 1 мл препарата
Слайд 33
Результаты
В результате проведенной работы были протестированы методики количественного
определения ранитидина и эргокальциферола методом ВЭЖХ;
Подобраны оптимальные условия анализа;
Выполнена
проверка аналитических методик по таким критериям как специфичность,прецизионность, правильность, линейность, определен диапазон применения данных методик;
Проведена статистическая обработка полученных данных
По итогу валидационных работ было сделано заключение о возможности применения данных аналитических методик для дальнейшего анализа препаратов Ранитидин-ЛекТ и Эргокальциферол-ЛекТ на предприятии.
Слайд 36
Устройство жидкостного хроматографа
1. узел подготовки подвижной фазы, включая емкость
с подвижной фазой (или емкости с отдельными растворителями, входящими
в состав подвижной фазы) и систему дегазации подвижной фазы;
2. насосная система предназначена для создания постоянного потока растворителя;
3. смеситель подвижной фазы;
4. система ввода пробы (инжектор), может быть ручным или автоматическим (автосамплер) обеспечивает ввод пробы смеси разделяемых компонентов в колонку с достаточно высокой воспроизводимостью;
5. хроматографическая колонка;
6. термостат обеспечивает постоянство выбранного температурного режима;
7. детектор (один или несколько с разными способами детектирования);
8. система управления хроматографом, сбора и обработки данных.












![Высокоэффективная жидкостная хроматография в анализе готовых лекарственных форм и контроле технологии их производства Опробация методики количественного определения эргокальциферола (витамин Д2) раствор [в масле] 0,0625 % методом ВЭЖХ](/img/tmb/15/1427967/fd303377656bccc661522ef3d72c0a12-720x.jpg)