Слайд 2
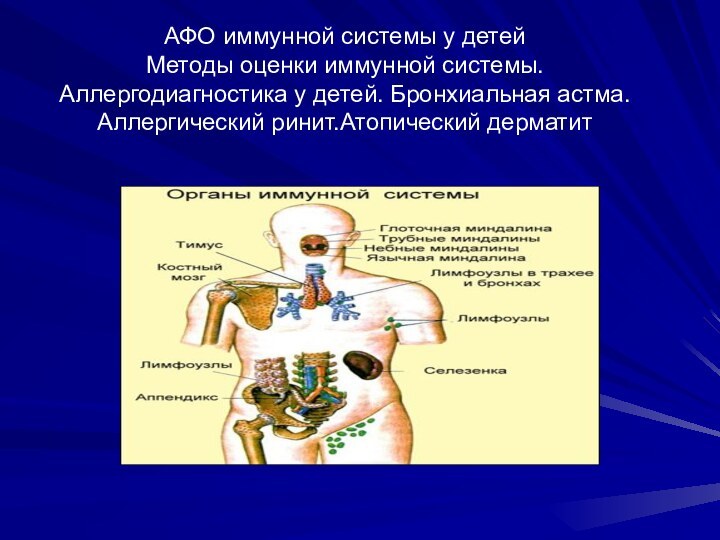
Органы иммунной системы
разделяют на центральные и периферические.
К
центральным (первичным) органам иммунной системы относят костный мозг и
тимус.
В центральных органах иммунной системы происходит созревание и дифференцировка клеток иммунной системы из стволовых клеток.
Слайд 3
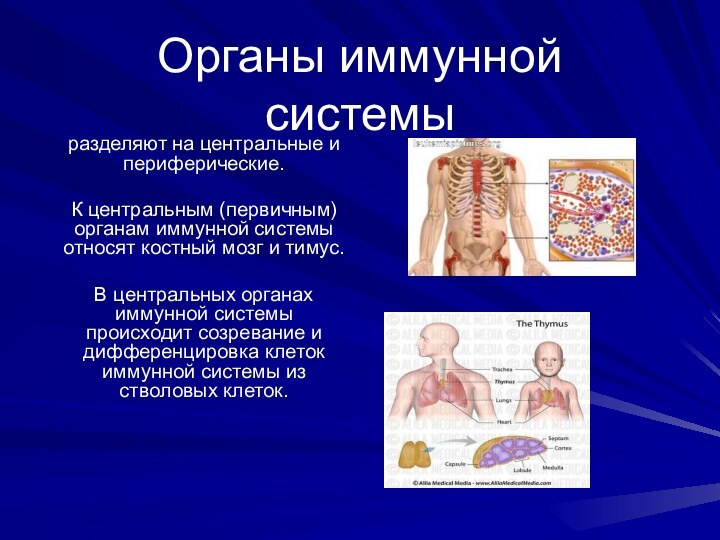
Органы иммунной системы
В периферических (вторичных) органах происходит дозревание
лимфоидных клеток до конечной стадии дифференцировки.
К ним относят
селезенку, лимфоузлы и лимфоидную ткань слизистых оболочек.
Слайд 4
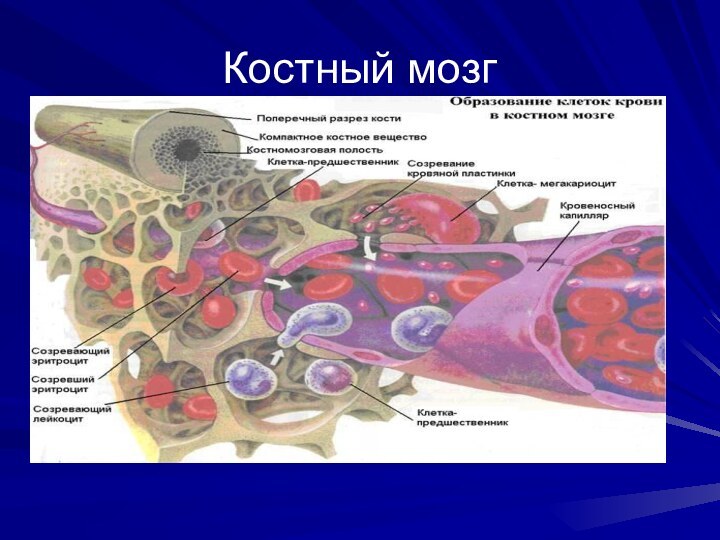
Центральные органы иммунной системы Костный мозг.
Здесь образуются все
форменные элементы крови.
Кроветворная ткань представлена цилиндрическими скоплениями вокруг
артериол.
Образует шнуры, которые отделены друг от друга венозными синусами. Последние впадают в центральный синусоид.
Клетки в шнурах располагаются островками.
Стволовые клетки локализованы в основном в периферической части костномозгового канала. По мере созревания они перемешаются к центру, где проникают в синусоиды и затем поступают в кровь.
Слайд 6
Костный мозг у детей
Миелоидные клетки в костном мозге
составляют 60—65%, лимфоидные — 10-15%, 60% клеток — это
незрелые клетки.
Остальные — созревшие или вновь поступившие в костный мозг
Ежедневно из костного мозга на периферию мигрирует около 200 млн. клеток, что составляет 50% от их общего количества.
В костном мозге человека идет интенсивное созревание всех типов клеток, кроме Т-клеток.
Последние проходят только начальные стадии дифференцировки (про-Т-клетки, мигрирующие затем в тимус).
Слайд 7
Костный мозг
Стволовые клетки, поступающие из костного мозга в
кровь, уже на 7-8-й неделе эмбрионального развития заселяют тимус,
где из этих клеток образуются Т-лимфоциты
(тимусзависимые) и B-лимфоциты (бурсазависимые)
Слайд 8
В-лимфоциты
Не зависят в своей дифференцировке от тимуса.
Развиваются из стволовых клеток в самом костном мозге, который
в настоящее время рассматривается в качестве аналога бурсы (сумки) Фабрициуса (клеточного скопления в стенке клоачного отдела кишки у птиц).
B-лимфоциты с током крови поступают из костного мозга в периферические органы иммунной системы.
Слайд 9
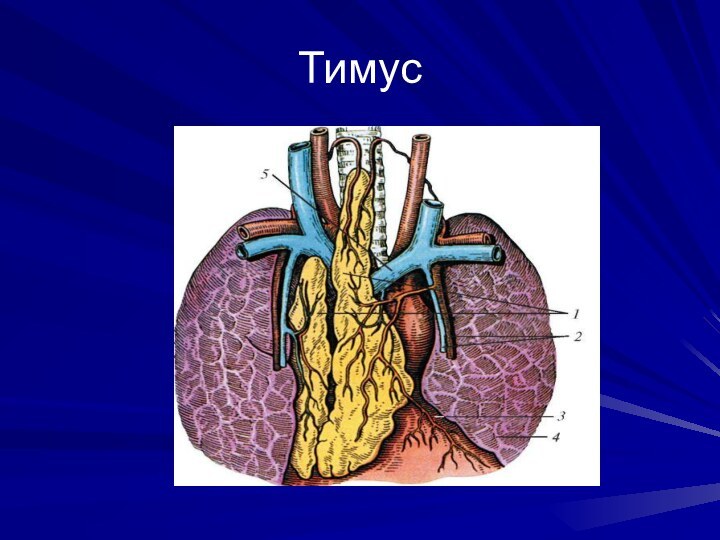
Тимус.
Тимус. Специализирован исключительно на развитии Т-лимфоцитов. Имеет эпителиальный
каркас, в котором развиваются Т-лимфоциты.
Тимус у человека состоит из
двух долек. Каждая из них ограничена капсулой, от которой внутрь идут соединительно-тканные перегородки. Перегородки разделяют на дольки периферическую часть органа — кору. Внутренняя часть органа называется мозговой.
Слайд 10
Возрастные особенности тимуса
К моменту рождения масса тимуса составляет
в среднем 13,3 г (от 7,7 до 34,0 г). В течение первых
3 лет жизни ребенка тимус растет наиболее интенсивно.
Тимус достигает максимальных размеров к периоду полового созревания.
После 16 лет масса тимуса постепенно уменьшается.
Лимфоидная ткань тимуса не исчезает полностью даже в старческом возрасте. Она сохраняется, но ее значительно меньше, чем в детском и подростковом возрасте.
Тельца тимуса размерами 35-40 мкм и более определяются уже у новорожденного - до 4-8 телец на срезе каждой дольки. В дальнейшем их количество и величина возрастают, к 8 годам размеры достигают 140-320 мкм.
Слайд 11
Тимус
До 10 лет корковое вещество преобладает над мозговым,
хотя начиная с 3-4 лет оно постепенно сужается и
теряет четкость внутренней границы.
К 10 годам размеры коркового и мозгового вещества примерно равны (соотношение 1:1).
В дальнейшем в тимусе зона коркового вещества становится тоньше, постепенно начинает преобладать мозговое вещество.
Отдельные жировые клетки обнаруживаются в тимусе у детей 2-3 лет.
В дальнейшем наблюдаются разрастание соединительнотканной стромы в органе и увеличение количества жировой ткани. К 30-50 годам жировая ткань замещает большую часть паренхимы органа. В результате лимфоидная ткань (паренхима) сохраняется лишь в виде отдельных отростков (долек), разделенных жировой тканью. Если у новорожденного соединительная ткань составляет только 7% массы тимуса, то в 20 лет она достигает 40% (в том числе и жировая), а у лиц старше 50 лет - до 90%.
Слайд 12
Три основные события, происходящие в процессе созревания Т-клеток
в тимусе
1. Появление у созревающих тимоцитов антигенраспознающих Т-клеточных рецепторов.
2. Дифференцировка Т-клеток на субпопуляции (CD4 и CD8).
3. Отбор (селекция) клонов Т-лимфоцитов, способных распознавать только чужеродные антигены
Слайд 14
Тимус
Протимоциты поступают в корковый слой и по мере
созревания перемещаются в мозговой слой. Срок развития тимоцитов в
зрелые Т-клетки — 20 дней.
В тимус незрелые Т-клетки поступают, не имея на мембране маркеров Т-клеток: CD3, CD4, CD8.
В тимусе у созревающих тимоцитов появляются антигенраспознающие Т-клеточные рецепторы.
Затем созревающие тимоциты размножаются и проходят два этапа селекции.
Слайд 15
Тимус
1.Позитивная селекция — отбор на способность узнавать с
помощью Т-клеточного рецептора собственные молекулы главного комплекса гистосовместимости.
Клетки,
не способные распознавать собственные молекулы главного комплекса гистосовместимости, погибают путем апоптоза (программируемая клеточная смерть).
Выжившие тимоциты теряют один из четырех Т-клеточных маркеров — или CD4, или CD8 молекулу.
В итоге из так называемых «двойных позитивных» (CD4 CD8) тимоциты становятся одинарными позитивными.
На их мембране экспрессируется или молекула CD4, или молекула CD8.
Тем самым закладываются различия между двумя основными популяциями Т-клеток — цитотоксических СD8-клеток и хелперных СD4-клеток.
Слайд 16
Тимус
3. Негативная селекция — отбор клеток на их
способность не узнавать собственные антигены организма.
На этом этапе
элиминируются потенциально аутореактивные клетки, то есть клетки, чей рецептор способен распознавать антигены собственного организма. Негативная селекция закладывает основы формирования толерантности, то есть неотвечаемости иммунной системы на собственные антигены. После двух этапов селекции выживает всего 2% тимоцитов.
Выжившие тимоциты мигрируют в мозговой слой и затем выходят в кровь, превращаясь в «наивные» Т-лимфоциты.
Слайд 18
Периферические лимфоидные органы
Разбросаны по всему телу. Основная функция
периферических лимфоидных органов — активация наивных Т- и В-лимфоцитов
с последующим образованием эффекторных лимфоцитов.
Различают инкапсулированные периферические органы иммунной системы (селезенка и лимфатические узлы) и неинкапсулированные лимфоидные органы и ткани.
Слайд 19
Лимфатические узлы
Составляют основную массу организованной лимфоидной ткани.
Лимфоузлы
имеют В-клеточную корковую область (кортикальную зону), Т-клеточную паракортикальную область
(зону) и центральную, медуллярную (мозговую) зону, образованную клеточными тяжами, содержащими Т- и В-лимфоциты, плазматические клетки и макрофаги. Корковая и паракортикальная области разделены соединительно-тканными трабекулами на радиальные секторы.
Слайд 20
Лимфатические узлы
Защищают организм от антигенов, проникающих через кожу
и слизистые оболочки.
Чужеродные антигены транспортируются в регионарные лимфоузлы
по лимфатическим сосудам, или с помощью специализированных антигенпрезентирующих клеток, или с током жидкости.
В лимфоузлах антигены предъявляются наивным Т-лимфоцитам профессиональными антигенпрезентирующими клетками.
Результатом взаимодействия Т-клеток и антигенпрезентирующих клеток является превращение наивных Т-лимфоцитов в зрелые эффекторные клетки, способные к выполнению защитных функций.
В-клетоки превращаются в плазматические антителопродуцирующие клетки.
Плазматические клетки представляют собой конечный этап созревания В-лимфоцитов.
Слайд 21
Лимфатические узлы
Различают следующие группы периферических лимфатических узлов, доступных
пальпации:
1) затылочные лимфатические узлы, расположенные на буграх затылочной кости
и собирающие лимфу с кожи волосистой части головы и задней части шеи;
2) сосцевидные лимфатические узлы, располагающиеся за ушами области сосцевидного отростка, а предушные - впереди уха на околоушной слюнной железе и собирающие лимфу из среднего уха, с кожи, окружающей ухо, ушных раковин и наружного слухового прохода, вместе они определяются, как околоушные;
Слайд 22
Лимфатические узлы
3) подчелюстные лимфатические узлы, расположенные под ветвями
нижней челюсти и собирающие лимфу с кожи лица и
слизистой оболочки десен;
4) подбородочные лимфатические узлы (обычно по одному с каждой стороны) и собирающие лимфу с кожи нижней губы, слизистой оболочки десен и области нижних резцов;
5) переднешейные и тонзиллярные лимфатические узлы, находящиеся кпереди от грудино-ключично-сосцевидной мышцы преимущественно в верхнем шейном треугольнике и собирающие лимфу с кожи лица, околоушной железы, слизистых оболочек носа, зева и рта;
Слайд 23
Лимфатические узлы
6) заднешейные лимфатические узлы, расположенные сзади от
грудино-ключично-сосцевидной мышцы перед трапециевидной мышцей преимущественно в нижнем шейном
треугольнике и собирающие лимфу с кожи, шеи и частично гортани; группы лимфатических узлов 1-6 нередко объединяют под общим названием – шейные;
7) надключичные лимфатические узлы, расположенные в области надключичных ямок и собирающие лимфу с кожи верхней части груди, плевры и верхушек легких;
8) подключичные лимфатические узлы, расположенные в подключичных областях и собирающие лимфу с кожи грудной клетки, плевры;
9) подмышечные лимфатические узлы, находящиеся в подмышечных ямках и собирающие лимфу с кожи верхней конечности, за исключением V, IV и III пальцев и внутренней поверхности кисти;
Слайд 24
Лимфатические узлы
10) торакальные лимфатические узлы, располагающиеся кнутри от
передней подмышечной линии под нижним краем большой грудной мышцы
и собирающие лимфу с кожи грудной клетки, париетальной плевры, отчасти легких и молочных желез;
11) локтевые, или кубитальные лимфатические узлы, расположенные в желобке двуглавой мышцы и собирающие лимфу от III, IV, V пальцев и внутренней поверхности кисти;
12) паховые лимфатические узлы, расположенные по ходу паховой связки и собирающие лимфу с кожи нижних конечностей, нижней части живота, ягодиц, промежности, с половых органов и заднего прохода;
13) подколенные лимфатические узлы, находящиеся в подколенной ямке и собирающие лимфу с кожи стопы.
Слайд 25
Лимфатические узлы
У новорождённых капсула лимфатических узлов очень тонкая
и нежная, трабекулы недостаточно развиты.
Лимфатические узлы мелкие, мягкой
консистенции, поэтому их пальпация вызывает затруднения.
К 1 году жизни лимфатические узлы уже можно пропальпировать у большинства детей. Вместе с постепенным увеличением объёма происходит их дальнейшая дифференцировка.
К 3 годам жизни тонкая соединительнотканная капсула хорошо выражена, содержит медленно разрастающиеся ретикулярные клетки.
К 7-8 годам в лимфатическом узле с выраженной ретикулярной стромой начинают постепенно формироваться трабекулы, прорастающие в определённых направлениях и образующие остов узла.
К 12-13 годам лимфатический узел имеет законченное строение: хорошо развитую соединительнотканную капсулу, трабекулы, фолликулы, синусы и менее обильную ретикулярную ткань, зрелый клапанный аппарат.
Слайд 26
Лимфатические узлы
В периоде полового созревания рост лимфатических узлов
останавливается, они частично подвергаются обратному развитию.
Реакцию лимфатических узлов
на различные (чаще всего инфекционные) агенты выявляют у детей начиная с 3-го месяца жизни.
В 1-2 года барьерная функция лимфатических узлов низкая, что объясняет частую в этом возрасте генерализацию инфекции.
В преддошкольном периоде лимфатические узлы уже могут служить механическим барьером и отвечать на присутствие возбудителей инфекционных болезней воспалительной реакцией. У детей этого возраста часто возникают лимфадениты, в том числе гнойные и казеозные (при туберкулёзе).
К 7-8 годам становится возможным подавление инфекции в пределах лимфатического узла.
Слайд 27
Селезенка
Крупный лимфоидный орган
Основная иммунологическая функция - накопление
антигенов, принесенных с кровью, и активации Т- и В-лимфоцитов,
реагирующих на принесенный кровью антиген.
В селезенке различают два основных типа тканей
Белая пульпа состоит из лимфоидной ткани, Т- и В-клеточные области.
Красная пульпа — ячеистая сеть, образованная венозными синусоидами, клеточными тяжами и заполненная эритроцитами, тромбоцитами, макрофагами, а также другими клетками иммунной системы.
Красная пульпа является местом депонирования эритроцитов и тромбоцитов.
Слайд 28
Неинкапсулированная лимфоидная ткань
Большая часть неинкапсулированной лимфоидной ткани расположена

в слизистых оболочках. Кроме того, неинкапсулированная лимфоидная ткань локализована
в коже и других тканях. К лимфоидной ткани слизистых оболочек относятся: —
Лимфоидные органы и образования, ассоциированные с желудочно-кишечным трактом (GALT — gut-associated lymphoid tissues). Включают лимфоидные органы окологлоточного кольца (миндалины, аденоиды), аппендикс, пейеровы бляшки, внутриэпителиальные лимфоциты слизистой оболочки кишечника.
Лимфоидная ткань, ассоциированная с бронхами и бронхиолами (BALT — bronchial-associated lymphoid tissue), а также внутриэпителиальные лимфоциты слизистой оболочки дыхательных путей.
Лимфоидная ткань других слизистых оболочек (MALT — mucosal associated lymphoid tissue), включающая в качестве основного компонента лимфоидную ткань слизистой урогенитального тракта.
Примером лимфоидной ткани слизистой могут служить пейеровы бляшки, встречающиеся обычно в нижней части подвздошной кишки.
Слайд 29
Неинкапсулированная лимфоидная ткань
Лимфоидная ткань слизистых оболочек обеспечивает
механизмы местного иммунитета на уровне слизистой оболочки — продукция
и транспорт секреторных антител класса IgA непосредственно на поверхность эпителия.
Основная функциональная нагрузка пейеровых бляшек — активация В-лимфоцитов и их дифференцировка в плазмоциты, продуцирующие антитела классов IgA и IgE.
Слайд 30
Неинкапсулированная лимфоидная ткань
Скопления клеток лимфоидного ряда в толще
стенок конечного отдела тонкой кишки обнаруживаются уже на 4-м
месяце внутриутробного развития.
Однако границы будущих узелков нечеткие, а клеточные элементы в них располагаются рыхло.
У 5-месячного плода узелки в слизистой оболочке становятся округлыми.
мУ новорожденных бляшки не выступают над поверхностью слизистой оболочки.
По мере увеличения возраста ребенка число узелков, содержащих центр размножения, быстро увеличивается.
В грудном возрасте лимфоидные бляшки уже выступают над поверхностью слизистой оболочки.
Слайд 31
Неспецифические механизмы иммунной системы
На ранних этапах онтогенеза играют
первостепенную роль в защите организма ребенка.
Содержание фибронектина (компонента
внеклеточного матрикса) у плода составляет 50% концентрации взрослых.
При снижении его биосинтеза у детей развиваются респираторные инфекции, респираторный дистресс-синдром, бактериемия и сепсис.
Слайд 32
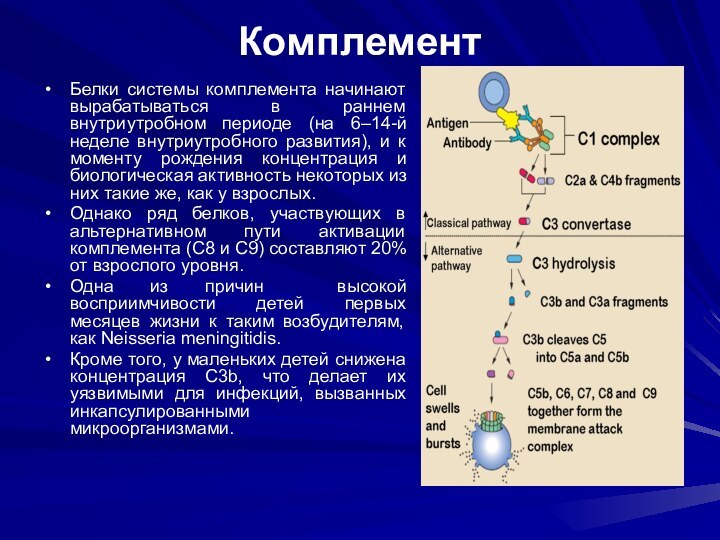
Комплемент
Белки системы комплемента начинают вырабатываться в раннем внутриутробном
периоде (на 6–14-й неделе внутриутробного развития), и к моменту
рождения концентрация и биологическая активность некоторых из них такие же, как у взрослых.
Однако ряд белков, участвующих в альтернативном пути активации комплемента (C8 и C9) составляют 20% от взрослого уровня.
Одна из причин высокой восприимчивости детей первых месяцев жизни к таким возбудителям, как Neisseria meningitidis.
Кроме того, у маленьких детей снижена концентрация C3b, что делает их уязвимыми для инфекций, вызванных инкапсулированными микроорганизмами.
Слайд 33
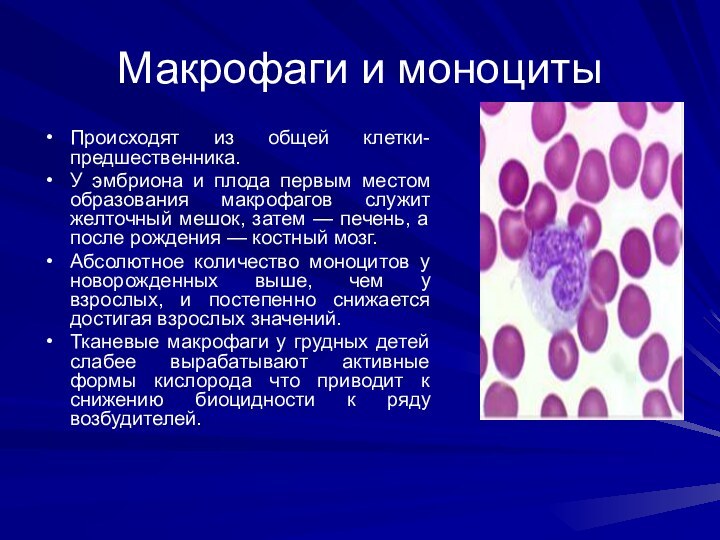
Макрофаги и моноциты
Происходят из общей клетки-предшественника.
У эмбриона
и плода первым местом образования макрофагов служит желточный мешок,
затем — печень, а после рождения — костный мозг.
Абсолютное количество моноцитов у новорожденных выше, чем у взрослых, и постепенно снижается достигая взрослых значений.
Тканевые макрофаги у грудных детей слабее вырабатывают активные формы кислорода что приводит к снижению биоцидности к ряду возбудителей.
Слайд 34
Макрофаги и моноциты
У новорожденных моноциты в меньшей
степени, чем
у взрослых, реагируют на интерферон γ,выделяемый NK- и T-лимфоцитами.
У новорожденных моноциты и макрофаги недостаточно секретируют ряд цитокинов и факторов роста (ФНОα, ИЛ-8, ИЛ-6, гранулоцитарный колониестимулирующеий фактор)
Резко различается хемотаксис макрофагов в очаги инфекции и воспаления.
Так, при повреждении кожи у новорожденного моноциты оказываются в месте повреждения значительно позже, чем у взрослого; эта разница стирается только к 6–10-летнему возрасту
Слайд 35
Неспецифические механизмы иммунной системы
Фагоцитарная функция гранулоцитов плода формируется
к 12-й неделе беременности и, как правило, носит незавершенный
характер.
Это обусловлено сниженным хемотаксисом, а также несовершенством внутриклеточных механизмов бактерицидности.
Слайд 36
Нейтрофилы
Зрелые нейтрофилы появляются в крови плода уже на14–16-й
неделе внутриутробного развития, и затем их количество нарастает.
Сразу
после рождения у ребенка наблюдается резкое повышение числа нейтрофилов в крови, однако способность костного мозга новорожденных поставлять нейтрофилы довольно ограниченна возможно, поэтому значительного нейтрофильного лейкоцитоза в ответ на инфекцию не возникает.
Слайд 37
Нейтрофилы
хемотаксис нейтрофилов новорожденных в очаг инфекции происходит медленно.
Причины
слабая адгезия на эндотелии
сниженная выработка цитокинов
моноцитами и физиологическая недостаточность хемотаксиса
Только к двухлетнему возрасту скорость миграции нейтрофилов достигает таковой у взрослых
Слайд 38
NK-лимфоциты
NK-лимфоциты появляются в крови плода начиная с шестой
недели внутриутробного развития
Их цитолитическая активность у новорожденных примерно
вдвое ниже, чем у NK-лимфоцитов
взрослых, и достигает нормального уровня примерно через 9–12 месяцев.
Способность к антителозависимой
клеточной цитотоксичности в отношении клеток, инфицированных герпесвирусами, также снижена, что повышает воспри-
имчивость ребенка к вирусу простого герпеса и цитомегаловирусу
Слайд 39
Дендритные клетки
снижена способность дендритных клеток представлять антигены
Дендритные клетки
пуповинной крови экспрессируют меньше молекул HLA и ICAM-1 и
хуже поддерживают пролиферацию T-лимфоцитов в ответ на воздействие антигена, чем дендритные клетки взрослых
способности стимулировать CD4+Tх 1 типа.
Слайд 40
Т-система иммунитета
Т-лимфоциты
Т-клетки с фенотипом CD4+
и CD8+ появляются в фетальной печени и селезенке плода
на 14-й неделе гестации.
Все неонатальные Т-лимфоциты экспрессируют молекулу CD38+ (маркер тимоцитов).
90% неонатальных Т-клеток экспрессируют CD45RA (маркер наивных Т-клеток),
Слайд 41
Т-система иммунитета
Особенности Т-лимфоцитов новорожденных связаны с выходом в
кровоток недозрелыхпредшественников.
Регуляторная функция Т лимфоцитов несовершенна
Экспрессия рецепторов для
цитокинов понижена (в частности (ИЛ-2R) рецептора и молекулы CD40L
Цитотоксическая активность Т-лимфоцитов составляет 30–60% уровня активности Т-клеток взрослого человека.
Слайд 42
Т-система иммунитета
Выработка ИЛ-1, ИЛ-2, ИЛ-3, ИЛ-4 составляет примерно
10% уровня взрослых
Выработка ИЛ-5, ИЛ-6, ИЛ-8 составляет 10–50%
уровня взрослых
Содержание интерферонов α и β, ФНО-α соответствует уровню взрослых, а γ-интерферона составляет 10%.
Слайд 43
Т-система иммунитета
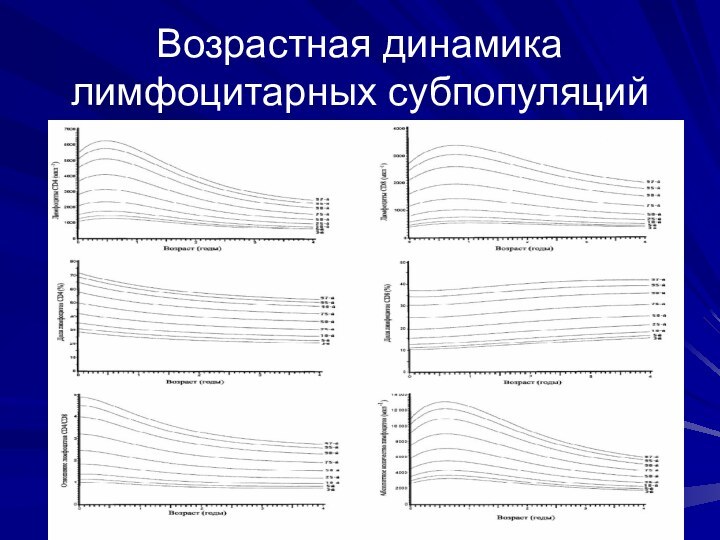
Относительное количество Т-лимфоцитов у новорожденных понижено по
сравнению со взрослыми, но в связи с возрастным лимфоцитозом
абсолютное количество Т-лимфоцитов в крови новорожденных даже выше, чем у взрослых.
В связи с дефектностью клеточных механизмов защиты на протяжении всего периода детства сохраняется высокая степень риска заболевания туберкулезом
Слабость клеточных механизмов защиты делает детей особенно чувствительными к вирусным и грибковым инфекциям, защита от которых требует участия функционально полноценных Т-лимфоцитов
Слайд 44
Возрастная динамика лимфоцитарных субпопуляций
Слайд 45
В-система иммунитета
Пре-В-лимфоциты выявляются у плода в фетальной печени
на 8-й неделе гестации. Фетальные В-клетки экспрессируют только молекулы
IgM, без экспрессии IgD.
В-лимфоциты новорожденных дифференцируются в плазматические клетки, секретирующие IgM, но они не могут переключаться в клетки, продуцирующие IgG и IgA.
Это объясняется недостаточно эффективной помощью со стороны СD4+ Т-лимфоцитов-хелперов.
Слайд 46
В-система иммунитета
Содержащиеся в крови плода антитела IgG класса
имеют материнское происхождение и защищают плод от того спектра
патогенов, к которым у матери в процессе жизни сформировался приобретенный иммунитет.
Транспорт их через плаценту (трансплацентарная передача антител) начинается на 8-й неделе.
Эти же антитела формируют пассивный иммунитет, защищающий ребенка от инфекции в первые 3–6 месяцев постнатального периода жизни.
Слайд 47
В-система иммунитета
У преждевременно рожденных детей концентрация иммуноглобулинов в
крови заметно ниже, чем у родившихся в срок.
Содержание В-лимфоцитов
у новорожденных повышенное. Они экспрессируют на мембране клеток молекулы IgM и IgD.
В пуповинной крови новорожденных определяются только IgM и IgG
После рождения материнские иммуноглобулины постепенно подвергаются катаболизму и выводятся, их концентрация в крови прогрессивно снижается
Слайд 49
В-система иммунитета
К 3–4-му месяцу жизни происходит становление биосинтеза
собственных IgG, и их концентрация к этому времени составляет
примерно 30–40% уровня взрослых. В последующем их содержание постепенно возрастает
К концу первого года жизни достигает 50–60% уровня взрослых, уровень IgM сыворотки крови ребенка также практически достигает уровня взрослых.
Повышенное содержание IgM в крови новорожденных является неблагоприятным признаком и часто свидетельствует о внутриутробном инфицировании плода (краснуха, сифилис, герпес, ВИЧ и др.).
Слайд 50
В-система иммунитета
Продукция собственных IgА заметно отстает и к
концу первого года составляет только 25–30% уровня взрослых.
Секреторные
IgA и специфические антитела данного изотипа в секретах появляются на 3–4-м месяце жизни. Содержание IgG и IgA у детей 5–6 лет достигает уровня взрослых.
Уровень секреторных IgA у детей в 3–4 раза ниже, чем у взрослых, и достигает их концентрации только к 10–15 годам. Иммунный ответ детей на полисахаридные вакцины – гемофилюс инфлуенца, псевдомонас и пневмококк — ослаблен вплоть до 2-летнего возраста.
В крови новорожденных IgE не выявляются, 4–6 годам их концентрация увеличивается и к 8–11 годам достигает уровня взрослых.
Слайд 51
Первый критический период
это период новорожденности (до 29 дней
жизни),
организм ребенка защищен почти исключительно материнскими антителами, полученными
через плаценту и с грудным молоком.
Чувствительность новорожденного ребенка к бактериальным и вирусным инфекциям в этот период очень высока.
Группу повышенного риска развития инфекций среди новорожденных составляют недоношенные, а среди них — маловесные дети, страдающие наиболее выраженными и стойкими иммунологическими дефектами.
Слайд 52
Первый критический период
Повышенное количество гранулоцитов в крови новорожденных
в какой-то степени компенсирует недостаточную активность их защитных функций.
Абсолютное количество моноцитов крови у новорожденных выше, чем у детей более старшего возраста, но они также отличаются низкой защитной активностью.
Содержание антибактериального фермента лизоцима в сыворотке крови новорожденного превосходит уровень материнской крови уже при рождении, он нарастает в течение первых дней жизни, а к 7-8-ому дню жизни несколько снижается и достигает уровня взрослых людей.
Слайд 53
Первый критический период
Низкое содержание основных компонентов системы комплемента
в крови новорожденных является причиной недостаточной вспомогательной активности сыворотки
крови при фагоцитозе. Только ко второму году жизни окончательно созревает продукция компонентов системы комплемента.
В крови новорожденных содержание естественных киллеров значительно ниже, чем у взрослых. Естественные киллеры детской крови отличаются сниженной цитотоксической и секреторной активностью.
Как видно из выше сказанного, у новорожденных детей резко ослаблены все основные механизмы неспецифической защиты организма от патогенных бактерий и вирусов, чем объясняется высокая чувствительность новорожденных и детей первого года жизни к бактериальным и вирусным инфекциям.
характерно затяжное течение инфекций (например, пневмонии) и низкая эффективность антибиотикотерапии.
Слайд 54
Второй критический период (4-6 мес. жизни)
утратой полученных от
матери антител. Способность к продукции собственных антител в этот
период ограничивается слабым синтезом только иммуноглобулинов M,
Недостаточность местной защиты слизистых связана с более поздним накоплением секреторного иммуноглобулина A. В связи с этим чувствительность ребенка ко многим воздушно-капельным и кишечным инфекциям в этот период очень высока.
Слайд 55
Третий критический период (2-й год жизни),
когда значительно расширяются
контакты ребенка с внешним миром и с возбудителями инфекций.
Иммунный ответ ребенка на инфекционные антигены остается неполноценным.
Местная защита слизистых все еще остается несовершенной из-за низкого уровня секреторного IgA.
Чувствительность ребенка к респираторным и кишечным инфекциям все еще высока.
Слайд 56
Четвертый критический период (6-7й годы жизни),
Когда в крови
у ребенка уменьшается абсолютное и относительное количество лимфоцитов.
В
этот период уровни иммуноглобулинов М и G в крови ребенка приближаются к уровням взрослых, но уровень иммуноглобулина A все еще остается более низким, с чем связана слабая местная защита слизистых.
Содержание иммуноглобулина E, напротив, достигает максимального уровня в связи с высоким уровнем глистных инвазий, чем объясняется повышенная чувствительность к аллергическим реакциям у детей данной возрастной группы. Чувствительность детей этого возраста к инфекциям все еще высока.
Слайд 57
Пятый критический период
подростковый возраст (у девочек с 12-13
лет, у мальчиков с 14-15 лет), когда скачок роста
сочетается с относительным уменьшением массы лимфоидных органов, а начавшаяся секреция половых гормонов служит причиной угнетения клеточных механизмов иммунитета.
В этом возрасте резко возрастают внешние, часто неблагоприятные, воздействия на иммунную систему.
Дети этого возраста характеризуются высокой чувствительностью к вирусным инфекциям.
Слайд 58
В ФУНКЦИОНАРОВАНИИ ИММУННОЙ СИСТЕМЫ ВЫДЕЛЯЮТ 3 ВАРИАНТА
-НОРМАЛЬНОЕ ИЛИ
ФИЗИОЛОГИЧЕСКОЕ
-ПАТОЛОГИЧЕСКОЕ ФУНКЦИОНИРОВАНИЕ В ВИДЕ УСИЛЕНИЯ ФУНКЦИИ -АЛЛЕРГИЯ, АУТОИММУНИТЕТ
-СТОЙКОЕ УГНЕТЕНИЕ ФУНКЦИИ ПЕРВИЧНОГО ИЛИ ПРИОБРЕТЕННОГО ХАРАКТЕРА
Слайд 59
Диагностика аллергических заболеваний-аллергоанамнез
Сбор аллергоанамнеза можно условно разделить на
несколько этапов: •
установление основных сведений о наследственной предрасположенности
пациента к аллергии (аллергические заболевания у отца, матери, ближайших родственников); •
выявление аллергических заболеваний, возникших у пациента ранее;
установление (по возможности) вида аллергена, причинно-значимого для настоящего аллергического заболевания.
Слайд 60
Диагностика аллергических заболеваний-аллергоанамнез
В перечень основных вопросов следует включить:
реакции на различные лекарства (какие, когда),
реакции на введение
вакцин, сывороток,
реакции на пищевые продукты,
сезонность заболевания, ухудшение состояния на улице в солнечную, ветреную либо сырую влажную погоду, появление симптоматики или ухудшение состояния в пыльных помещениях, при уборке, в поле, днем (ночью), при контакте с животными и т.д.,
характер жилищно-бытовых условий пациента и, соответственно, возможное влияние аллергенов окружающей среды: сырость и наличие плесени в помещениях, ковры, мягкая мебель, спальные принадлежности, книги, животные, аквариумные рыбы, птицы, цветы; •
Слайд 61
Анамнез ребенка, характерный для атопической предрасположенности
1) концентрация в семье
заболеваний типа поллиноза, бронхиальной астмы, экземы, дерматита, реакций непереносимости
пищевых продуктов или медикаментов;
2) зудящие, повторяющиеся кожные сыпи, формирование устойчивых проявлений экземы или нейродермита;
3) связь кожных реакций и расстройств стула с введением в питание молочных смесей или блюд прикорма;
4) выраженное затруднение дыхания, «пыхтение» или одышка при некоторых простудных заболеваниях, физической нагрузке;
5) периодические приступы чиханья с зудом слизистой оболочки носа и обильным слизистым отделяемым;
6) периодические приступы слабости, головокружения, обильного потоотделения с ощущением зуда кистей, стоп, губ или языка.
Слайд 62
Диагностика аллергических заболеваний.Кожные пробы.
Основаны на воспроизведении аллергической реакции
у больного путём экспозиции минимального количества аллергена.
Наиболее часто
эти реакции проводят на коже пациента.
Применяют 3 основных вариантов кожного теста скарификационный, близкий к нему прик-тест (тест уколом) и внутрикожные пробы.
Прик-тест (тест уколом) проводят путём прокалывания кожи на определённую глубину специальной иглой через каплю раствора аллергена. В связи с простотой выполнения и малым количеством ограничений этот тест используется наиболее часто.
Внутрикожная проба. Производят инъекцию малого количества аллергена в поверхностный слой кожи. В связи с повышенным риском развития системных реакций внутрикожную пробу проводят после получения отрицательного результата прик-теста
Слайд 64
Провокационные тесты
Различают
Назальные тесты
Назальные тесты применяют для
диагностики аллергического ринита.
Конъюнктивальные тесты
Конъюнктивальные тесты используют для диагностики
аллергического конъюнктивита.
Ингаляционные тесты
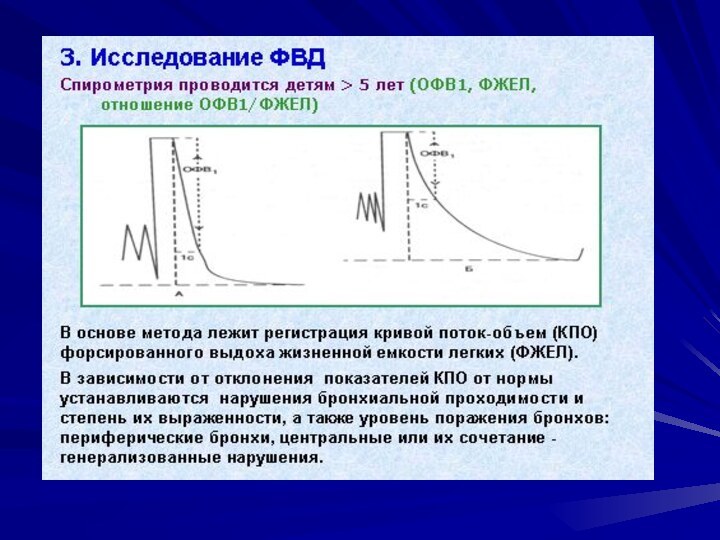
Ингаляционные тесты применяют для диагностики бронхиальной астмы и проводят только в условиях стационара. Сначала оценивают показатели функции внешнего дыхания — ОФВ1 (первоначально не менее 70% от должных величин).При снижении показателя более чем на 20% тест считается положительным..
Сублингвальные тесты
Сублингвальный тест применяют для диагностики лекарственной и пищевой аллергии. Тест считается положительным при возникновении местной воспалительной реакции на слизистой оболочке полости рта или системной реакции.
Слайд 66
Диагностика аллергических заболеваний ЦИТОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ НАЗАЛЬНОГО СЕКРЕТА И
МОКРОТЫ
Эозинофилия при цитологическом исследовании характерна для аллергических заболеваний
Слайд 75
Учитывается возрастная динамика концентрации Ig E
Слайд 78
Технология MAST-хемилюминесценция-батарейный скрининг
Слайд 84
УГНЕТЕНИЕ ФУНКЦИИ иммунной системы ПЕРВИЧНОГО ИЛИ ПРИОБРЕТЕННОГО ХАРАКТЕРА
первичные
(врожденные) и вторичные (приобретенные) иммунодефицитные состояния.
Из анамнеза предположение об
ИД возникает
: ребенок страдает рецидивирующими и (или) тяжело протекающими инфекционными (чаще всего бронхолегочной системы, желудочно-кишечного тракта, мочевыводящих путей, кожных покровов) нередко с развитием гнойных осложнений (отитов, синуситов и др.) или сепсиса
отмечаются необычные реакции на банальные инфекционные агенты (например, гигантоклеточная пневмония при краснухе, пневмония при ветряной оспе)
инфекционное заболевание вызвано необычными микроорганизмами (например, пневмоцистой Карини);
наличие у ребенка необычных реакций (системных) на вакцинацию живыми вирусными вакцинами или БЦЖ;
необъяснимый гематологический дефицит у ребенка (анемия или лейкопения, или тромбоцитопения);
стойкое расстройство пищеварения с развитием синдрома мальабсорбции.
Слайд 85
Вторичные иммунодефициты
Сопровождаются инволюцией лимфоидной ткани,
К вторичным иммунодефицитам
относятся: патологические процессы, сопровождающиеся потерей белка (нефротический синдром, ожоги
кожи, экссудативные энтеропатии);
дистрофии, авитаминозы;
многие вирусные заболевания (корь, грипп и др.),
бактериальные заболевания (холера),
грибковые инфекции (кандидозы)
гельминтозы;
тяжелые хирургические травмы и послеоперационные осложнения;
некоторые лечебные воздействия (рентгеновское облучение, терапия кортикостероидами и цитостатиками);
опухоли лимфоретикулярной природы (лимфогранулематоз, хронический лимфолейкоз и т.д.).. В настоящее время для коррекции в
Слайд 86
Вторичные иммунодефициты
Генерализованное поражение всех компонентов иммунной системы (Т-
и В- клеток) и неспецифических гуморальных факторов (комплементарной и
фагоцитарной систем) характерно для СПИДа
Слайд 87
Первичные иммунодефициты
В-клеточной системы
Проявляются
Повторными и тяжелыми гнойными заболеваниями,
вызываемыми стрептококками, пневмококками, редко грибковыми и вирусными заболеваниями;
Отитами, синуситами,
повторными пневмониями, гнойными конъюктивитами в анамнезе, требующими нескольких курсов антибактериального лечения;
Диарейными болезнями или расстройствами, связанными с лямблиозом;
Умеренным отставанием в росте.
Слайд 88
Т-клеточный ПИД
характеризуется:
Повторными тяжелыми инфекциями, вызываемыми вирусами,
грибковыми осложнениями, инвазиями простейшими, упорными гельминтозами;
тяжелыми осложнениями на иммунизацию
живыми вирусными вакцинами или вакциной BCG;
частыми диарейными расстройствами;
истощением, отставанием в росте и развитии;
концентрацией опухолевых заболеваний в семье.
Слайд 89
характеризуются:
1) повторными кожными инфекциями и грибковыми поражениями кожи с
наиболее вероятными возбудителями, такими как стафилококк, псевдомонас, кишечная палочка;
2) абсцессами
подкожной клетчатки, легких;
3) гнойными артритами и остеомиелитами.
характеризуются:
1) повторными кожными инфекциями и грибковыми поражениями кожи с наиболее вероятными возбудителями, такими как стафилококк, псевдомонас, кишечная палочка;
2) абсцессами подкожной клетчатки, легких;
3) гнойными артритами и остеомиелитами.
Первичные фагоцитарные расстройства
Слайд 109
Определение киллинга и расщепления патогенов
НСТ-тест восстановления нитросинего
тетразолия
Индуцированная хемилюминесценция
Слайд 110
Бронхиальная астма заболевание характеризующееся
обратимой обструкцией дыхательных путей, вследствие
бронхоспазма, отека слизистой бронхов, гиперсекреции слизи;
- эпизодами кашля, свистящих
хрипов, одышки, чувства стеснения в груди, связанными с воздействием специфических и неспецифических триггеров;
- гиперреактивностью дыхательных путей
Слайд 111
Этиология
1. Бытовые - домашняя пыль, клещи
дом.
пыли: Dermatophagoideus
pteronissinum и D. farinae,
перо подушки, библиотечная
пыль;
2. Эпидермальные (шерсть, пух,
перхоть, экскременты, слюна живот-
ных, тараканы);
3. Грибковые: плесневые грибы (Al-
ternaria, Aspergillus, Cladosporium,
Penicillium) и дрожжевые грибы родаCandida. -
Слайд 112
Этиология
Пыльцевые : пыльца
деревьев, злаковых и сорных трав.
Три пика
цветения:
1-й пик – конец апреля, май
( деревья);
2-й пик – июнь, июль (цветут злаковые травы, липа);
3-й пик – август, сентябрь (цветут
сорные травы)
Вызывают сезонную БА
Слайд 113
Этиология
Пищевые аллергены:
Коровье молоко, яйца, рыба,
крупы, фрукты, овощи
и др.
Вызывают БА у детей ранне-
го возраста.
4. Лекарственные аллергены:
антибиотики,
сульфанилами-
ды, НПВС.
Слайд 114
Неспецефические триггеры
1.Острая респираторная вирусная инфекция
2. Синуситы
3. Физическая нагрузка
4.
Психоэмоциональная нагрузка
5. Изменение метеоситуации
6. Загрязнения атмосферного воздуха
7. Табачный дым
8.
Краска, резко пахнущие вещества
9. Пищевые добавки
10. Паразитарные инфекции
Слайд 117
Клиника
После контакта с аллергеном (через 20-30 мин) появляются
предвестники: ринорея, чиханье, кашель, зуд в глотке и др.
Приступ БА: затрудненное дыхание или удушье, одышка экспираторного характера, чувство сдавления в груди, тахипноэ, дистанционные свистящие хрипы, вынужденное положение с фиксацией верхнего плечевого пояса, кашель приступообразный с вязкой стекловидной мокротой, участие вспомогательной мускулатуры в акте дыхания. Цианоз носогубного треугольника. В легких жесткое дыхание, сухие свистящие, жужжащие и крупнопузырчатые влажные хрипы. Перкуторно - коробочный звук.
Приступ длится от 30-40 мин до нескольких час. Купируется спонтанно или после приема бронхолитиков
Слайд 118
Клиника в зависимости от вида сенсибилизации
БЫТОВАЯ СЕНСИБИЛИЗАЦИЯ
Круглогодичные обострения
Ухудшение
в ночное время в домашней обстановке
Улучшение при смене
места жительства
Улучшение при создании гипоаллергенного быта в доме
ЭПИДЕРМАЛЬНАЯ СЕНСИБИЛИЗАЦИЯ
Ухудшение состояния после посещения цирка, зоопарка, игры с домашними животными
ГРИБКОВАЯ СЕНСИБИЛИЗАЦИЯ
Ухудшение во влажное время года, в сырых помещениях
Плохая переносимость продуктов, содержащих грибы
Реакция на антибиотики пенициллины и цефалоспорины
Слайд 119
Клиника у детей раннего возраста
В силу анатомо-физиологических особенностей
детского возраста (узость просвета бронхов, обильное кровоснабже-ние) приступ БА
сопровождается выраженным отеком и ги-персекрецией с преобладанием экссудативного компонента над бронхоспазмом.
Одышка смешанного характера с затрудненным выдохом.
В легких обилие влажных хрипов (влажная астма)
Начальные проявления БА часто протекают на фоне ОРВИ в виде бронхообструктивного синдрома
Дети грудного возраста, имеющие 3 и более эпизода свистящих хрипов, связанных с воздействием триггеров, расцениваются как больные БА.
Слайд 123
Диагностика
Сбор аллергологического анамнеза (отягощенный семейный анамнез
по АЗ, наличие у ребенка АД, АР)
Клиника - наличие следующих симптомов:
кашель, усиливающийся преимущественно в ночное время;
рецидивирующие свистящие хрипы;
повторные эпизоды свистящего дыхания;
рецидивирующее чувство стеснения в грудной клетке;
Появление или усиление симптомов:
в ночное время;
при воздействии специфических (аллергенов) или неспецифических триггеров.
Слайд 125
Пикфлоуриметрия
Проводится для ежедневного мониторинга течения БА.
Измеряется ПСВ
утром (наиболее низкие значения) и перед сном (более высокие
значения).
В норме дневной разброс показателей составляет не более 20%.
Слайд 126
Диагностика
4. Оценка аллергологического статуса
Кожное тестирование с аллергенами: скарификационные
пробы (в периоде ремиссии);
Определение общего и специфических IgE
По показаниям
– провокационные тесты (назальный, ингаляционный).
5. Рентгенография органов грудной клетки
эмфизематозной вздутие легких
6. Общий анализ крови:
При приступе БА – лейкопения,
эозинопения, которая сменяется
эозинофилией
7. Микроскопия мокроты:
эозинофилы, эпителиальные клетки, кристаллы Шарко-Лейдена и спирали Куршмана
Слайд 127
Лечение
предупреждение контакта с аллергеном
фармакотерапия
специфическая иммунотерапия
обучение пациента (астма школа)
Слайд 128
Лечение
БАЗИСНАЯ ИЛИ КОНТРОЛИРУЮЩАЯ –противовоспалительная терапия, применяемая для полного
контроля симптомов БА в периоде ремиссии постоянно (ПОДДЕРЖИВАЮЩАЯ ТЕРАПИЯ)
СИМПТОМАТИЧЕСКАЯ
ИЛИ НЕОТЛОЖНАЯ ТЕРАПИЯ – применяемая для купирования приступа БА
Слайд 129
Лечение
Топические кортикостероиды:
– беклометазон (альдецин, бекотид, беклозон легкое дыхание,
беклозон эко, беклофорте) 2-4 раза в сутки;
- будесонид (бенакорт,
пульмикорт турбухайлер);
флутиказон (фликсотид)
мометазона фуроат (астманекс 200 и 400 мг 1 раз/сут– с 12 лет).
Обладают мощной противовоспалительной активностью. Назначаются до полного контроля симптомов.
Антилейкотриеновые препараты – монтелукаст (4 мг на ночь с 2-5 лет, 5 мг – с 6 лет), аколат (с 12 лет по 20 мг/2 раза). Назначают самостоятельно и как дополнительную терапию вместе с ИКС.
Кромоны: интал, кромогексал, тайлед. Слабая противовоспалительная активностью. Показаны только при легкой БА у детей. Назначаются 3-4 раза в день.
Слайд 130
Лечение
β2-агонисты пролонгированного действия – салметерол (серевент), формотерол (форадил).
Приме-няются при недостаточном контроле БА на фоне ИКС. Вызывают
длительную бронходилятацию на 12 ч.
Пролонгированные теофиллины – теопэк, теостат, теодур. Однократный прием перед сном в дозе 15 мг/кг предотвращает ночные симптомы. Применяются для усиления терапии в месте с ИКС или кромонами.
Комбинированные препараты – ИКС + пролонгиро-ванный β2-агонист – серетид, тевакомб (флютиказон 100-250-500 мкг+сальметерол-50 мкг) 2 раза в день и симбикорт (бутесонид 80-160 мкг+формотерол – 4,5 мкг), зенхейл – (мометазона фуроат 50-100-200 мкг + формотерол 5 мкг) .
Слайд 133
Лечение
Для снятия остро возникших нарушений используют:
β2-агонисты короткого действия
сальбутамол, (вентолин, саламол эко легкое дыхание и др.), фенотерол
(беротек)
Антихолинергические препараты (атровент)
Комбинированные препараты (β2-агонист короткого действия и антихолинергический препарат) – беродуал
Ингаляционные КС – пульмикорт через небулайзер
Системные кортикостероиды – преднизолон
Теофиллины короткого действия (эуфиллин)
Слайд 134
Лечение
Легкий и среднетяжелый приступ БА (ОФВ1, ПСВ >
60%)
Ингаляции β2-агонистов короткого действия (сальбутамол, фенотерол - беротек) через
ДАИ или небулайзер.
Оценить эффект через 20 мин. Эффект хороший: наблюдать в течение часа; β2-агонисты каждые 4-6 часов в течение 24-48 ч.
Эффект плохой: повторить ингаляции β2-агонистов каждые 20 мин в течение часа; ИКС через небулайзер – будесонид по 0,25-0,5 мг 2 р/сут; системные кортикостероиды – преднизолон 1-1,5 мг/кг.
Слайд 135
Лечение
Тяжелый приступ БА
Ингаляционные β2-агонисты короткого действия (сальбутамол, беротек)
в сочетании с холинолитиками (атровент) или беродуал каждые 20
мин в течении часа
Отсутствие улучшения: ингаляции КС - будесонид через небулайзер 2 раза/сут; парантерально или внутрь преднизолон 1-2 мг/кг 3-5 дней; оксигенотерапия
Эффект хороший: продолжить лечение β2-агонистами каждые 6-8 часов в течение 48-72 час и ингаляции будесонида.
Эффект плохой: продолжить ингаляционные β2-агонисты короткого действия + холинолитики (атровент) или беродуал каждый час; системные кортикостероиды – парентерально или внутрь преднизолон 1-2 мг/кг;
- метилксантины (эуфиллин) внутривенно 4-5 мг/кг в течение 20-30 минут, затем в дозе 0,6-1 мг/кг/ч каждые 4-5 час, не более 10-15 мкг/мл в сутки.
Эффект плохой: перевод в отделение ИТ
Слайд 136
Профилактика
ПЕРВИЧНАЯ ПРОФИЛАКТИКА
Направлена на предотвращение возникновения заболевания у лиц
из групп высокого риска
- Антенатальная профилактика
Поощрение грудного вскармливания, его
преимущества включают защитный эффект отно-сительно возникновения свистящих хрипов
Отказ родителей от курения
Неспецифическая профилактика ОРВИ
Уменьшение аллергенной нагрузки в жилище
Слайд 137
Профилактика, вторичная
Направлена на уменьшение воздействия триггерных факторов для
улучшения контроля БА и уменьшения объема базисной терапии:
Элиминационный режим
(гипоаллергенный быт, гипоаллергенная диета)
Профилактика ОРВИ и риносинусита (неспецифическая и специфическая)
Слайд 138
Аллергический ринит (АР)
заболевание, в основе которого лежит IgE-опосредованное
воспаление слизистой оболочки носа, развивающееся под действием аллергенов, которое
характеризуется:
ринореей (передней и задней),
чиханием,
заложенностью носа,
и/или зудом в носу.
Слайд 139
Аллергический ринит (АР)
Являются широко распространенным заболеваний (в детской
популяции болеют до 40%)
Количество больных АР продолжает неуклонно расти
АР
является 2-й стадией атопического марша, промежуточной между атопическим дерматитом и бронхиальной астмой
Слайд 140
Этиология
Причиной аллергических ринитов являются аллергены:
Пыльцевые (пыльца деревьев,
злаковых и сорных трав)
Бытовые (аллергены клещей домашней пыли)
Эпидермальные
(аллергены животных: кошки,собаки, грызунов, лошади)
Грибковые (споры непатогенных плесневых и дрожжевых грибов)
Аллергены насекомых
Слайд 141
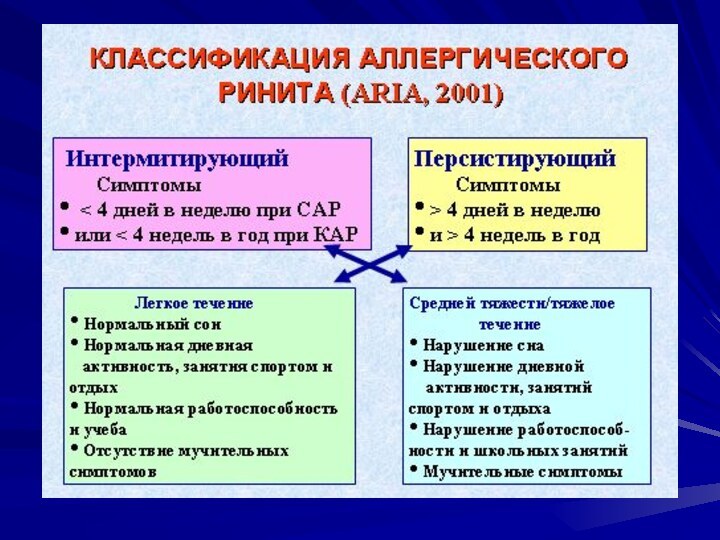
Классификация
Сезонный АР
пыльца растений
споры плесневых грибов
Заболевание характеризуется строгой сезонностью
Круглогодичный АР
Аллергены клещей домашней пыли
Аллергены домашних животных и насекомых
Симптомы
АР появляются на протяжении всего года
периодически или постоянно
Слайд 144
Клиника
Отечная форма – преобладает заложенность носа над ринореей
(блокадники)
Гиперсекреторная форма – ринорея ведущий симптом (эффективны антигистамнные препараты)
- чихальщики
Слайд 145
Клиника
Раздражение, отечность гиперемия кожи над верхней губой и
крыльев носа
Носовые кровотечения вследствие форсированного сморкания
Боль в
горле, покашливание (проявление сопутствующего аллергического фарингита, ларингита)
Боль и треск в ушах, особенно при глотании, нарушение слуха (аллергический тубоотит)
Слайд 146
Диагностика
1. Анамнез заболевания и наследственность
2. Типичная клиническая картина
ринита
3. Осмотр: характерные признаки АР: «аллергический салют», «аллергические
круги», постоянно открытый рот, «шмыганье носом», покраснение кожи вокруг носа.
4. Специфическая аллергологическая диагностика (кожные пробы с аллергенами, определение общего и спец. IgЕ, назальный провокационный тест со специфическими аллергенами)
5. Исследование периферической крови (эозинофилия)
6. Цитологическое исследование секрета (эозинофилия)
7. Риноскопия
8. По показаниям – рентгенография, КТ, эндоскопия
Слайд 147
Лечение
предупреждение контакта с аллергеном
фармакотерапия
специфическая иммунотерапия
обучение пациента
Слайд 148
Лечение
антигистаминные средства (пероральные, топические – назальный спрей: аллергодил)
интраназальные
кортикостероиды
интраназальные кромоны
интраназальные деконгестанты
антилейкотриеновые препараты
Слайд 149
Антигистаминные препараты 1 поколения
Не являются селективными: наличие седативного
и антихолинергического эффектов
Имеют побочные действия на ССС и ЖКТ
Не
оказывают противоаллергического и противовоспалительного действия
Имеют кратковременный эффект
К ним развивается тахифилаксия
Не являются препаратами выбора при АР
Слайд 150
Антигистаминные препараты 2,3 поколения
Зиртек – с 6 мес
Эриус
–с 1 года
Кларитин – с 2-х лет
Ксизал – с
2-х лет
Телфаст – с 6 лет
Можно применять длительно в течение всего сезона цветения.
Не развивается привыкание.
Слайд 151
Антигистаминные препараты 2,3 поколения
Оказывают мощное противовоспалительное действие –
подавляют раннюю и позднюю стадии аллергической реакции
Быстро снимают симптомы
АР: заложенность носа, ринорею, зуд, чиханье
Снижают назальную гиперреактивность
Действуют непосредственно в очаге поражения
Слайд 152
Назальные КС
Безопасны при длительном применении
Назонекс и авамис –
снимают глазные симптомы.
Детям до 12 л – по 1
ингаляции в каждую ноздрю, > 12 л – по 2 ингаляции.
Применяют длительно – весь сезон цветения
Слайд 155
Топические сосудосуживающие средства
Могут назначаться кратковременно не более 5-7
дней при выраженной заложенности носа
Длительный прием способствует развитию медикаментозного
ринита
Побочные действия: тахикардия, аритмия, беспокойство, возбуждение
Слайд 156
АНТИЛЕЙКОТРИЕНОВЫЕ ПРЕПАРАТЫ
СИНГУЛЯР (МОНТЕЛУКАСТ)
При АР - в любое
время суток.
Дозы:
4 мг – жевательные таблетки с вкусом
вишни:
возраст 2-5 лет
5 мг – жевательные таблетки с вкусом вишни:
возраст 6-14 лет
10 мг – таблетки, покрытые оболочкой: возраст 15 и старше
Слайд 157
Профилактика -первичная
Соблюдение рациональной диеты беременной (исключать из рациона
питания высокосенсибилизирующие продукты, в т.ч. коровье молоко и соевый
белок)
Устранение проф. вредностей с 1-го месяца беременности
Прекращение активного и пассивного курения.
Естественное вскармливание. Не менее 4-6 месяцев – период число грудного вскармливания. Не рекомендуется раннее введение прикорма (не раннее 4-х месяцев по 1 компоненту)
При искусственном вскармливании применять частичные белковые гидролизаты (Нутрилон ГА, Нан ГА или Нэнни)
Ограничить контакты с внешними аэроаллергенами и поллютантами, так как способствуют ранней аллергизации
Слайд 158
Профилактика-вторичная
Контроль за окружающей средой: элиминация бытовых аллергенов, борьба
с курением и загрязнением окружающей среды;
Превентивная терапия антигистаминными препаратами
Профилактика
респираторных инфекций, как триггеров аллергии
Образовательные программы, которые направлены на улучшение понимание болезни, освоение самостоятельного контроля за симптомами заболевания, знакомство с принципами терапии.
Слайд 159
Атопический дерматит
хроническое аллергическое воспаление кожи, возникающее в результате
готовности иммунной системы к развитию аллергической реакции. Сопровождается кожным
зудом и частым инфицированием.
Частота АД составляет 10-20%
Слайд 160
Этиология
1. Пищевые аллергены:
белки коровьего молока. Коровье молоко
содержит до 15 антигенов,
наиболее активны: αS1 – казеин,
γ-казеин;
белок куриного яйца;
рыба и морепродукты;
пшеница;
антигены свинины и говядины и др.
высокосенсибилизирующие продукты (мед, орехи, шоколад и др.)
2. Аэроаллергены жилищ:
домашняя пыль,
клещи домашней пыли;
грибковые аллергены (плесневые)
- эпидермальные (аллерген кошки)
Слайд 161
Этиология
В ходе проведенного в США исследования выявлено, что
в 93%
случаев причиной пищевой аллергии являются 8 продуктов:
Слайд 163
Этиология
У детей раннего возраста
ведущими являются
пищевые аллергены.
У
детей старше 3-х лет
процент детей, имеющих
пищевую аллергию
уменьшается.
Ведущими становятся
аэроаллергены жилищ
Слайд 164
Патогенез
Специфическая и неспецифическая гиперреактивность
Нарушения обмена липидов и связанная
с этим повышенная сухость кожи
Нарушения физиологического шелушения
Снижение барьерной функции
кожи
Склонность к вторичному инфицированию
Слайд 165
Патогенез
Генетически обусловленное нарушение кожного барьера
– ключевой симптом
АД. В норме процесс кератинизации в клетках эпидермиса регулируется
белком, филаггрином (FLG). Мутации в гене FLG приводят к нарушению кожного барьера, проникновению через кожу аллергенов. Именно это является причиной дефектного эпидермального барьера у больных с АД.
Сухость кожи отмечается у всех больных независимо от стадии и степени тяжести АД
Слайд 167
Младенческая форма
В 70% случаев преобладает экзематозная форма (экссудативная)
с островоспалительными явлениями: эритема, микровезикулы, мокнущие бляшки, коркообразование;
В 30%
встречается эритематозно-сквамозная форма с гиперемией, шелушением, инфильтрацией (без мокнутия)
Локализация:
чаще – лицо (щеки, лоб), ягодицы
реже - туловище, разгибательные поверхности конечностей, распространенные поражения
Слайд 171
Детская форма
Хроническое воспаление – лихенификация (усиление и огрубение
кожного рисунка)
Преобладание лихеноидных папул
Ограниченный характер поражений
Локализация:
локтевые сгибы и
подколенные ямки,
сгибательные поверхности лучезапястных суставов,
тыльная поверхность кистей рук
Слайд 174
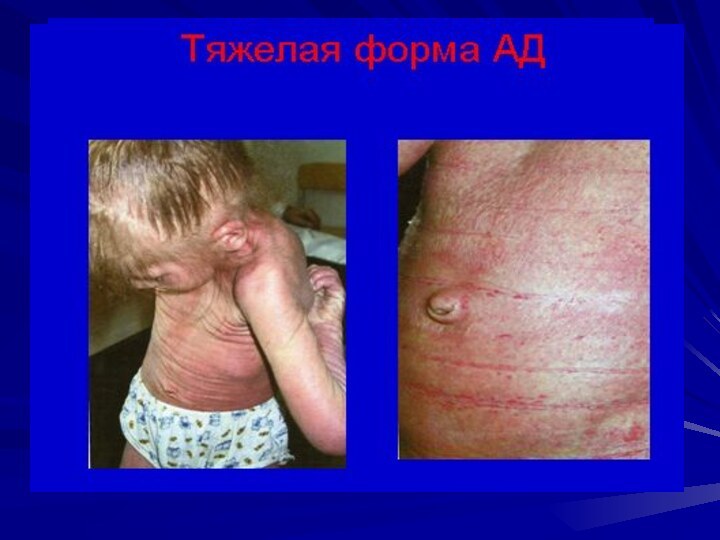
Подростковая форма
Диффузные инфильтративные высыпания
Сухость, лихенификация, зуд
Локализация: лицо,
шея, верхняя часть туловища и конечностей
Чаще является продолжением заболевания,
развившегося в младенческом или раннем детском возрасте. В подростковом возрасте АД начинается в 17% случаев
Слайд 176
Диагностика
Положительный аллергологический анамнез:
семейная отягощенность АЗ,
наличие у
ребенка других проявлений атопической болезни;
связь обострений с воздействием аллергена
(пищевых, бытовых);
анамнестические сведения о факторах риска (патология беременности, нарушение диеты, профессиональные вредности, ранний перевод на искусственное всармливание и др.).
Наличие клинических критериев заболевания
Повышение общего и спецефических IgE