Слайд 3
Классификация
противоревматических препаратов
I. Симптом – модифицирующие препараты:
А.
Нестероидные противовоспалительные препараты
Б. Глюкокортикостероидные гормоны
II. Болезнь - модифицирующие препараты:
А.
Цитотоксические препараты
Метотрексат
Азатиоприн
Циклофосфан
Циклоспорин А
Б. Нецитотоксические препараты
Аминохинолиновые производные
Препараты золота
Сульфасалазин
III. Болезнь – контролирующие препараты
Слайд 4
НПВП
лекарственные препараты, обладающие противовоспалительным, анальгетическим и жаропонижающим эффектами,
а также гастротоксичностью и антитромботическим действием.
Слайд 5
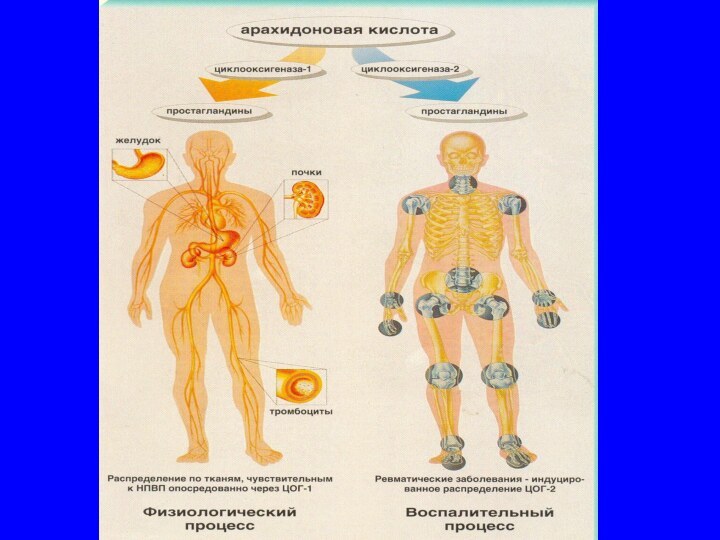
Механизм действия НПВП
1) ингибиция циклооксигеназы (ЦОГ) –
ключевого
фермента синтеза физиологических (ЦОГ – 1) и провоспалительных (ЦОГ
– 2) простагландинов;
Слайд 6
Функциональная активность ЦОГ - 1
Синтез физиологических простагландинов:
Простациклин
Тромбоксан А2
Простагландин Е2
Слайд 7
Патогенетическое значение
ЦОГ - 2
Синтез провоспалительных простагландинов:
воспаление
боль
лихорадка
ангиогенез
пролиферация синовиальной
оболочки
Слайд 9
Патогенетическая классификация НПВП
Селективные ингибиторы ЦОГ –1
Низкие дозы аспирина
2.
Неселективные ингибиторы ЦОГ
«Стандартные» НПВП
3. Преимущественно селективные ингибиторы ЦОГ –
2
Нимесулид
Мелоксикам
4. Селективные ингибиторы ЦОГ – 2
Целекоксиб
Рофекоксиб
5. Селективные ингибиторы ЦОГ – 3
Парацетамол
Слайд 10
Принципы назначения НПВП
1) начало лечения при постановке
диагноза,
2) лечение проводится длительно (до развития эффекта базисных препаратов
и достижения ремиссии),
3) назначение в достаточных дозах,
4) оценка эффекта в течение двух недель,
5) критерии эффективности - клинические признаки (выраженность и длительность болей и скованности, локальные признаки воспаления, функциональная способность).
Слайд 11
НПВП в педиатрии
НПВП Суточная доза,
Кратность приема
мг/кг
Диклофенак
2,5 – 3 3 – 4
Индометацин 2,5 – 3 3 – 4
Ибупрофен 30 – 40 3 – 4
Нимесулид 5 2 – 3
Напроксен 10 – 15 2 - 3
Слайд 12
Побочные эффекты НПВП
Желудочно – кишечные:
диспепсия, язвы, кровотечение,
перфорация
2. Кардио – ренальные:
артериальная гипертензия, периферические отеки
3. Тромбоцитарные:
нарушение
агрегации, повышение риска кровотечений
4. Печеночные:
повреждение печеночных клеток
5. Почечные:
снижение клубочковой фильтрации, интерстициальный нефрит
Слайд 13
Показания для системного назначения ГКС
1) наличие ярких
системных проявлений,
2) высокая персистирующая активность,
3) недостаточный эффект
от приема НПВП и внутрисуставного и/или внутривенного введения глюкокортикоидов.
Слайд 14
Принципы системной терапии
глюкортикостероидами - I
Назначение по строгим
показаниям
Незамедлительное назначение при явных показаниях
Назначение в оптимальной дозе
Оптимальный срок
применения (не превышать срок, необходимый для контроля активности болезни, в среднем 2 –3 недели)
Применение глюкокортикоидов короткого действия (преднизолон, метилпреднизолон)
Назначение в ранние утренние часы
Постепенное снижение
Слайд 15
Принципы системной терапии
глюкортикостероидами - II
Схема снижения
дозы преднизолона:
Постепенное снижение по ½ - ¼ таблетки каждые
5 – 10 дней до дозы 0,3 мг/кг
Снижение по альтернирующему методу: по ¼ таблетки каждые 2 недели только по четным или нечетным дням
Прием поддерживающей дозы 0.1 – 0,2 мг/кг в течение нескольких месяцев и лет
Слайд 16
Побочные эффекты ГКС
остеопороз,
усиление аппетита,
прибавка веса,
кушингоидный синдром,
ухудшение заживления ран,
повышение чувствительности к инфекциям,
задержка роста,
подавление гипоталамо-гипофизарно-надпочечниковой системы,
эрозивно-язвенное поражение ЖКТ,
артериальная гипертензия,
миопатия,
психические расстройства (возбудимость, бессонница).
Слайд 17
Метотрексат – «золотой стандарт»
лечения ЮРА
1) один
из самых эффективных стандартных БПВП;
2) может применяться в любой
стадии РА;
3) самая высокая длительная переносимость;
4) простое дозирование;
5) хорошо известные и контролируемые токсические реакции;
6) несложный мониторинг;
7) низкая стоимость.
Слайд 18
Дозирование метотрексата
(1 раз в неделю)
Стартовая доза –
10 мг/кв.м
Эффективная доза – 12,5-15 мг/кв.м
Максимальная доза – 20
мг/кв.м
Пульс-терапия – 30 мг/кв.м 1 раз в квартал
Слайд 19
Побочные эффекты:
1) эффекты, связанные с дефицитом фолатов
(стоматит, депрессии кроветворения);
2) идиосинкразические реакции;
3) реакции, связанные с накоплением
полиглютаминированных метаболитов (гепатотоксичность).
Слайд 20
Лефлюномид (Арава)
1) ингибирование активности фермента лигидрооротатдегидрогеназы,
2)
снижение синтеза пиримидинов, преимущественно в активированных Т-лимфоцитах.
Слайд 21
Дозирование лефлюномида
Ударная доза - 100 мг в
сутки в течение 3 дней
Поддерживающая доза 10-20 мг/сутки
Дети - 0,3-0,6 мг/кг.
Слайд 22
Показания для назначения циклоспорина А
1) неэффективность метотрексата,
2) системный вариант,
3) олигоартикулярный вариант с поражением глаз.
Слайд 23
Дозирование циклоспорина А
Стартовая доза - 3,0-3,5 мг/кг
в 2 приема с интервалом 12 часов
При отсутствии эффекта
в течение месяца доза постепенное увеличение дозы на 25 мг каждые 2 недели
Максимальная доза - 5 мг/кг
Слайд 24
Мониторинг нефротоксичности
Исходная концентрация креатинина Первые 3 месяца
каждые 2 недели После 6 месяцев: каждые 4-8 недель
Увеличение
уровня креатинина на 30-50%: снижение дозы
Увеличение дозы креатинина >50%: снижение дозы в 2 раза
Слайд 25
Сульфасалазин
Конъюгат 5 – аминосалициловой кислоты, обладающей противовоспательной
активностью, и сульфапиридина, оказывающего противомикробное действие.
Эффекты сульфасалазина:
- противовоспалительный,
- иммуномодулирующий (ингибиция синтеза ФНО-α, хемотаксиса, пролиферации эпителиальных клеток_.
Слайд 26
Схема применения сульфасалазин
Суточная доза - 30 –
40 мг/кг в 2 – 3 приема.
Стартовая доза
- 250 мг/сутки
Постепенное увеличение дозы (по 125 мг каждые 5-7 дней) в течение 2 – 4 недель
Мониторинг: общий и биохимический анализы крови каждые 2 недели, затем каждые 3 месяца
Слайд 27
Биологическая терапия
использование в терапевтических целях активных веществ,
играющих существенную роль в естественном функционировании основных биологических систем
организма – антител, цитокинов, клеточных рецепторов, их антагонистов и т.д
Слайд 28
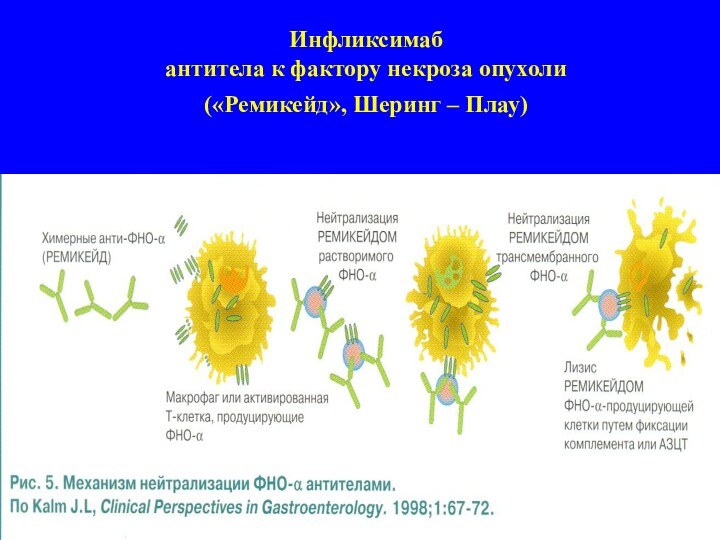
Инфликсимаб
антитела к фактору некроза опухоли
(«Ремикейд», Шеринг
– Плау)
Слайд 29
Методы биологической терапии
1. Нейтрализация ФНО-α с помощью
моноклональных антител (инфликсимаб, адалимумаб) или растворимых рецепторов (этанерцепт).
2. Нейтрализация
интерлейкина-1 (анакинра).
3. Анти-В-клеточная терапия (ритуксимаб).
4. Торможение взаимодействия иммунокомпетентных клеток (абатацепт, алефасепт).
5. Торможение функции CD4+лимфоцитов.
6. Нейтрализация интерферона-γ (фонтолизумаб).
7. Нейтрализация интерлейкина-6 (тоцилизумаб).
Слайд 30
Инфликсимаб
(«Ремикейд», Шеринг – Плау)
Схема применения:
Внутривенная
инфузия в дозе 3 мг/кг в течение 2 часов.
Повторные
введения через 2 и 6 недель после первой инфузии, затем каждые 8 недель
Слайд 31
Инфликсимаб
(«Ремикейд», Шеринг – Плау)
Показания:
Отсутствие
эффекта («неприемлемая активность болезни») на лечение метотрексатом в максимально
эффективной и переносимой дозе (20 мг/нед в течени 3 месяцев)
Противопоказания к назначению базисных противоревматических препаратов
Слайд 32
Показания для назначения ритуксимаба
1) активный (активность не
менее умеренной) РА при неадекватном ответе (или непереносимости) на
терапию ингибиторами ФНО;
2) при противопоказаниях к ингибиторам ФНО (особенно при лимфоме) и неадекватном ответе на терапию противоревматическими препаратами, модифицирующими заболевание.