- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Классификация и принцип действия химиопрепаратов. Принцип действия лучевой и таргетной терапии, радиочастотной абляции
Содержание
- 2. Лекарственная терапияприменение с лечебной целью лекарственных препаратов, которые замедляют развитие опухолевых клеток или необратимо повреждают их.
- 3. Принципы химиотерапии:выбор активных при данной опухоли препаратов;назначение
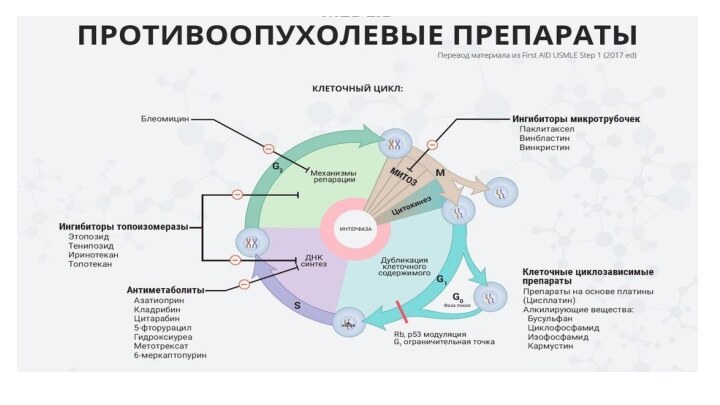
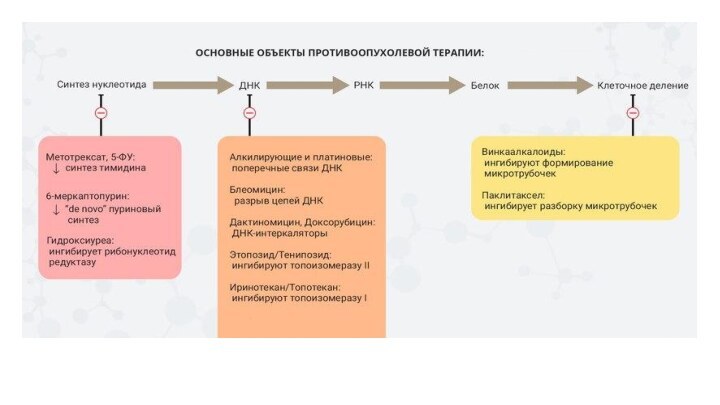
- 4. Классификация противоопухолевых препаратовАлкилирующие агентыАнтиметаболитыПротивоопухолевые антибиотикиПрепараты растительного и животного происхожденияФерментыГормоны и антигормоныТаргентные препаратыМодификаторы биологических реакцийОстемодифицирующие препараты
- 7. I. АЛКИЛИРУЮЩИЕ АГЕНТЫвещества различной химической структурыМеханизм действия:разрушают
- 8. Классификация алкилирующих агентов:Хлорэтиламины (мехлорэтамин, мелфалан, хлорамбуцид, циклофосфамид,
- 9. II. АНТИМЕТАБОЛИТЫМеханизм действия:Вступают в конкурентные отношения с
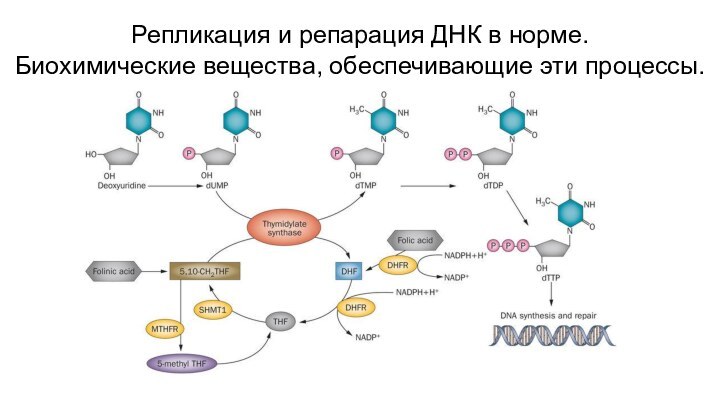
- 10. Репликация и репарация ДНК в норме. Биохимические вещества, обеспечивающие эти процессы.
- 11. Классификация антиметаболитов:Антифолаты – метотрексат (наиболее часто используют
- 12. III. ПРОТИВООПУХОЛЕВЫЕ АНТИБИОТИКИОказывают иммунодепрессивное и антибактериальное действие,
- 13. Классификация противоопухолевых антибиотиков:Антрациклины – наиболее эффективны (карминомицин,
- 14. IV. ПРЕПАРАТЫ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ1) Микротрубочковые ингибиторыВинкаалколоиды, содержащиеся
- 15. Механизм действия винкаалкалоидов – денатурация белка тубулина
- 17. V. ФЕРМЕНТЫПр.: L-аспарагиназа, протеазы «+»-быстрое снижение объема
- 18. VI. ГОРМОНЫ И АНТИГОРМОНЫЗлокачественные опухоли могут развиваться
- 19. Классификация гормонов:Андрогены (тестостерона пропионат, метилтестостерон)Эстрогены и их
- 20. Классификация гормонов:Кортикостероиды (дексаметазон, преднизолон, метилпреднизолон)Ингибиторы ароматазы: Нестероидные
- 21. VII. ТАРГЕТНЫЕ ПРЕПАРАТЫНазначение таргетной терапии зависит от
- 22. Классификация таргетных препаратов (с учетом механизма
- 23. Классификация таргетных препаратов (с учетом механизма
- 25. Классификация таргетных препаратов (с учетом механизма действия):Ингибиторы протеасом бортезомиб, карфилзомибИнгибиторы рецепторов ретиноидов третиноинАнтисмысловые нуклеотиды облимерсен
- 27. VIII. МОДИФИКАТОРЫ БИОЛОГИЧЕСКИХ РЕАКЦИЙОсновные биологические эффекты —
- 28. Классификация модификаторов биологических реакций:Цитокины: Интерфероны (ИФН-α,
- 29. IX. ОСТЕОМОДИФИЦИРУЮЩИЕ ПРЕПАРАТЫБисфосфонатыМоноклональное антитело против RANKLМеханизм действия:
- 30. Общие побочные эффекты химиотерапии:Потенциально необратимая кумулятивная дозозависимая
- 32. К абсолютным противопоказаниям к назначению лекарственной терапии
- 33. Принцип действия лучевой терапииРадикальное лечение предусматривает полное
- 34. Применение лучевой терапии
- 35. Принцип действия радиочастотной терапииАблация – это методика
- 36. Скачать презентацию
- 37. Похожие презентации






















Слайд 2
Лекарственная терапия
применение с лечебной целью лекарственных препаратов, которые
замедляют развитие опухолевых клеток или необратимо повреждают их.
Слайд 3
Принципы химиотерапии:
выбор активных при данной опухоли препаратов;
назначение адекватных
доз препаратов и соблюдение режимов их введения;
коррекция доз и
режимов введения препаратов с учётом индивидуальных клинических ситуаций
Слайд 4
Классификация противоопухолевых препаратов
Алкилирующие агенты
Антиметаболиты
Противоопухолевые антибиотики
Препараты растительного и животного
происхождения
Ферменты
Гормоны и антигормоны
Таргентные препараты
Модификаторы биологических реакций
Остемодифицирующие препараты
Слайд 7
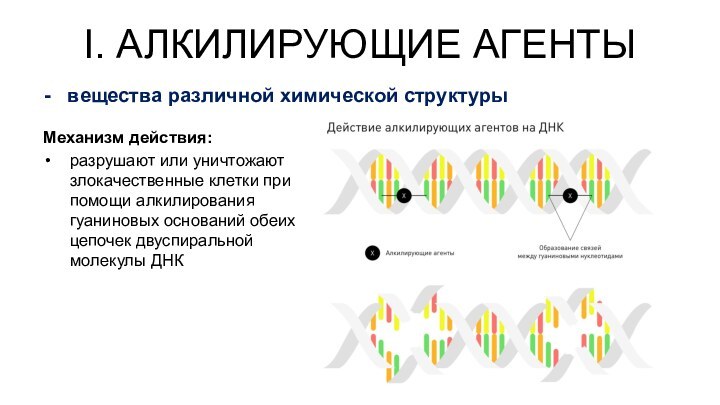
I. АЛКИЛИРУЮЩИЕ АГЕНТЫ
вещества различной химической структуры
Механизм действия:
разрушают или
уничтожают злокачественные клетки при помощи алкилирования гуаниновых оснований обеих
цепочек двуспиральной молекулы ДНК
Слайд 8
Классификация алкилирующих агентов:
Хлорэтиламины (мехлорэтамин, мелфалан, хлорамбуцид, циклофосфамид, ифосфамид,
сарколизин, допан)
Производные нитрозомочевины (кармустин, ломустин, лизомустин, араноза)
Этиленимины (тиофосфамид, имифос,
фотрин, гексаматилмеламин)Эфиры дисульфоновых кислот (бусульфан)
Комплексные соединения платины (цисплатин, карбоплатин)
Триазины (дакарбазин, прокарбазин)
Слайд 9
II. АНТИМЕТАБОЛИТЫ
Механизм действия:
Вступают в конкурентные отношения с нормальными
метаболитами и блокируют обменные процессы в клетках, что приводит
к нарушению передачи генетической информации и пролиферации клеток.аналоги веществ, обеспечивающих нормальные биохимические реакции в клетке
Слайд 11
Классификация антиметаболитов:
Антифолаты – метотрексат (наиболее часто используют при
опухолях шеи и головы, также при хорионэпителиоме и раке
молочной железы)Ингибиторы тимидилатсинтетазы – ралтитрексид
Фторпиримидины – 5-фторурацил, тегафур, фторфуран (применяются при неоперабельных формах рака желудка и кишечника)
Аналоги цитидина – цитарабин, гемцитабин
Антагонисты пуринов - меркаптопурин
Ингибиторы рибонуклеозиддифосфатредуктазы - гидроксимочевина
Слайд 12
III. ПРОТИВООПУХОЛЕВЫЕ АНТИБИОТИКИ
Оказывают иммунодепрессивное и антибактериальное действие, но
не применяются в качестве антимикробных средств
Механизм действия:
Ингибирование синтеза нуклеиновых
кислот путем нарушения вторичной спирализации ДНКСвязывание с липидами клеточных мембран и изменение транспорта ионов
Слайд 13
Классификация противоопухолевых антибиотиков:
Антрациклины – наиболее эффективны (карминомицин, доксимицин,
идарубин, валрубин, даунорубицин)
Флеомицины (блеомицин, блеомицитин, пепломицин)
Блеомицин = смесь различных
гликопептидов, часто применяется для комбинированного лечения тестикулярных видов ракаПрозводные ауреловой кислоты (оливомицин, пликамицин)
Прочие антибиотики (брунеомицин, митомицин) действуют аналогично алкилирующим агентам
Актиномицины синтезируются актиномицетами (дактиномицин)
Слайд 14
IV. ПРЕПАРАТЫ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ
1) Микротрубочковые ингибиторы
Винкаалколоиды, содержащиеся в
растениях барвинок розовый (винбластин, винкристин, эрибулин)
Таксаны, синтезируемые из европейского
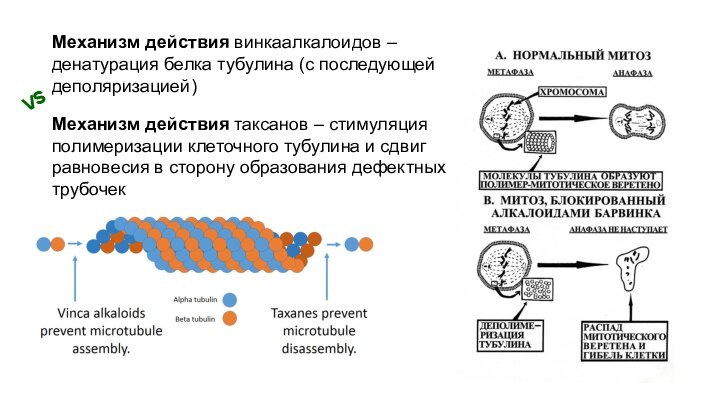
тисса (паклитаксен, иксабепилон)Слайд 15 Механизм действия винкаалкалоидов – денатурация белка тубулина (с
последующей деполяризацией)
Механизм действия таксанов – стимуляция полимеризации клеточного тубулина
и сдвиг равновесия в сторону образования дефектных трубочекVS
Слайд 17
V. ФЕРМЕНТЫ
Пр.: L-аспарагиназа, протеазы
«+»
-быстрое снижение объема и размеров
опухоли
(уменьшение болевых патологий)
Современная стратегия энзимотерапии в отношении новообразований
построена с учетом разной чувствительности нормальных клеток и клеток опухоли к эссенциальным факторам роста. К факторам, стимулирующим рост, относятся пищевые факторы и ряд «заменимых» веществ (заменимых аминокислот), к недостатку которых клетки новообразований оказываются более чувствительными, чем нормальные.
Слайд 18
VI. ГОРМОНЫ И АНТИГОРМОНЫ
Злокачественные опухоли могут развиваться непосредственно
в эндокринных органах.
В некоторых органах и тканях, не
обладающих эндокринной секрецией, имеются гормональные рецепторы (в молочной железе, яичниках, матке, предстательной железе)Известен факт эктопического гормонообразования — продукции гормоноподобных веществ в опухолевой ткани органов, нормальные клетки которых не являются эндокринными.
снижение уровня гормонов, стимулирующих рост опухоли
блокирование стимулирующего действия гормонов на клетки опухоли (воздействие на клетки-мишени);
повышение чувствительности клеток опухоли к цитостатикам и использование гормонов в качестве носителей ХП.
Механизм действия:
Слайд 19
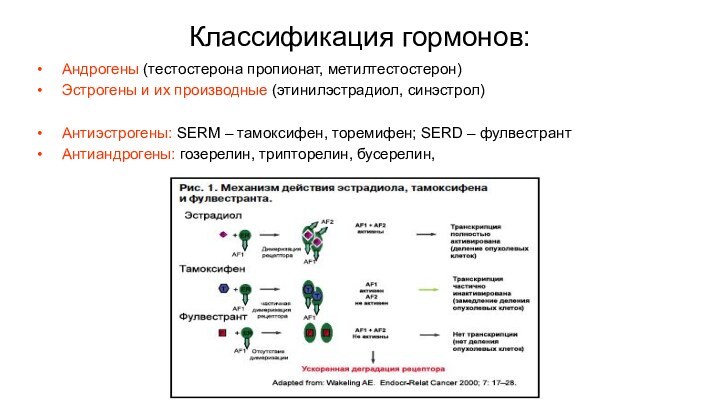
Классификация гормонов:
Андрогены (тестостерона пропионат, метилтестостерон)
Эстрогены и их производные
(этинилэстрадиол, синэстрол)
Антиэстрогены: SERM – тамоксифен, торемифен; SERD – фулвестрант
Антиандрогены:
гозерелин, трипторелин, бусерелин,
Слайд 20
Классификация гормонов:
Кортикостероиды (дексаметазон, преднизолон, метилпреднизолон)
Ингибиторы ароматазы:
Нестероидные - летрозол,
анастрозол, аминоглутетимид; стероидные - эксеместан
Аналоги соматостатина (октреотид)
Супрессоры коры надпочечников
(митотан)Гормоны щитовидной железы (левотироксин)
Гормоноцитостатики (экстрамустин, преднимустин)
Слайд 21
VII. ТАРГЕТНЫЕ ПРЕПАРАТЫ
Назначение таргетной терапии зависит от наличия
специфических рецепторов в самих опухолевых клетках. Наличие этих рецепторов
определяется иммуногистохимическим анализом либо FISH — исследованием биоптата.«+»
- высокая специфичность
избирательность лекарственного препарата на клетки мишени
минимальное влияние на организм.
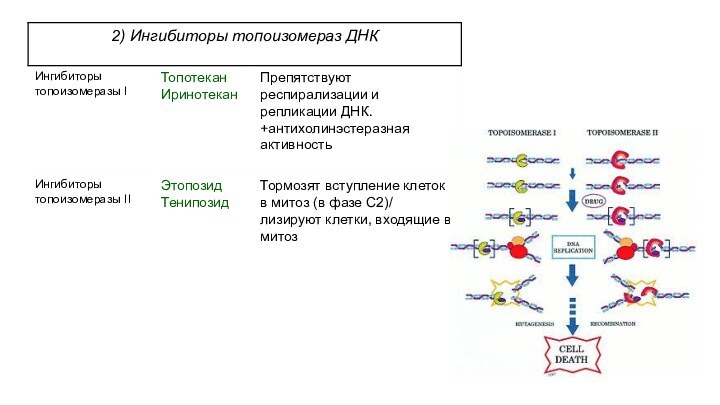
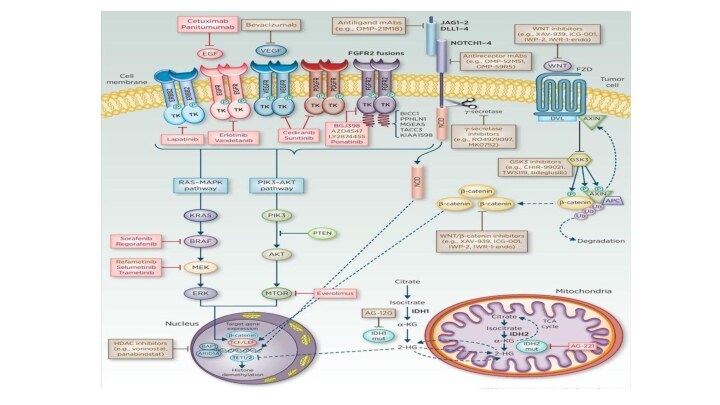
Слайд 22
Классификация таргетных препаратов
(с учетом механизма действия):
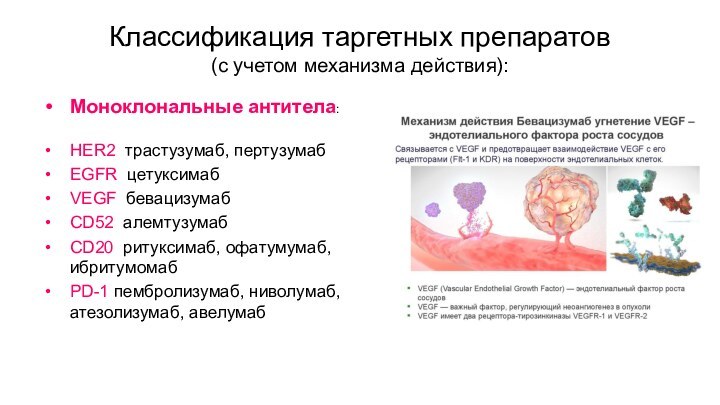
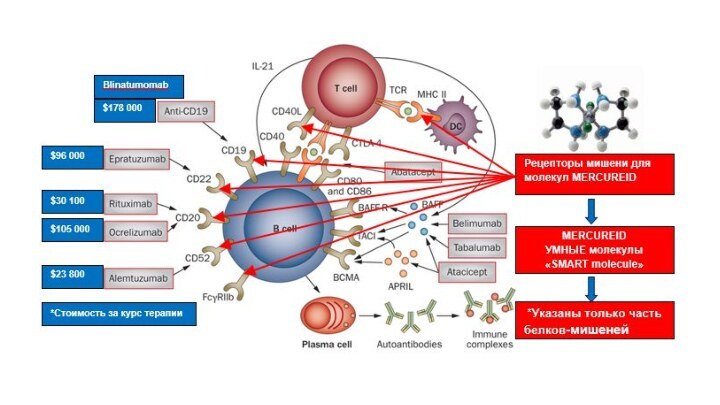
Моноклональные антитела:
HER2
трастузумаб, пертузумаб
EGFR цетуксимаб
VEGF бевацизумаб
CD52 алемтузумаб
CD20 ритуксимаб, офатумумаб, ибритумомаб
PD-1 пембролизумаб,
ниволумаб, атезолизумаб, авелумаб
Слайд 23
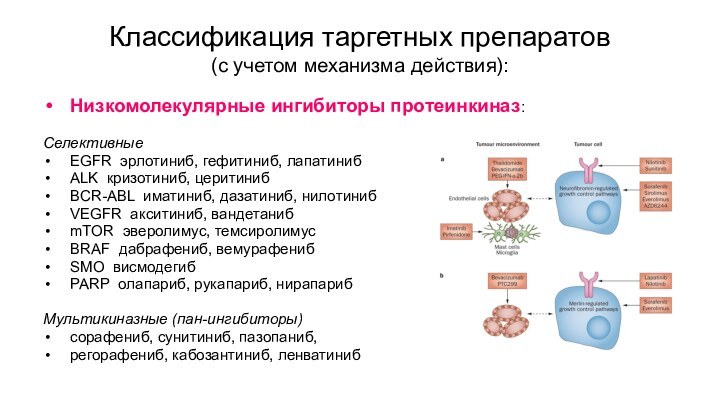
Классификация таргетных препаратов
(с учетом механизма действия):
Низкомолекулярные ингибиторы
протеинкиназ:
Селективные
EGFR эрлотиниб, гефитиниб, лапатиниб
ALK кризотиниб, церитиниб
BCR-ABL иматиниб, дазатиниб, нилотиниб
VEGFR
акситиниб, вандетанибmTOR эверолимус, темсиролимус
BRAF дабрафениб, вемурафениб
SMO висмодегиб
PARP олапариб, рукапариб, нирапариб
Мультикиназные (пан-ингибиторы)
сорафениб, сунитиниб, пазопаниб,
регорафениб, кабозантиниб, ленватиниб
Слайд 25
Классификация таргетных препаратов
(с учетом механизма действия):
Ингибиторы протеасом
бортезомиб, карфилзомиб
Ингибиторы рецепторов ретиноидов третиноин
Антисмысловые нуклеотиды облимерсен
Слайд 27
VIII. МОДИФИКАТОРЫ БИОЛОГИЧЕСКИХ РЕАКЦИЙ
Основные биологические эффекты —
модуляция
иммунных реакций
антипролиферативная активность (замедление клеточного цикла и переход в
фазу покоя)регуляция дифференцировки опухолевых клеток (контроль за пролиферацией)
ингибирование онкогенов
биомодуляция цитостатиков
ингибирование ангиогенеза
Слайд 28
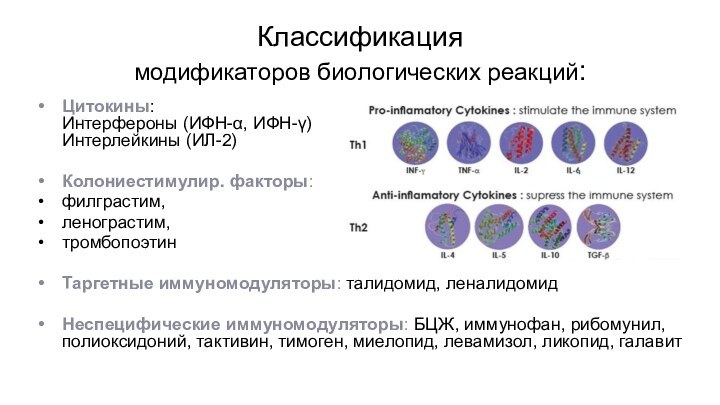
Классификация
модификаторов биологических реакций:
Цитокины:
Интерфероны (ИФН-α, ИФН-γ)
Интерлейкины (ИЛ-2)
Колониестимулир. факторы:
филграстим,
ленограстим,
тромбопоэтин
Таргетные иммуномодуляторы: талидомид, леналидомид
Неспецифические иммуномодуляторы: БЦЖ, иммунофан,
рибомунил, полиоксидоний, тактивин, тимоген, миелопид, левамизол, ликопид, галавит
Слайд 29
IX. ОСТЕОМОДИФИЦИРУЮЩИЕ ПРЕПАРАТЫ
Бисфосфонаты
Моноклональное антитело против RANKL
Механизм действия: связывание
и ингибирование RANK-лиганда, что тормозит созревание остеокластов
Только при
наличии костных метастазов, подтвержденных на КТ/МРТТерапия начинается сразу же при выявлении метастазов (даже при отсутствии клинических признаков)
НЕ РЕКОМЕНДУЕТСЯ использовать у пациентов с метастазами в других органах при отсутствии метастазов в кости
Слайд 30
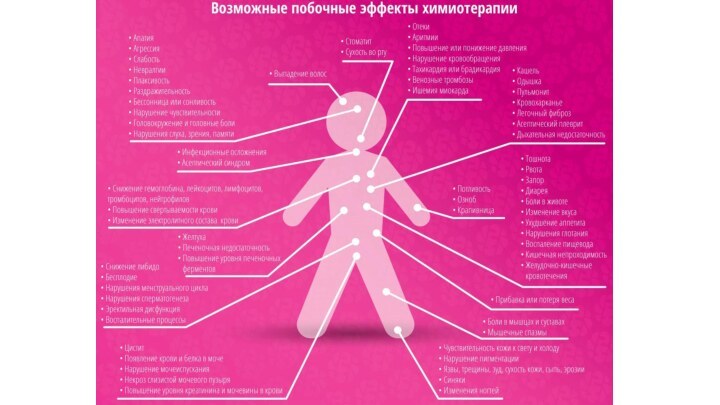
Общие побочные эффекты химиотерапии:
Потенциально необратимая кумулятивная дозозависимая КАРДИОТОКСИЧНОСТЬ
АНАФИЛАКТИЧЕСКИЙ
ШОК
РЕСПИРАТОРНАЯ ТОКСИЧНОСТЬ
ЛИХОРАДКА
МИЕЛОСУПРЕССИЯ (вплоть до развития апластической анемии)
ГЕМАТОТОКСИЧНОСТЬ
ГАСТРОИНТЕСТИНАЛЬНАЯ ТОКСИЧНОСТЬ
АЛОПЕЦИЯ
ПЕРИФЕРИЧЕСКИЕ НЕЙРОПАТИИ
Слайд 32
К абсолютным противопоказаниям к назначению лекарственной терапии относят:
тяжёлое
общее состояние больного;
угнетение кроветворения;
гнойные процессы и распад опухоли;
инфекционные заболевания;
кровохарканье;
инфаркт
миокарда;острое нарушение мозгового кровообращения;
выраженная сердечно-сосудистая недостаточность;
тяжёлое нарушение функции печени и почек;
тяжёлый сахарный диабет.
Слайд 33
Принцип действия лучевой терапии
Радикальное лечение предусматривает полное уничтожение,
как первичного очага опухоли, так и возможных метастазов.
Паллиативное
лечение преследует цель задержать рост и развитие опухоли, продлить жизнь больному. Симптоматическое лечение назначается, чтобы снять какие либо тяжелые проявления опухолевого роста, например, сдавливание опухолью прилежащих органов с развитием тяжелых функциональных расстройств.
В технике лучевой терапии используются два основных технических подхода:
Телетерапия (tele = дальний) подразумевает, что лечение проводится на расстоянии, с помощью того или иного аппарата.
Брахитерапия (brachy = короткий) проводится, когда источник радиации помещается рядом или внутрь облучаемого объекта. При этом источник может оставаться в ткани (как, например, золото-198 или йод-125) или должен быть удален (цезий-137, иридий-192, кобальт-60).
Слайд 35
Принцип действия радиочастотной терапии
Аблация – это методика прямого
направленного разрушения ткани, которое достигается путем термического либо химического/
электрохимического воздействияНаиболее применяемый сегодня метод - радиочастотная деструкция. Эта технология подразумевает введение специального атравматичного электрода в опухоль и воздействие на последнюю током частотой 450-500 кГц.
В результате опухолевая ткань разогревается до температуры (60-90°С), при которой происходят необратимые изменения в клетках. Опухолевая масса некротизируется.
Современные РЧ системы дают возможность получать область некроза до 7 см в диаметре в ходе одной аппликации.