Слайд 2
ЭПИДЕМИОЛОГИЯ И ФАКТОРЫ РИСКА

Печеночноклеточный (гепатоцеллюлярный) рак
Составляет 90% всех первичных злокачественных опухолей печени и внутрипеченочных желчных протоков. В мире от первичного рака печени ежегодно умирает 1 млн 250 тыс. человек. Ввиду многократного превалирования гепатоцеллюлярного рака над холангиоцеллюлярным (рак внутрипеченочных желчных протоков) и другими формами первичного рака печени, понятие первичный рак печени (ПРП) в данных по эпидемиологии опухолей отождествляется с понятием печеночноклеточный рак. ПРП стоит на восьмом месте в ряду наиболее распространенных опухолей в мире: на шестом месте среди опухолей у мужчин и на одиннадцатом — у женщин. Заболеваемость ПРП значительно отличается в различных географических зонах. Страны мира по заболеваемости ПРП делятся на 3 группы.
Первая группа — страны с высоким уровнем заболеваемости, свыше 20 человек на 100 тыс. населения. Это Мозамбик, Зимбабве, ЮАР, Мали, Гамбия, Китай, Гонконг, Сингапур.
Вторая группа — страны со средним уровнем заболеваемости, от 6 до 19 человек на 100 тыс. населения. Это Аргентина, Бразилия, другие страны Центральной и Южной Америки.
Третья группа — страны с низким уровнем заболеваемости, не превышающим 5 человек на 100 тыс. населения. Это страны Западной Европы, Россия, Индия, США, Канада, Австралия.
Слайд 3
ЭПИДЕМИОЛОГИЯ И ФАКТОРЫ РИСКА
Частота печеночноклеточного рака среди лиц
с выявленными антителами к вирусу гепатита С в 4
раза выше, чем среди носителей HBsAg (приблизительно 0,01-2% доноров крови во всем мире являются носителями вируса гепатита С). Среди мужчин заболеваемость в 1,5-8 раз выше, чем среди женщин. Страны с высоким уровнем заболеваемости являются эндемичными по заболеваемости вирусным гепатитом В — у 80% больных в крови определяется поверхностный антиген вируса гепатита В.
В странах с низким уровнем заболеваемости у 80-90% заболевших гепатоцеллюлярным раком в крови не определяется поверхностный антиген вируса гепатита В. В то же время в этих странах не менее чем у 50% больных ПРП, серонегативных по вирусному гепатиту В, в крови выявляются антитела к вирусу гепатита С.
Слайд 4
ЭПИДЕМИОЛОГИЯ И ФАКТОРЫ РИСКА
В России (2000 г. )

заболеваемость ПРП среди мужчин - 6, среди женщин -
4.1 тыс. на 100 тыс.населения. Средний возраст заболевших мужчин - 64,2 г., женщин - 68,3 г. Наиболее высокая заболеваемость ПРП в России отмечается на Дальнем Востоке (среди мужчин - 8,4, среди женщин — 3,5).
Смертность по причине ПРП среди мужчин -7 , среди женщин – 4,7 на 100 тыс. В структуре смертности населения от злокачественных опухолей у мужчин доля ПРП составляет 2,9% (9-е место причин смерти от злокачественных новообразований), у женщин - 2,7% (10-е место). Средний возраст умерших по причине ПРП совпадает со средним возрастом заболевших. В России максимальные показатели смертности по причине ПРП среди мужчин и женщин отмечается на Дальнем Востоке (9,4 и 3,7 человек соответственно). Приблизительно одинаковое ежегодное количество больных с впервые обнаруженным ПРП и умерших по причине ПРП как в России, так и в других странах свидетельствует, во-первых, о поздней диагностике ПРП, а, во-вторых, о неудовлетворительных результатах лечения .
В Краснодарском крае заболеваемость ПРП составляет 6,0 на 100 тыс. нас. (2008г.), смертность – 7,2 (2007г.). Заболеваемость выше у мужчин и составляет 6,3 (2007г.), у женщин – 4,2 (2007г.)
Слайд 5
ФАКТОРЫ РИСКА ДЛЯ ГЕПАТОЦЕЛЛЮЛЯРНОГО РАКА ПЕЧЕНИ
Вирусные гепатиты В,

С и др.
Цирроз печени любой этиологии.
Наследственные метаболические заболевания
печени (поздняя кожная порфирия, острая перемежающаяся порфирия, смешанная порфирия, гликогеноз I типа, гликогеноз III типа, гиперцитруллинемия, фруктоземия, тирозинемия, недостаточность
альфа-1-антитрипсина, идиопатический гемохроматоз, гепатолентикулярная дегенерация (болезнь Вильсона – Коновалова), прогрессирующий внутрипеченочный холестаз (болезнь Байера), артериопеченочная дисплазия).
Венозное полнокровие печени при синдроме Бадда—Киари.
Экзогенные (пероральные) стероидные гормоны (например, доказана связь гепатоцеллюлярного рака с применением половых стероидных гормонов в регионах, не эндемичных по вирусному гепатиту В).
Пищевые микотоксины (афлатоксины).
Химические агенты разных групп: торотраст — коллоидный раствор диоксида радиоактивного тория, применяемый ранее как рентгеноконтрастный препарат, винилхлорид, алкалоиды пирролизидина, дубильная кислота, ароматические азосоединения (моноазобензол, N,N-диметил-4-аминоазобензол), сафрол, ароматические аминосоединения (2-нафтиламин, производные 2-флуоренилацетамида и др.), нитрозамины, азатиоприн и др.
Эндогенные метаболиты тирозина.
Наследственный анамнез, отягощённый первичным раком печени.
Слайд 6
Патологическая анатомия и особенности клинического течения ПРП
Гистологически первичный

рак печени и внутрипеченочных желчных протоков представлен следующими формами:
Гепатоцеллюлярный рак, его гистологические варианты - трабекулярный, псевдожелезистый (ацинарный), компактный, скиррозный, плеоморфный, светлоклеточный, фиброламеллярный (с грубой коллагеновой стромой);
Холангиоцеллюлярный рак - аденокарцинома внутрипеченочных желчных протоков. Опухолевые клетки напоминают эпителий желчных протоков, иногда они образуют папиллярные структуры. Секреция желчи отсутствует. Гистологически опухоль не отличается от метастазов аденокарциномы в печень. Иммуноморфологическое исследование на кератин позволяет установить билиарное происхождение аденокарциномы;
Смешанный гепатохолангиоцеллюлярный рак содержит участки как гепатоцеллюлярного, так и холангиоцеллюлярного рака;
Внутрипротоковая цистаденокарцинома - кистозная опухоль, чаще локализуется в правой доле печени, содержит окрашенную желчью слизь. Гистологически кисты выстланы злокачественными эпителиальными клетками, образующими папиллярные структуры, содержат выраженную фиброзную строму;
Гепатобластома - развивается преимущественно у детей до 4-летнего возраста. Гистологическая структура опухоли отражает стадии эмбрионального развития печени.
Недифференцированный рак - эпителиальная злокачественная опухоль, о гистогенезе которой в силу низкой дифференцировки клеток можно судить лишь ориентировочно .
Первые три формы превалируют по частоте, а среди них гепатоцеллюлярная форма - абсолютно преобладает в структуре ПРП.
Слайд 7
МАКРОСКОПИЧЕСКИЕ ФОРМЫ ПРП
Массивная форма:

- простая – один крупный узел без метастазов;
- с сателлитами – один крупный узел с одним или более метастазами (сателлитами) вокруг.
Встречается в 10-43% случаев ПРП.
Узловая форма - в печени 2 или больше опухолевых узлов, схожих по размерам. Могут быть мелкие узелки вокруг основных узлов, возможно слияние узлов в конгломерат. Узловая макроскопическая форма наиболее характерна для ПРП, встречается в 52-84% случаев.
Диффузная форма - опухоль в виде неравномерной инфильтрации печени или множественные опухолевые узлы, с трудом дифференцирующиеся от узлов регенераторной гиперплазии печени. Всегда поражены обе доли печени. Почти у половины больных сочетается с циррозом печени. Печень на разрезе имеет пятнистый вид и внешне не отличается от цирротической печени. Без гистологического исследования установить диагноз почти невозможно. Встречается у 3,9-19,6% больных ПРП.
Печеночноклеточная опухоль па ножке - чрезвычайная редкость, описаны единичные наблюдения. Чаще диагностируется высокодифференцированная инкапсулированная форма гепатоцеллюлярного рака
Слайд 8
РАСПРОСТРАНЕНИЕ ПРП
Происходит в результате непосредственного прорастания опухолью окружающих
органов и тканей и путем метастазирования.
Гематогенный путь метастазирования (основной):
чаще в печень, легкие, диафрагму; реже - в кости, надпочечники, почки, другие органы.
Лимфогенный путь метастазирования - в лимфоузлы ворот печени, гепатодуоденальной связки, панкреатодуоденальные, парааортальные л/у.
Имплантационный путь метастазирования - по париетальной и висцеральной брюшине.
По данным ГУ РОНЦ им. Н.Н. Блохина РАМН, виутриорганные метастазы отмечаются у 64% больных гепатоцеллюлярным раком и реже при холангиоцеллюлярном раке.
Слайд 9
КЛИНИКА ПРП
Клинические проявления ПРП многообразны и неспецифичны. Симптоматика
зависит от выраженности заболевания печени, на фоне которого развился
ПРП, распространенности опухоли, наличия осложнений ПРП и свидетельствует о запущенности заболевания, но не исключает возможность хирургического удаления опухоли. Все клинические классификации ПРП в большей или меньшей степени рассматривают синдромы и симптомы, практически малополезные для лечения пациента, так как указанные клинические проявления обусловлены или генерализацией заболевания, или опухолью значительных размеров на фоне цирроза печени, или выраженной дисфункцией печени.
Паранеопластические синдромы
Для 10-15% всех больных ПРП характерны паранеопластические синдромы: гипогликемия (у 30% больных ПРП в терминальной стадии), кожный зуд без желтухи, гинекомастия, атрофия яичек, гиперпаратиреоз, гипертиреоз, гиперкортицизм, гиперхолестеринемия, гипокалиемия, эритроцитоз, гиперкальциемия и остеопороз, гипертрофическая остеоартропатия и др.
Гипогликемический синдром связан с нарушением инактивации инсулина в клетках печени, усиленным гликогенозом в опухолевых клетках, секрецией опухолью веществ, стимулирующих бета-клетки поджелудочной железы.
Слайд 11
КЛИНИКА ПРП
Клиническая классификация
ПРП (Шапкин B.C., 1970)
типичный рак;
цирроз-рак;
осложненный рак;
"маскированный", или метастатический рак;
бессимптомный,
или скрыто протекающий ПРП.
Указанная классификация в основном касается больных ПРП в странах, не эндемичных по вирусному гепатиту В, то есть, пациентов с более или менее длительным анамнезом предсуществующего диффузного неопухолевого поражения печени, например, цирроза.
Слайд 12
КЛИНИКА ПРП
Клиническая картина "типичного" ПРП в значительной степени

слагается из общих симптомов: нарастающая слабость, ухудшение аппетита, похудание,
изменение вкусовых ощущений. Указанные общие симптомы практически неотличимы от таковых при циррозе печени без ПРП. Позднее присоединяются тошнота, рвота, субфебрильная или умеренно высокая лихорадка. Чувство тяжести в области печени нарастает и приобретает характер постоянной тупой боли. Отмечается гепатомегалия. Пальпируемая при этом в 58-93% случаев опухоль чаще всего заставляет пациента обратиться к врачу. Спленомегалия обусловлена или циррозом печени и развитием печеночной портальной гипертензии, или нарушением портального кровообращения, вызванным сдавлением опухолью ветвей воротной вены. Отмечается у 10-39% больных ПРП. Желтуха при ПРП всегда носит холестатический характер и либо свидетельствует о прогрессировании гепатита-цирроза (у
2/3 больных ПРП), либо обусловлена опухолевым стенозом крупных желчных протоков в воротах печени. Асцит отмечается у 19-40% больных и свидетельствует о нарушении портального кровообращения (сдавление, тромбоз воротной вены), постсинусоидальном блоке лимфо- и кровообращения в печени при прогрессировании цирроза, опухолевой диссеминации по брюшине. Угнетение белково-синтетической функции печени усугубляет отечно-асцитический синдром. Лихорадка у 13—38% больных ПРП, как правило, резистентна к антибиотикам и носит различный характер: от длительной и постоянной на уровне небольших колебаний в диапазоне субфебрильных и умеренно высоких цифр до перемежающейся с суточными колебаниями 1 °С и выше (febris remittens). Происхождение ее до конца не ясно.
Слайд 13
КЛИНИКА ПРП
2. Цирроз-рак. У больного всегда имеется длительный

анамнез цирроза печени. Развивается диффузная форма первичного рака печени.
О
развитии ПРП свидетельствует ухудшение состояния больного с преобладанием общих симптомов. Хотя интенсивность болей в области печени также увеличивается. При этом опухоль не пальпируется, печень не увеличена. Тяжесть состояния резко усугубляется повторяющимися
желудочно-пищеводными кровотечениями, асцит перестает купироваться лекарственной терапией.
3. Осложненный рак печени. Данную клиническую форму ПРП
принято выделять, когда заболевание, протекающее бессимптомно или
субклинически, сразу проявляется осложнениями. Тромбоз воротной
вены и ее ветвей, печеночных артерий, тромбоз печеночных вен и НПВ
(синдром Бадди - Киари) с развитием острой печеночной недостаточно
сти, распад опухоли с разрывом печени и внутрибрюшным кровотечением, формирование артерио-портальных шунтов, развитие механической желтухи, желчных свищей, гемобилии, формирование внутрипеченочных абсцессов.
Слайд 14
КЛИНИКА ПРП
4. "Маскированный" рак печени. Симптомокомплекс, обусловленный внепеченочными

метастазами ПРП. Подразумевают клинические формы ПРП, симптоматика которых обусловлена
не первичной опухолью, а метастазами. При метастазах в легкие - легочная форма, при метастазах в головной мозг - мозговая форма, при поражении метастазами костей - костная форма и др.
5. Бессимптомный, или скрыто протекающий ПРП. Выявляется
случайно при лапаротомии не по поводу ПРП, во время аутопсии без
прижизненного диагноза ПРП, при патолого-анатомическом исследовании печени, удаленной во время трансплантации по поводу неопухолевого поражения печени. Именно в этой клинической группе опухоль печени может оказаться небольших размеров, менее 3 см в наибольшем измерении.
Средняя продолжительность жизни после начала клинических проявлений заболевания без лечения 4,3-6 мес. Есть данные, указывающие на разную скорость роста и прогрессирования гепатоцеллюлярного рака в разных странах. В странах, не эндемичных по вирусному гепатиту В, время удвоения массы опухоли составляет 6 мес, что выше, чем у коренных жителей в странах, эндемичных по вирусному гепатиту В.
Слайд 15
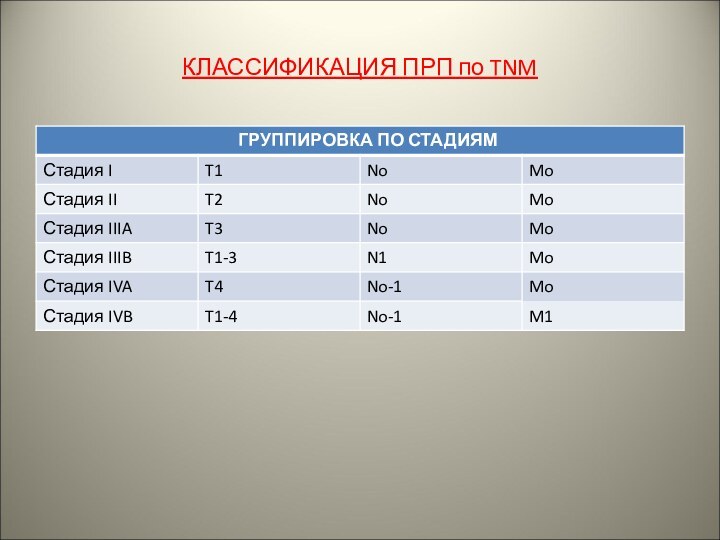
КЛАССИФИКАЦИЯ ПРП по TNM
Критерий Т:
Т1 — солитарная опухоль до 2 см в наибольшем измерении без инвазии сосудов;
Т2 — солитарная опухоль до 2 см в наибольшем измерении с инвазией сосудов или множественные опухоли до 2 см без инвазии сосудов, ограниченные одной долей, или солитарная опухоль более 2 см без инвазии сосудов;
Т3 — солитарная опухоль более 2 см в наибольшем измерении с инвазией сосудов или множественные опухоли не более 2 см в наибольшем измерении с инвазией сосудов, ограниченные одной долей, или ограниченные одной долей множественные опухоли, любая из которых более 2 см с или без инвазии сосудов;
Т4 — множественные опухоли в обеих долях или опухоль, поражающая основную ветвь портальной или печеночной вены. Прорастание висцеральной брюшины.
Слайд 16
КЛАССИФИКАЦИЯ ПРП по TNM
Критерий N:
No — лимфоузлы ворот печени и гепатодуоденальной связки не поражены;
N1 — имеется поражение метастазами лимфоузлов ворот печени или гепатодуоденальной связки (при патологоанатомическом исследовании материала лимфаденэктомии (pN) должно быть исследовано не менее 3 лимфоузлов).
Критерий М:
Мо— нет данных за наличие отдаленных метастазов;
М1— наличие отдаленных метастазов.
Слайд 18
СКРИНИНГ ПРП
Несовершенен. Основан на определении в крови обследуемых

лиц в группах риска один раз в 4-6 мес
уровня АФП крови и, в случае повышения его концентрации, применении УЗИ печени. Практическая ценность скрининга ПРП в странах, эндемичных по вирусному гепатиту В, невелика, так как гепатоцеллюлярная карцинома там характеризуется чрезвычайно быстрым и агрессивным течением. Кроме того, в большинстве указанных стран проведение данного скрининга экономически невозможно. Напротив, в странах не эндемичных по вирусному гепатиту В, указанный скрининг ПРП может привести к доклиническому выявлению незапущенных форм рака печени, чему способствует возможность бесплатного определения АФП и выполнения УЗИ в группе риска.
АФП — гликопротеид, у большинства больных ПРП с опухолью больше 3 см концентрация маркера в сыворотке крови выше 20 нг/мл (20 мкг/л). Концентрация маркера прямо пропорциональна массе опухоли. Данный иммунохимический маркер имеет диагностическое значение при гепатоцеллюлярном, гепатохолангиоцеллюлярном раке и гепатобластоме. Холангиокарцинома, цистаденокарцинома, недифференцированный рак печени не сопровождаются повышением концентрации АФП в сыворотке крови. Специфичность теста ограничена ввиду повышения концентрации маркера у беременных женщин, у детей 1-го года жизни практически при любом заболевании, у больных гепатитом и циррозом печени, эмбриональными, герминогенными опухолями; редко — раком легкого, поджелудочной железы, толстой кишки.
Слайд 19
ГРУППЫ РИСКА ПРП
В странах, эндемичных по вирусному гепатиту

В, группа риска включает лиц мужского пола старше 40
лет — носителей поверхностного антигена (HBsAg) вирусного гепатита-В. В странах с низким и средним уровнем заболеваемости группа риска состоит из больных хроническими заболеваниями печени, включая лиц, положительных анти-HCV.
Определение АФП пригодно для скрининга гепатоцеллюлярной карциномы в указанных группах риска, особенно на фоне постоянно возрастающей активности ферментов — ЩФ, гамма-ГТ, ACT, АЛТ.
Дополнительные (кроме АФП) маркеры, ассоциированные с первичным раком печени, используемые в диагностике заболевания и в его мониторинге: дес-гамма-карбоксипротромбин, РЭА, карбогидрагный антиген 19-9 (СА 19-9).
Дес-гамма-карбоксипротромбин (дес-гамма-КПТ) — витамин К-зависимый предшественник протромбина, синтезируемый нормальными гепатоцитами и клетками гепатоцеллюлярного рака. Повышение уровня этого фактора до 100 нг/мл и более свидетельствует о возможном гепатоцеллюлярном раке. Специфичность этого показателя выше, чем АФП, но чувствительность недостаточна при диагностике опухолей небольшого размера.
РЭА и СА 19—9 имеют большее значение в диагностике и мониторировании больных холангиоцеллюлярным раком, а также в выявлении больных метастатическим раком печени.

Ультразвуковое исследование
Достоинства УЗИ в гепатологии:
а) возможность дифференцировать солидные образования и жидкостьсодержащие кисты, гемангиомы и злокачественные опухоли;
б) выявление в опухоли зоны некроза.
Метод высокоинформативен в определении пораженной доли и сегментов печени, позволяет судить о состоянии ворот печени, инвазии опухоли в прилежащие к печени органы. Легко выявляются увеличенные лимфоузлы в гепатодуоденальной связке, панкреатодуоденальной зоне, асцит.
Опухоль, отличающаяся по эхогенности от паренхимы печени дифференцируется при УЗИ на современных аппаратах, начиная с размеров 2-3 мм.
Изоэхогенные с печенью образования дифференцируются по косвенным признакам при размерах не менее 1 см.
Комбинирование с тонкоигольной пункционной биопсией (ПБ) позволяет достоверно судить о морфологическом строении опухоли в печени.
Интраоперационное УЗИ позволяет выявить внутрипеченочные непальпируемые метастазы рака печени и опухолевые тромбы, идентифицировать опухолевые узлы менее 1 см при циррозе печени, уточнить внутрипеченочную сосудистую архитектуру.

Рентгеновская
Компьютерная Томография (РКТ)
Является информативным методом в диагностике опухолей печени. Исследование следует проводить с контрастированием и без него (нативная РКТ). Чаще всего узлы гепатоцеллюлярной карциномы выглядят в виде очагов пониженной плотности. При холангиоцеллюлярном раке РКТ выявляет образование с низким коэффициентом поглощения. С помощью метода внутривенного "усиления" РКТ позволяет дифференцировать первичный рак печени от гемангиом, узлов регенераторной гиперплазии, метастазов опухолей внепеченочных локализаций. Виды РКТ:
Стандартная - метод информативен в топической диагностике опухолей печени — точно указываются пораженные сегменты печени. Тем не менее в диагностике первичных злокачественных опухолей печени нечасто дополняет квалифицированно проведенное УЗИ.
РКТ со спиральным сканированием - лучше визуализируются гиперваскулярные опухоли печени, к которым относится гепатоцеллюлярная карцинома, гепатобластома, ангиосаркома . Визуализируются и сосуды печени.
Спиральная динамическая РКТ с контрастированием - используется сразу при затруднениях в выявлении тромбоза воротной вены и ее ветвей, печеночных вен при ПРП с помощью УЗИ.
Компьютерно-томографическая ангиография - основана на выполнении РКТ с введением рентгеноконтрастного препарата в артериальные сосуды изучаемого органа или региона.
Магнитно-резонансная томография (МРТ)
МРТ в диагностике первичных
злокачественных опухолей печени и внутрипеченочных желчных протоков включает:
динамическую МРТ с внутривенным контрастированием;
бесконтрастную магнитно-резонансную ангиографию (МРА);
МРА с внутривенным контрастированием;
трехмерные изображения.
Все это при отсутствии артефактов и возможности получения изображений в любой плоскости (мультипланарность) позволяет говорить о МРТ как "всеобъемлющем" методе визуализации второй очереди, т.е. методе исследования, выполняемом после УЗИ и вместо РКТ.
Томография с меченными 99mTc эритроцитами
Необходимость в однофазной эмиссионной компьютерной томографии с меченными 99mTc эритроцитами возникает при дифференциальной диагностике между образованием сосудистой природы и хорошо кровоснабжаемой опухолью несосудистого происхождения.
ПЭТ (позитронная эмиссионная
томография)
Диагностические возможности метода в гепатологии активно изучаются. Считается, что ПЭТ — высокоинформативный метод дифференциальной диагностики образований печени опухолевой и неопухолевой природы, определения распространенности злокачественных опухолей. Предполагается высокая чувствительность и специфичность метода.
ПБ (пункционная биопсия) с визуализацией
ПБ — метод морфологической диагностики опухолей печени. Осуществляется под контролем УЗИ, РКТ, лапароскопии. Может выполняться неоднократно, в т.ч. в амбулаторных условиях. Осложнениями практически не сопровождается.
Слайд 24
ДИАГНОСТИКА ПРП
Цитологическое исследование материала, полученного путем тонкоигольной аспирационной
пункции
При высокодифференцированном гепатоцеллюлярном раке можно не подтвердить диагноз, поскольку
цитоморфологические признаки умеренной и выраженной дисплазии гепатоцитов, полученных из узла регенераторной гиперплазии, и клеток высокодифференцированной гепатоцеллюлярной карциномы схожи.
Ангиография (АГ)
АГ — рентгенологическое исследование сосудов печени, высокоинформативное в установлении природы, характера опухоли печени, распространенности процесса внутри и вне печени. Метод позволяет довольно точно предположить гистогенез высококровоснабжаемых опухолей печени.
Слайд 25
Методы оценки функционального состояния печени
Исследование

функции печени необходимо для диагностики заболеваний и оценки тяжести
поражения печени, для определения прогноза болезни и возможности компенсации функций печени в период лечения и после него, в т.ч. после резекций печени и трансплантации органа, для осуществления контроля за эффективностью лечения.
Основные биохимические показатели крови
Билирубин. Повышение уровня билирубина в сыворотке подтверждает наличие желтухи.
Определение сывороточных ферментов
Щелочная фосфатаза (ЩФ). Повышается при холестазе и в меньшей степени при первичном повреждении гепатоцитов.
Гамма - глутамилтранспептидаза (гамма-ГГ). Активность возрастает при холестатическом и паренхиматозном поражении печени. При холестазе гамма-ГТ повышается параллельно с щелочной фосфатазой. При метастатическом поражении печени гамма-ГТ повышается чаще, чем щелочная фосфатаза.
Трансаминазы
Аспартатаминотрансфераза ( митохондриальный фермент) (AcAT). Активность АсАТ повышается при любом остром повреждении паренхимы печени и других тканей и органов (скелетная мускулатура, миокард, почки).
Аланинаминотрансфераза ( цитоплазматиеский фермент ) (АлАТ). Поскольку Ал AT в гепатоцитах значительно больше, чем в клетках других органов, его повышение более специфично для заболеваний печени.
Лактатдегидрогеназа (ЛДГ). Малочувствительный показатель поражения печени. Значительное повышение активности ЛДГ отмечается при опухолевом поражении печени.
Слайд 26
Методы оценки функционального состояния печени

Другие показатели
Альбумин (37—52 г/л). Снижение концентрации может свидетельствовать о снижении белковосинтети ческой функции печени.
Фибриноген (2—6 г/л). Концентрация возрастает при остром поражении печени. При хронических заболеваниях печени различной этиологии концентрация в крови снижается.
Протромбиновое время (11-15с). Возрастает при диффузных поражениях печени различной этиологии.
Альфа2-глобулиин(6—10 г/л), бета-глобулин (7-11 г/л), гамма-глобулин (8-16 г л). Концентрация возрастает при различных поражениях печени, в т.ч. холестазе. Кореллируют с липопротеинами крови.
Мочевина (2,5—7,5 ммоль /л). Снижение концентрации свидетельствует об угнетении образования мочевины в гепатоцитах из аминокислот.
Аминокислоты. Концентрация возрастает при всех заболеваниях печени, особенно характерно повышение концентрации метионина (>40 мкмоль/л), фенилаланина (>109 мкмоль/л), тирозина (>72 мкмоль /л).
Желчные кислоты (суммарно-2,5-6,8 мкмоль/л). Концентрация возрастает после приема пищи при различных поражениях печени. Высокочувствительный метод подтверждает поражение печени, позволяет оценить ее выделительную функцию и наличие портосистемного шунтирования крови.
Глюкоза (3,8-5,8 ммоль/л). При фульминантном некрозе печени содержание глюкозы снижается. При хронических диффузных заболеваниях печени нарушается толерантность к глюкозе.
Галактоза (2,2—3,3 ммоль/л). При хронических диффузных заболеваниях печени концентрация возрастает.
Слайд 27
Методы оценки функционального состояния печени

Иммунохимические тесты сыворотки крови
АФП (<10 мкг|л). Повышение в крови может свидетельствовать о гепатоцеллюлярном раке, хроническом гепатите и циррозе печени.
Иммуноглобулины классов G, М, А. Концентрация повышается из-за угнетения секвестрации антигенов в звездчатых клетках печени и нарушения катаболизма иммунных комплексов в печени. Уровень существенно возрастает при гепатитах и циррозах разной этиологии.
Количественное исследование функции печени. Функциональные печеночные пробы
Практически значимыми являются две функциональные печеночные пробы.
Проба с индоцианином зеленым. Клиренс индоцианина зеленого менее 0,4 мг/кг/мин даже после экономных резекций печени ассоциируется с достоверно более высокой частотой острой печеночной недостаточности в послеоперационном периоде. Для больных, которым планируются обширные резекции печени, этот показатель должен быть не менее 1,0 мг/кг/мин.
Исследование поглотительно-выделительной функции печени с помощью меченного радиоактивным технецием Brom Mesida. Функциональное состояние печени оценивается в цифровом выражении. Каждому цифровому уровню соответствует процент сохраненного функционального резерва печени.
Слайд 28
Методы оценки функционального состояния печени
Оценка печёночноклеточной функции при
циррозе по Child-Pugh (1973) подразумевает три класса: A, B,
C, определяемое по числу баллов.
Класс А – 5-6 баллов; класс В – 7-9 баллов; класс С – 10 и более баллов.
Слайд 29
Методы оценки функционального состояния печени
Функциональные тесты при ПРП
столь существенны, что преимущественно на их основе разработана классификация
гепатоцеллюлярного рака (Okuda К. et al., 1984). Рассматриваемые в классификации признаки: асцит, объем опухоли более 50% печени, альбумин сыворотки крови меньше 30 г/л, общий билирубин сыворотки крови больше 30 мкмоль/л.
Классификация гепатоцеллюлярного рака по К. Okuda:
I стадия — указанные признаки отсутствуют;
II стадия — не более 2 признаков;
III стадия - имеются все 4 признака.
Абсолютно точных функциональных тестов переносимости резекции печени нет. В практике является достаточным сочетание:
1) базовые биохимические показатели + система критериев Child-Pugh;
2) базовые биохимические показатели + один из методов количественной оценки функции печени (например, проба с индоцианином зеленым).
Слайд 30
ЛЕЧЕНИЕ ПРП
I. Хирургическое лечение:
резекция печени;
гепатэктомия с ортотопической алло(ауто-)трансплантацией печени.
II. Локальное
аблативное и циторедуктивное лечение:
радиочастотная термодеструкция опухоли;
криодеструкция опухоли;
микроволновая фокусная деструкция
опухоли;
ультразвуковая фокусная деструкция опухоли;
лазерная фокусная деструкция опухоли;
деструкция опухоли печени путем введения в опухоль этанола,
уксусной кислоты, цитостатиков, радиоактивных изотопов;
другие виды локального циторедуктивного лечения;
сочетанное локальное циторедуктивное лечение.
Слайд 31
ЛЕЧЕНИЕ ПРП
III. Внутрисосудистое чрескатетерное (рентгеноэндоваскулярное) лечение:
эмболизация печеночной артерии (ЭПА);
химиоэмболизация
печеночной артерии (ХЭПА);
масляная химиоэмболизация печеночной артерии (МХЭПА);
артерио-портальная химиоэмболизация;
химиоинфузия в
печеночную артерию;
химиотерапия в воротную вену;
регионарная радиотерапия;
сочетанное внутрисосудистое чрескатетерное лечение.
IV. Системное лекарственное лечение:
цитостатическая химиотерапия;
иммунотерапия;
гормональное лечение;
биотерапия (генная терапия, противоопухолевая вакцинотерапия);
сочетанное лекарственное лечение.
Слайд 32
ЛЕЧЕНИЕ ПРП
V. Комбинированное лечение:
резекция печени с внутрисосудистым чрескатетерным лечением;
резекция
печени с локальным аблативным и циторедуктивным лечением;
резекция печени с
системным лекарственным лечением;
резекция печени с внутрисосудистым чрескатетерным и системным противоопухолевым лечением;
локальное циторедуктивное лечение с внутрисосудистым чрезкатетерным лечением;
локальное циторедуктивное лечение с чрескатетерным и системным противоопухолевым лекарственным лечением;
другие виды комбинированного лечения.
Слайд 33
Хирургическое лечение больных злокачественными опухолями печени

Хирургический доступ
Резекции и трансплантация печени могут быть выполнены любым из двух абдоминальных доступов: срединного (срединная лапоротомия) и двухподреберного. Трансдиафрагмалъная торакотомия может потребоваться только при резекции вовлеченной в опухоль печени диафрагмы.
Резекция печени
Все резекции печени по методу (принципу) выполнения подразделяются на 2 группы.
1) Типичные (анатомические) резекции, которые определяются
удалением части печеночной паренхимы, производимым по анатомическим
щелям в соответствии с топографией более или менее крупных
судов и протоков внутри печени. Это - сегментэктомии, лобэктомии,
гемигепатэктомии (гепатэктомии) (в соответствии с портальной классификацией сегментов печени по Couinaud С., 1957);
2) Атипичные резекции печени, которые состоят из удаления части паренхимы печени без учета анатомических щелей.
Анатомический метод резекции печени по поводу опухолей наиболее полно отвечает требованиям онкологического радикализма и функциональности операции. Поэтому радикальной будет та oneрация при которой удаляется пораженная опухолью анатомическая часть органа.
Слайд 34
Хирургическое лечение больных злокачественными опухолями печени
Гепатэктомия и ортотопическая
трансплантация печени представлена тремя видами:
гепатэктомия и ортотопическая трансплантация трупной
печени
или ее части;
гепатэктомия и ортотопическая трансплантация части печени от
живого родственного донора
гепатэктомия и ортотопическая аутотрансплантация печени (применяется также по поводу метастатических опухолей печени).
Выбор метода хирургического лечения определяется следующими параметрами:
на ортотопическую трансплантацию печени отбираются больные,
имеющие маленькую опухоль, но с выраженной печеночной недостаточностью;
на резекцию печени - больные, имеющие большую резектабельную опухоль, но с удовлетворительной функцией печени.
В США производится 3-4 тыс. трансплантаций печени в год, из которых только около 100 (2,5-3,3%) операций выполняется по поводу злокачественных опухолей печени.
Слайд 35
Локальное аблативное и циторедуктивное лечение ПРП
Радиочастотная термодеструкция опухоли

печени
В основе методики лежит нагревание опухоли до температуры 80-110
°С с помощью переменного тока (4 МГц) мощностью 50 до 90 Вт, что приводит к коагуляционному некрозу опухоли прилежащей паренхимы печени. Лечение может осуществляться чрескожно, во время лапароскопии, интраооперационно (после лапаротомии). Радиочастотная термодеструкция выполняется при нерезектабельном раке печени, функциональной недостачности печени на фоне цирроза, исключающей резекцию органа, мультифокальном поражении печени. Лечение может комбинироваться с резекцией печени
Криодеструкция ПРП
Гибель клеток при охлаждении до критических температур наступает в силу физико-химических и биохимических несовместимых с жизнью изменений в клетках, в частности, в результате повреждения клеток кристаллами внутриклеточного льда. Криовоздействие осуществляется прямым контактным способом, а также путем наложения криоаппликатора на поверхность
опухоли или внедрения в опухоль криоаппликатора особой кониче
ской формы. Температура криоаппликатора -170 - -190 °С. Время однократного воздействия 10-20 мин.
Слайд 36
Локальное аблативное и циторедуктивное лечение ПРП
Микроволновая и лазерная
фокусная деструкция опухоли печени
Могут осуществляться интраоперационно (после лапаротомии), во
время лапароскопии, пункционно под контролем УЗИ. Применение методик ограничено ввиду очень небольшой зоны некроза опухолевой ткани-мишени, что требует повторного введения микроволнового (при опухоли более 1 см) или лазерного (при опухоли более 2 см) зондов.
Инъекционное введение этанола в опухоль
Лечение основано на алкогольном повреждении мелких артерий, кровоснабжающих опухоль, развитии их тромбоза, что, в свою очередь, обусловливает ишемию и коагуляционный некроз опухолевой ткани. Mетод применяется при инкапсулированных опухолях. Чрескожное иньекционное введение в опухоль печени неразведенного спирта осуществляется иглой калибра 22 G под контролем УЗ И или РКТ дважды в неделю по 5-10 мл. Курс лечения от 3 до 15 процедур.
Слайд 37
Внутрисосудистое чрескатетерное (рентгеноэндоваскулярное) лечение больных ПРП
Эмболизация печеночной артерии

(ЭПА)
Основана на ишемическом повреждении опухоли. Осуществляется под рентгеноскопическим
контролем. В качестве окклюзирующего материала используют рассасывающиеся (аутогемосгустки, разные виды гемостатической губки) и нерассасывающиеся (поливиниловый спирт, металлические спирали, цианокрилатные клеи, разволокнённый велюр, гидрогель, ферромагнитные композиции, этиловый спирт, масляный ренттеноконтрастный препарат (МРП) и др.) эмболизаты.
Химиоэмболизация печеночной артерии (ХЭПА)
Применяется при нерезектабельном печеночноклеточном раке. Процедура призвана вызвать ишемическое повреждение опухоли и создать высокую концентрацию противоопухолевого вещества в опухоли. Из противоопухолевых препаратов используются доксорубицин, митомицин, цисплатин. Лечение может сопровождаться системной химиоммунотерапией с использованием схемы фторурацил + кальция фолинат с одним из рекомбинантных интерферонов альфа—2.
Слайд 38
Внутрисосудистое чрескатетерное (рентгеноэндоваскулярное) лечение больных ПРП
Масляная химиоэмболизация печеночной

артерии (МХЭПА)
Лучший противоопухолевый эффект связан с более длительной
задержкой цитостатика в опухоли. Используются цитостатики: доксорубицин и его аналоги, препараты платины, митомицин.
Артерио-портальная химиоэмболизация
Артериальная эмболизация сопровождается увеличением доли пор
тального кровоснабжения опухоли и активизацией артериопорталь-
ных шунтов в печени.
Химиоинфузия в печеночную apтерию(ХИПА)
При ПРП непрерывная химиоинфузия митоксантрона в дозах 5-8 мг/м2 в сутки в течение 72 ч, несколько курсов, обеспечивает минимальный эффект менее чем у трети больных, но у отдельных пациентов достижима 2-летняя выживаемость. В первый год после начала регионарной монохимиотерапии умирает 71% больных. Внутриартери-альная регионарная полихимиотерапия, включающая фторурацил, цисплатин, доксорубицин сопровождается почти такими же отдаленными результатами: 2-летний период от начала лечения переживают 7,5-12,5% больных.
Слайд 39
Внутрисосудистое чрескатетерное (рентгеноэндоваскулярное) лечение больных ПРП
Внутрипорталъная химиотерапия и
эмболизация воротной вены
Используется как метод химиотерапии нерезектабельных злокачественных опухолей
печени в комбинации с внутриартериальной химиоинфузией или артериальной химиоэмболизацией.
Регионарная радиотерапия (радиоэмболизация)
Возможный метод радиотерапии для больных опухолями печени, поскольку позволяет избирательно воздействовать на опухоль, минимально повреждая паренхиму радиочувствительной печени. Больные легко переносят внутриартериальную радиоэмболизацию микросферами 90Y в дозе от 50 до 150 Гр. Уровень радиации в опухоли в 6 раз выше, чем в нормальной ткани.