Слайд 2
Процесс перехода из жидкого или газообразного
состояния в
твердое, в результате чего образуется
кристаллическая решетка и возникают
кристаллы, называется кристаллизацией.
Слайд 3
Энергетическое состояние системы, имеющей
огромное число охваченных тепловым
движением частиц (атомов, молекул),
характеризуется особой термодинамической
функцией (F
), называемой свободной энергией,
которая определяется:
F= U – TS,
где U – внутренняя энергия системы;
Т - абсолютная температура;
S - энтропия
Можно сказать, что чем больше свободная энергия
системы, тем система менее устойчива, и если
имеется возможность, то система переходит в
состояние, где свободная энергия меньше.
Слайд 4
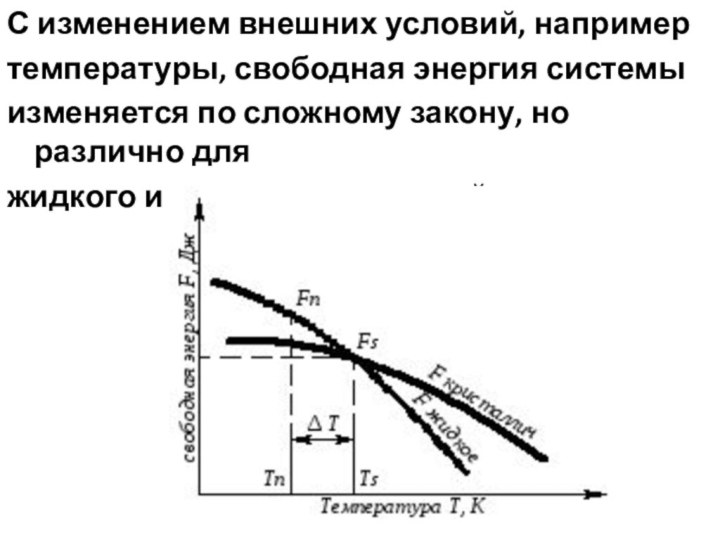
С изменением внешних условий, например
температуры, свободная энергия
системы
изменяется по сложному закону, но различно для
жидкого
и твердого состояний
Слайд 5
Для начала кристаллизации необходимо, чтобы
процесс был термодинамически
выгоден системе и
сопровождался уменьшением свободной энергии
системы. Их
кривых видно, что это возможно только
тогда, когда жидкость будет охлаждена ниже точки Ts.
Температура, при которой практически начинается
кристаллизация, может быть названа фактической
температурой кристаллизации.
Охлаждение жидкости ниже температуры кристаллизации
называется переохлаждением.
Обратное превращение из кристаллического состояния в
жидкое может произойти только выше температуры Ts, это
явление называется перенагреванием.
Слайд 6
Величиной или степенью переохлаждения
называют разность между теоретической
и
фактической температурами кристаллизации
T = Ts - Tф
Процесс перехода
металла из жидкого состояния
в кристаллическое можно изобразить кривыми в
координатах время – температура.
Слайд 8
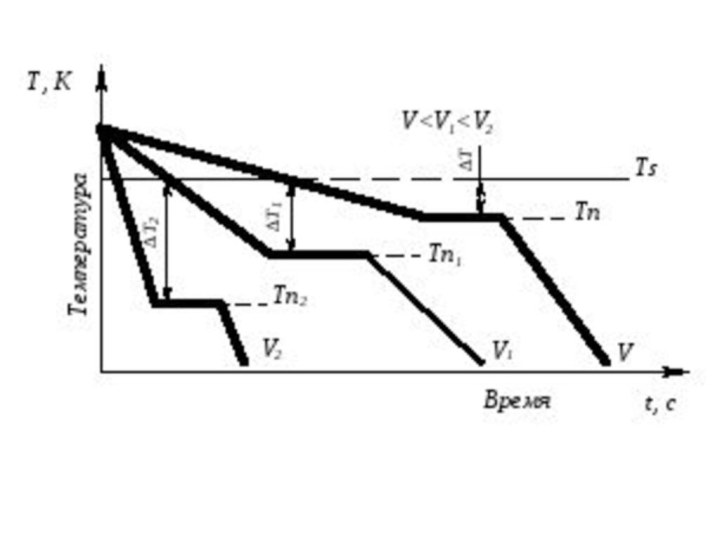
Охлаждение металла в жидком состоянии
сопровождается плавным понижением
температуры и может быть названо простым
охлаждением, так как
при этом нет качественного
изменения состояния. При достижении
температур кристаллизации на кривой
температура – время появляются горизонтальные
площадки, так как отвод тепла
компенсируется выделяющейся при
кристаллизации скрытой теплотой
кристаллизации.
Слайд 9
МЕХАНИЗМ ПРОЦЕССА КРИСТАЛЛИЗАЦИИ
Слайд 10
Процесс кристаллизации состоит из двух
элементарных процессов. Первый
процесс
заключается в зарождении мельчайших частиц
кристаллов, которые называются зародышами
или центрами кристаллизации. Второй процесс
состоит в росте кристаллов из этих центров.
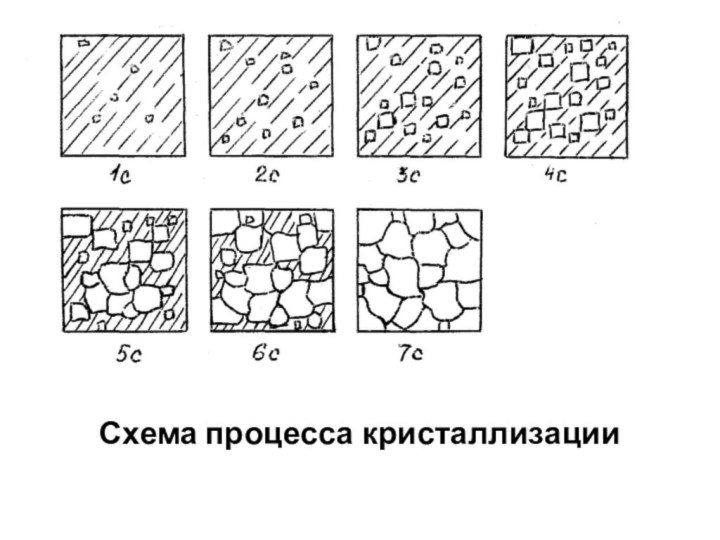
Модель кристаллизации металла в первые 7
секунд охлаждения представлена схемой
процесса кристаллизации и кинетической кривой
кристаллизации
Слайд 12
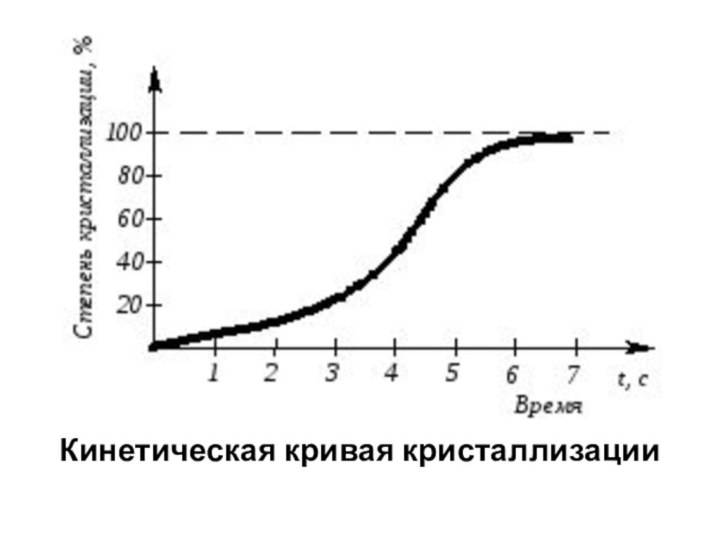
Кинетическая кривая кристаллизации
Слайд 13
По мере развития кристаллизации в нем участвуют
все
большее и большее число кристаллов. Поэтому
процесс вначале ускоряется,
пока в какой-то момент
взаимное столкновение растущих кристаллов
начинает заметно препятствовать их росту. Рост
кристаллов замедляется еще и потому, что
количество жидкости, в которой образуются новые
кристаллы, становится все меньше. В процессе
кристаллизации, пока кристалл окружен жидкостью,
он часто имеет правильную форму, но при
столкновении и срастании кристаллов их правильная
форма нарушается. Внешняя форма кристалла
оказывается зависимой от условий соприкосновения
растущих кристаллов. Вот почему кристаллы металла –
зерна (кристаллиты) не имеют правильной формы.
Слайд 14
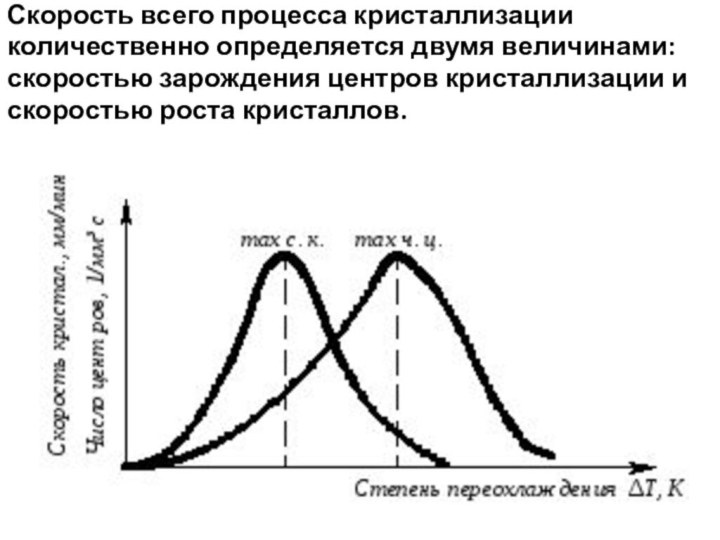
Скорость всего процесса кристаллизации
количественно определяется двумя величинами:
скоростью зарождения центров кристаллизации и
скоростью роста кристаллов.
Слайд 15
Величины оптимального переохлаждения до
достижения максимальной скорости
кристаллизации
(СК) и до образования
максимального числа центров кристаллизации
(ЧЦ)
не совпадают.
Размер образовавшихся кристаллов зависит от
соотношения СК и ЧЦ. При большом значении СК и
малом значении ЧЦ образуется мало крупных
кристаллов. При малых значениях СК и больших ЧЦ
образуется большое число мелких кристаллов.
Минимальный размер способного к росту зародыша
называется критическим размером зародыша.