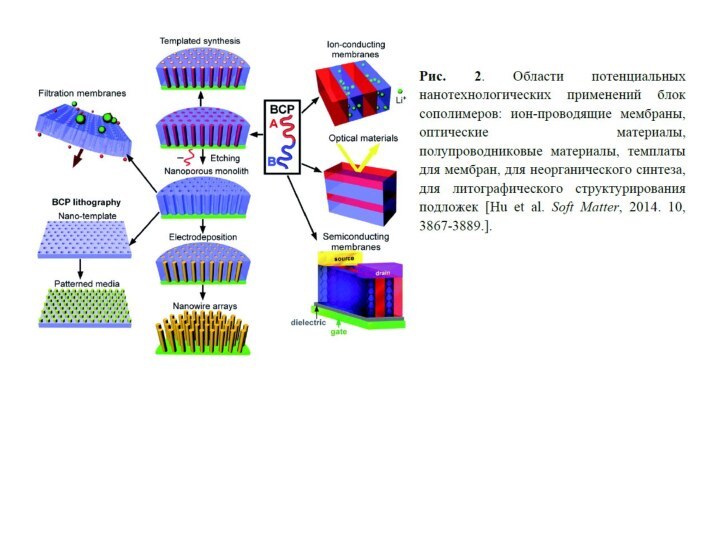
+ n где ф — число фаз (например, агрегатное
состояние), с — число степеней свободы, k — компоненты системы (примеры: H2O, CO2), n — число параметров, определяющих равновесное состояние системы
При переменном давлении (т. е. для жидкостей и газов, т. к. изменение давления на состояние твёрдого тела практически не влияет) правило фаз сводится к выражению:
ф + с = k + 2.
В случае однокомпонентной системы оно упрощается до:
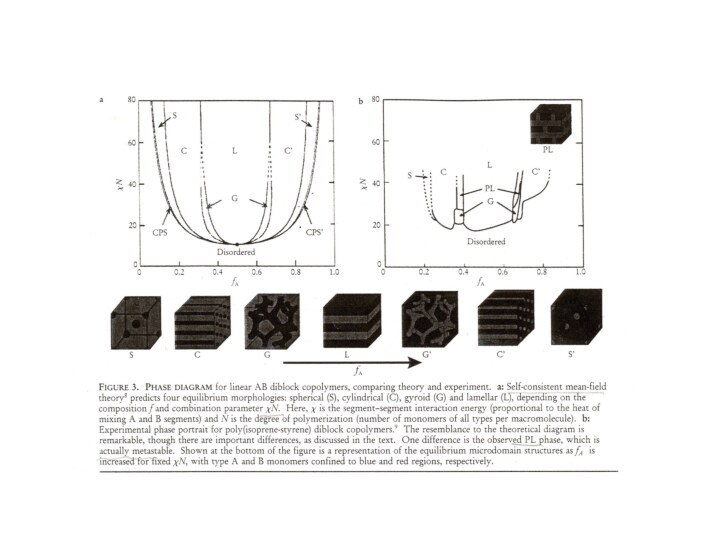
ф + с = 3, что значит, что в однокомпонентной системе при заданном давлении и температуре могут сосуществовать три фазы. На фазовой диаграмме это соответствует тройной точке.
При изменении либо давления, либо температуры могут сосуществовать две фазы и вторая переменная зависима, что соответствует линии. Если фаза одна, то число степеней системы равно двум, и температура и давление могут меняться до тех пор, пока система не окажется на одной из ограничивающих область линий.
Правило фаз Гиббса