кислот
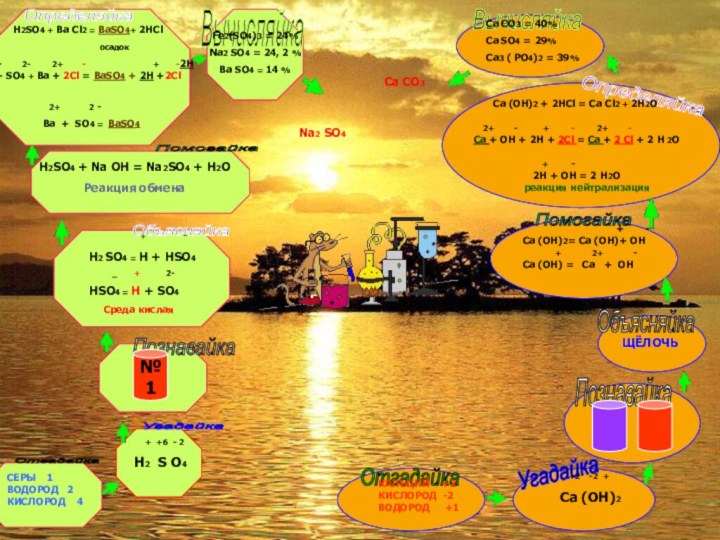
На примере гидроксида кальция – определить общие свойства
основанийПовторить решение задач на определение массовой доли химического элемента в соединении
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть








№1
КАЛЬЦИЙ +2 КИСЛОРОД -2 ВОДОРОД +1
ЩЁЛОЧЬ
Ca (OH)2 + 2HCl = Ca Cl2 + 2H2O
2+ - + - 2+ -
Ca + OH + 2H + 2Cl = Ca + 2 Cl + 2 H 2O
+ -
2H + OH = 2 H2O
реакция нейтрализация
Ca CO3 = 40%
Ca SO4 = 29%
Ca3 ( PO4)2 = 39%
+ -
Ca (OH)2= Ca (OH)+ OH
+ 2+ -
Ca (OH) = Ca + OH
+ -
H2 SO4 = H + HSO4
_ + 2-
HSO4 = H + SO4
Среда кислая
H2SO4 + Na OH = Na2SO4 + H2O
Реакция обмена
H2SO4 + Ba Cl2 = BaSO4+ 2HCl
осадок
+ 2- 2+ - + -2H + SO4 + Ba + 2Cl = BaSO4 + 2H +2Cl
2+ 2 -
Ba + SO4 = BaSO4
Fe2(SO4)3 = 24%
Na2 SO4 = 24, 2 %
Ba SO4 = 14 %
+2 -2 +
Ca (OH)2
Na2 SO4
Ca CO3
Оценочная шкала:
33—35 баллов - «5»
28—33 баллов - «4»
20—28 баллов - «3»
- или знаниями и умениями,
которые вы сегодня приобрели?