Слайд 2
Сроки и место проведения
Сроки ГИА 9-х классов по
химии в 2015 году:
Основной период - 29 мая
(пятница) ,
резерв - 9 июня (вторник) .
ОГЭ по химии выпускники сдают на добровольной основе по своему выбору.
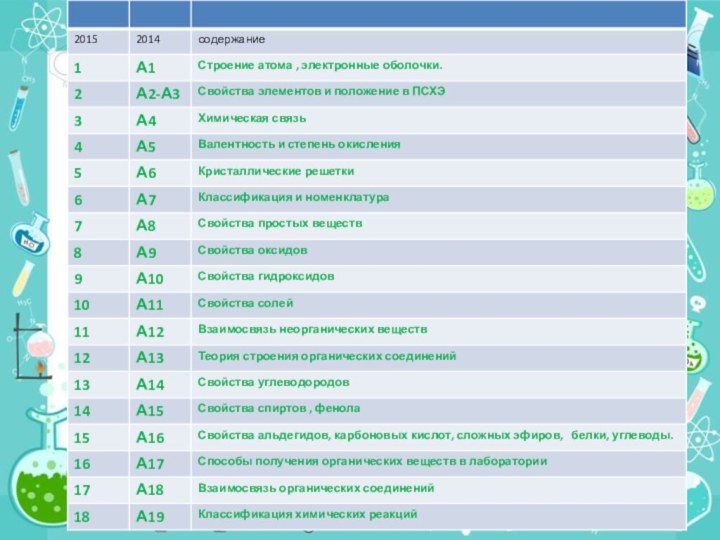
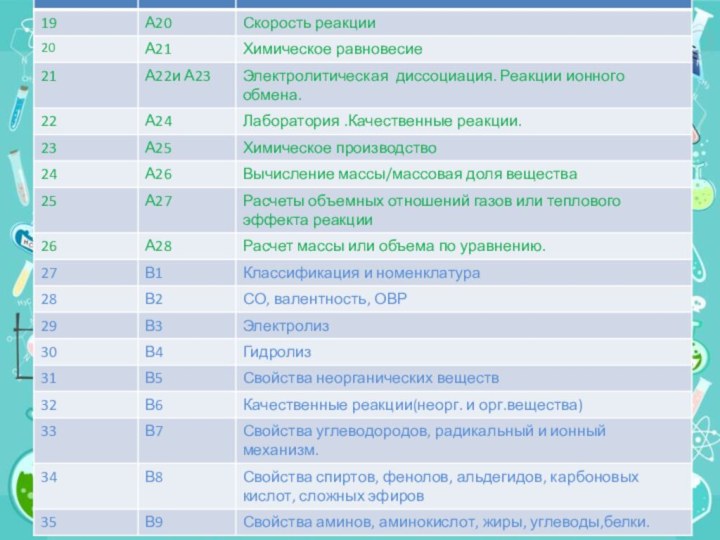
Структура и содержание
КИМ 2015
Согласно КИМ 2015 года в структуру ОГЭ по химии внесены следующие изменения:
1. Изменена структура варианта КИМ: каждый вариант состоит из двух частей (часть 1 – задания с кратким ответом, часть 2 – задания с развернутым ответом).
2. Задания в варианте КИМ представлены в режиме сквозной нумерации без буквенных обозначений А, В, С.
Изменения в содержании КИМ отсутствуют. Как и в 2014 году в проекте демоверсии предложено две модели проведения ОГЭ:
- модель 1 (без реального эксперимента) – 22 задания,
- модель 2 (с реальным экспериментом) – 23 задания.
Слайд 4
Содержание заданий аттестации по химии
Содержание КИМ определяетса
на основе документов:
Обязательный минимум содержания основного общего образования по
химии (Приказ МО РФ № 1236 от 19.05.98 г.).
Федеральный компонент государственных стандартов основного общего и среднего (полного) общего образования по химии (Приказ МО РФ № 1089 от 05.03.2004 г.).
Проверяемые элементы содержания учебного предмета представлены в Кодификаторе контрольно-измерительных материалов ГИА.
Слайд 5
Часть 1 содержит 19 заданий с кратким ответом,
в их числе 15 заданий базового уровня сложности (порядковые
номера этих заданий: 1, 2, 3, 4,…15) и 4 задания повышенного уровня сложности (порядковые номера этих заданий: 16, 17, 18, 19). При всем своем различии задания этой части сходны в том, что ответ к каждому из них записывается кратко в виде одной цифры или последовательности цифр (двух или трех).
Слайд 6
Часть 2 КИМ содержит 3 задания высокого уровня
сложности, с развернутым ответом. Задание 22, предусматривает выполнение «мысленного
эксперимента»;
Задания расположены по принципу постепенного нарастания уровня их сложности.
Доля заданий базового, повышенного и высокого уровней сложности составляет в работе 68, 18 и 14% соответственно.
Слайд 7
Задание 20 предусматривает расстановку коэффициентов в ОВР методом
электронного баланса (аналогично С1 ЕГЭ, на более простых реакциях).
- Задание 21 - расчетная задача .
- Задание 22 - мысленный эксперимент: для заданного набора веществ спланировать синтез нового вещества, написав уравнения реакций, указать признаки их протекания. Написать ионное уравнение одной из реакций.
Слайд 8
Новое
Бланк ответов №1
Изменена форма записи ответа на каждое
из заданий 1–15: в КИМ 2015 г. требуется записывать
цифру, соответствующую номеру правильного ответа.
Слайд 9
Продолжительность ОГЭ по химии
На выполнение экзаменационной работы отводится
120 минут;
Примерное время, отводимое на выполнение отдельных заданий,
составляет:
1)
для каждого задания части 1 – 3–8 минуты;
2) для каждого задания части 2 – 12–17 минут;
Слайд 10
Система оценивания выполнения отдельных заданий и экзаменационной работы

в целом
Верное выполнение каждого из заданий части 1 базового
уровня сложности (1–15) оценивается 1 баллом.
Верное выполненное каждого из заданий части 1 повышенного уровня сложности (16–19) максимально оценивается 2 баллами.
Задания 16 и 17 считаются выполненными верно, если в каждом из них правильно выбраны два варианта ответа. За неполный ответ – правильно назван один из двух ответов или названы три ответа, из которых два верные, – выставляется 1 балл. Остальные варианты ответов считаются неверными и оцениваются 0 баллов.
Задания 18 и 19 считаются выполненными верно, если правильно установлены три соответствия. Частично верным считается ответ, в котором установлены два соответствия из трех; он оценивается 1 баллом. Остальные варианты считаются неверным ответом и оцениваются 0 баллов.
Проверка заданий части 2 (20–23)
Максимальная оценка за верно выполненное задание: за задания 20 и 21 – по 3 балла; за задание 22 – 5 баллов;
Задания с развернутым ответом могут быть выполнены обучающимися разными способами.
Слайд 11
Шкалирование
Максимальный первичный балл за выполнение всех заданий
экзаменационной работы по химии составляет 34 балла. Шкала пересчета
первичного балла в пятибальную оценку:
Первичный балл 0-8 9 - 17 18 - 26 27 - 34
Отметка «2» «3» «4» «5»
Отметку «5» рекомендуется выставлять в том случае, если выпускник набрал достаточное общее число баллов и при этом не менее 5 баллов набрал за выполнение заданий части 2.
Слайд 12
Государственная итоговая аттестация
2015 год
Единый государственный экзамен
Слайд 13
Сроки и место проведения
Сроки ГИА 11-х классов по
химии в 2015 году:
Основной период – 8июня (понедельник)
,
резерв - 24 июня (среда) .
ЕГЭ по химии выпускники сдают на добровольной основе по своему выбору.
Слайд 14
Изменения в КИМ 2015 года по сравнению с
2014 годом
1. Изменена структура варианта КИМ: каждый вариант
состоит из двух
частей и включает в себя 40 заданий (вместо 42 заданий в 2014 г.), различаю-
щихся формой и уровнем сложности. Задания в варианте представлены в ре-
жиме сквозной нумерации.
2. Уменьшено число заданий базового уровня сложности с 28 до 26 заданий. Это сделано за счет объединения близких позиций в заданиях 2 (бывшие А2+А3) и 21 (бывшие А22+А23).
3. Изменена форма записи ответа на каждое из заданий 1–26: в КИМ
2015 г. требуется записывать цифру, соответствующую номеру правильного
ответа.
4. Изменено задание на нахождение формулы вещества (задание 40, бывшее С5). Добавлено требование написать структурную формулу вещества и уравнение реакции для него. Максимальный балл за его выполнение – 4 (вместо 3 баллов в 2014 году)
5. Максимальный балл за выполнение всех заданий экзаменационной работы 2015 г. составляет 64 (вместо 65 баллов в 2014 г.).
Слайд 18
Продолжительность ЕГЭ по химии
3 часа (180 минут).
Примерное время,
отводимое на выполнение отдельных заданий, составляет:
1) для каждого задания
базового уровня сложности части 1 – 2 минуты;
2) для каждого задания повышенного уровня сложности части 1 – 5–7 минут;
3) для каждого задания части 2 – до 10 минут.
Слайд 19
Оценивание
Минимальный первичный балл -14
Минимальный порог -36 баллов
Задания
1-26 оцениваются по 1 баллу.
27- 35
до 2 баллов,
36- до 3 баллов, 37,39, 40 -до 4 баллов, 38- до 5 баллов,.
Слайд 20
ФИПИ
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО НЕКОТОРЫМ АСПЕКТАМ СОВЕРШЕН-
СТВОВАНИЯ ПРЕПОДАВАНИЯ
ХИМИИ
(на основе анализа типичных затруднений выпускников при выполнении
заданий ЕГЭ)
Среди заданий повышенного уровня сложности с кратким ответом, включённых в экзаменационную работу, наибольшие затруднения у экзаменуемых вызвали задания, которые ориентированы на проверку усвоения знаний характерных химических свойств неорганических веществ (В5 -31) и задания, проверяющие усвоение знаний о качественных реакциях на неорганические вещества и ионы, а также знания об идентификации органических веществ (В6-32).
Слайд 21
В5-31 Средний процент выполнения этих заданий составляет 34%.
Задание:

Установите соответствие между формулой вещества и реагентами, с каждым
из которых это вещество может взаимодействовать.
ФОРМУЛА ВЕЩЕСТВА РЕАГЕНТЫ
А) O2
Б) CO2
В) Zn(OH)2
Г) KI
1) C, ZnS, FeO
2) HCl, Na2O, NaOH
3) Br2, AgNO3, (CH3COO)2Pb
4) Mg, NaOH, CaO
5) S, Na3PO4, HCl
Для вещества кислород (А) надо выбрать реагенты, указанные под цифрой 1. При этом экзаменуемые должны знать, что кислород способен окислять сульфид цинка и оксид железа(II).
Выбирая реагенты для оксида углерода(IV) (Б) необходимо помнить о его способности реагировать не только с веществами, проявляющими основные свойства (NaOH, CaO), но и с магнием (ответ 4).
Для гидроксида цинка (В) характерны амфотерные свойства – ответ 2.
Иодид калия (Г) способен вступать в реакции ионного обмена (с AgNO3, (CH3COO)2Pb), а также проявлять свойства восстановителя в реакции с Br2 (ответ 3).
Таким образом, выполнение таких заданий требует применения знаний не только об общих свойствах вещества как представителя определённого класса веществ, но и специфических свойств конкретного неорганического
вещества.
Слайд 22
В6-32 Средний процент выполнения этих заданий составляет 30%.
Задание:

Установите соответствие между формулами двух веществ и признаком реакции,
протекающей между этими веществами.
ФОРМУЛЫ ВЕЩЕСТВ
А) СН2(ОН)–СН(ОН)–СН2(ОН) и Cu(OH)2
Б)CH3CH=CHCH3 и КMnO4 (Н+)
В)СH3CHO и Cu(OH)2
Г)СH2=СНCOОH и Br2
ПРИЗНАК РЕАКЦИИ
1)обесцвечивание раствора
2)растворение осадка с образованием синего раствора
3)образование белого осадка
4)выделение газа
5)образование кирпично-красного осадка
На основании структурной формулы органического вещества А необходимо сделать вывод о том, что это вещество является многоатомным спиртом. В результате реакции многоатомного спирта с гидроксидом меди(II) осадок гидроксида меди(II) растворяется, при этом образовавшийся раствор приобретает синее окрашивание (ответ 2).
В молекуле органического вещества Б присутствует двойная связь. Такие вещества способны окисляться перманганатом калия (в кислой среде), при этом будет наблюдаться обесцвечивание раствора перманганата калия (ответ 1).
Как видно из структурной формулы, в молекуле вещества В присутствует альдегидная группа, способная окисляться под действием гидроксида меди(II). Признаком реакции является образование кирпично-красного осадка (ответ 5).
Структурная формула органического вещества Г показывает наличие в его молекуле, как двойной
связи, так и карбоксильной группы. Реакция присоединения брома будет проходить с разрывом двойной связи, и сопровождаться обесцвечиванием раствора (ответ 1).
Слайд 23
Выполнение этих заданий В6-32 требует сформированности знаний о
качественных реагентах, используемых для определения конкретных неорганических и органических
веществ, знаний признаков протекания качественных реакций, умения различить вещества на основании различия в их химических свойствах.
Слайд 24
Задания С1 ориентированы на проверку умений определять степень
окисления
химических элементов, определять окислитель и восстановитель,
составлять электронный баланс, на
его основе расставлять коэффициенты в
уравнениях реакций.
Как показывают статистические данные, к выполнению этих заданий приступают более 85% экзаменуемых. Но успешно выполняют задание выпускники с хорошим (82%) и наиболее высоким (97%) уровнями подготовки
Рассмотрим на конкретных примерах наиболее распространенные ошибки экзаменуемых при выполнении этих заданий.
Задание: Используя метод электронного баланса, составьте уравнение реакции
KNO2 + … + H2SO4 → I2 + NO + … + …
Определите окислитель и восстановитель.
Слайд 25
В ответе выпускника правильно определены степени окисления азота
и йода, а также характер изменения степеней окисления. Правильно
составлен электронный баланс – количество отданных и принятых электронов. Формулы веществ, пропущенные в схеме реакции, тоже записаны правильно, расставлены коэффициенты в уравнении. Но при указании окислителя и восстановителя допущены ошибки. Надо было указать, что йод в степени окисления –1 является восстановителем, а азот в степени окисления +3 (или нитрит калия за счет азота в степени окисления +3) -окислителем.
Во втором неверно указан о.в.
Слайд 26
Задание: Используя метод электронного баланса, составьте уравнение реакции:
NH3+KMnO4+…→…+K2MnO4+H2O
Определите

окислитель и восстановитель.
При выполнении этого задания, некоторые экзаменуемые допустили
ошибку в определении формулы вещества, пропущенного в правой части уравнения. Они ошибочно указали нитрат калия как продукт окисления аммиака, в то время как к правильному определению формулы продукта окисления должны были привести следующие рассуждения. Продуктом восстановления KMnO4 является K2MnO4, который существует только в щелочной среде. Значит, в левую часть уравнения нужно было вписать формулу щелочи KOH, а также учесть при этом, что перманганат калия в щелочной среде проявляет более слабые окислительные свойства, чем в кислой. Поэтому азот в степени окисления –3 в составе аммиака способен изменить степень окисления лишь до +2, но не до высшей степени окисления +5, как в нитрате калия. Теперь можно составить формулу вещества, содержащего азот в степени окисления +2, скорее всего это будет NO. А далее с помощью электронного баланса – установить необходимые коэффициенты и составить уравнение реакции: 2NH3 + 6KMnO4 + 6KOH = N2 + 6K2MnO4 + 6H2O.
Слайд 27
С2 С2
В условии задания С2, проверяющего знание
генетической связи раз-
личных классов неорганических веществ, предложено описание конкретного
химического
эксперимента, ход которого экзаменуемые должны были про-
иллюстрировать посредством уравнений соответствующих химических реак-
ций.
Задание: Газ, полученный при обработке нитрида кальция водой, пропустили над раскаленным порошком оксида меди(II). Полученное при этом твердое вещество растворили в концентрированной азотной кислоте, раствор выпарили, а полученный твердый остаток прокалили. Составьте уравнения четырех описанных реакций.
Слайд 28
В этом случае ошибка допущена в четвертом уравнении
реакции. В результате разложения нитрата меди(II) образуется оксид меди(II),
диоксид азота и кислород. Как видно, в ответе среди продуктов реакции ошибочно указана медь.
Второй случай вместо нитрида кальция записан нитрид калия. Во втором уравнении допущена ошибка в записи формулы продукта реакции: вместо азота указан оксид азота(II). Можно предположить, что причиной допущенной ошибки является неумение прогнозировать продукт реакции с учетом характера изменения степени окисления элемента в зависимости от условий реакции. В четвертом уравнении неверно расставлены коэффициенты.
Слайд 29
Задание С3
Выполнение этих заданий требует от выпускников целого
комплекса знаний по органической химии: глубокого понимания генетической взаимосвязи
органических веществ, знания их химических свойств и способов получения, умения учитывать условия проведения реакций, анализировать строение органических веществ.
Рассмотрим примеры ответов выпускников и отметим допущенные ими ошибки.
Задание: Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: При написании уравнений реакций используйте структурные формулы
органических веществ.
Слайд 30
Обратим внимание на то, что экзаменуемый не выполнил
требование
записи структурных формул органических веществ. Во втором уравнении
пропущен один
из продуктов реакции – вода. Пятое уравнение реакции не составлено.
Слайд 31
В этом ответе записаны структурные формулы веществ. Однако
в третьем уравнении отсутствует коэффициент 3 перед формулой ацетилена
(С2Н2). Вместе с тем по второму и пятому уравнениям реакций можно судить о том, что умение расставлять коэффициенты у экзаменуемого сформировано достаточно прочно. На этом основании можно высказать предположение о том, что ошибка в третьем уравнении допущена по невнимательности.
Слайд 32
В данном ответе не расставлены коэффициенты в пятом
уравнении реакции. Такую запись принято называть схемой реакции, но
в условии задания требовалось составить уравнение реакций. Подобная ошибка приводит к потере 1 балла за выполнение задания
Слайд 33
Задание С4
Задания С4 – это расчетные задачи. Их

выполнение требует знания хи-
мических свойств веществ и предполагает осуществление
некоторой сово-
купности действий, обеспечивающих получение правильного ответа.
Задание: Смешали 100 мл 30%-ного раствора хлорной кислоты (ρ = 1,11 г/мл) и 300 мл 20%-
ного раствора гидроксида натрия (ρ = 1,10 г/мл). Сколько миллилитров воды следует добавить к по- лученной смеси, чтобы массовая доля перхлората натрия в ней составила бы 8%?
Отметим следующие необходимые этапы рассуждений при выполнении этого задания:
1) химическую сущность условия задания описывает уравнение реакции:
HСlO4 + NaOH = NaClO4 + H2O
2) используя данные задачи, рассчитаем количество вещества каждого из реагентов, чтобы сделать вывод об избытке одного из веществ: n(NaOH) = 300 · 1,1 · 0,2/40 = 1,65 моль – в избытке
n(HСlO4) = 100 · 1,11 · 0,3/100,5 ≈ 0,33 моль
3) на основании предыдущего вывода вычислим массу соли:
n(NaClO4) = n(HСlO4) = 0,33 моль
m(NaClO4) = 0,33 · 122,5 ≈ 40,4 г
4) далее вычислим объем добавленной воды:
40,4
0,08 = ________________
100х 1,11 +300 х1,1+ x
откуда х = 64 г
V(H2O) = 64 мл
Ответ: объем добавленной воды – 64 мл
Слайд 34
Рассмотрим пример ответа экзаменуемых и проанализируем допу-
щенные ошибки.
Из
ответа экзаменуемого видно, что ошибка, как и в предыдущем
случае, допущена на заключительном этапе решения задачи. Но здесь, скорее всего, просматривается неумение использовать понятие «массовая доля вещества в растворе».
Слайд 35
Анализируя далее ответ экзаменуемого, отметим еще одну часто
встречающуюся ошибку. Получив формальный ответ (0,4752 мл), выпускник даже
не задумывается над тем, насколько полученная величина соотносится с данными условия задачи, – это всего несколько капель воды. Вряд ли такой объем добавленной воды сможет уменьшить концентрацию исходных растворов.
Такой формальный подход к значениям величин, которые ис пользуются при решении химических задач, говорит об отсутствии метапредметных навыков, необходимых для решения задач различного типа, а также навыков самоконтроля и самопроверки.
Заметим также, что выпускники зачастую совершают ошибки в расчетах на втором или третьем этапе решения задачи. Очевидно, что такие ошибки приводят к неправильному ответу. Однако они не свидетельствуют о несформированности умения решать химическую задачу.
Слайд 36
С5
Задание С5 предусматривают определение молекулярной формулы вещества. Выполнение
этого задания включает в себя три последовательных
операции: составление схемы
химической реакции; определение стехиометрических соотношений реагирующих веществ; вычисления на их основе,
приводящие к установлению состава неизвестного вещества.
Слайд 37
Задание:
Cложный эфир массой 30 г подвергнут щелочному
гидролизу. При этом получено
34 г натриевой соли предельной одноосновной
кислоты и 16 г спирта. Установите
молекулярную формулу этого эфира.
В процессе решения данной задачи надо было осуществить следующие
последовательные действия:
1) составить уравнение гидролиза эфира в общем виде:
RCOOR’ + NaOH → RCOONa + R’OH
2) вычислить количество вещества едкого натра:
m(NaOH) = (34 + 16) – 30 = 20 г
n(NaOH) = 20 / 40 = 0,5 моль
3) определить молярную массу эфира и его молекулярную формулу:
из уравнения следует, что n(RCOOR’) = n(NaOH) = 0,5 моль, тогда
m(RCOOR’) = m / n = 30/0,5 = 60 г/моль
m(R1 + R2) = 60 – 12 – 32 = 16 г/моль
следовательно, ими могут быть только атом Н и метил СН3
формула эфира: НСООСН3
Слайд 38
Первые два элемента ответа, представленные экзаменуемым, являются верными.
Последний элемент ответа логически не завершен. Однако экзаменуемый получил
верный ответ на задание практически методом подбора.