- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Карбонаты и силикаты
Содержание
- 2. Угольная кислотаСуществует в растворах;Является слабым электролитом;Неустойчива, легко разлагается.СО2 + Н2О → Н2О
- 3. Кремниевая кислотаH2SiO3 – твёрдое вещество, в воде не растворимое; разлагается при нагревании.H2SiO3 = SiO2 + H2O
- 4. Получение кремниевой кислоты.
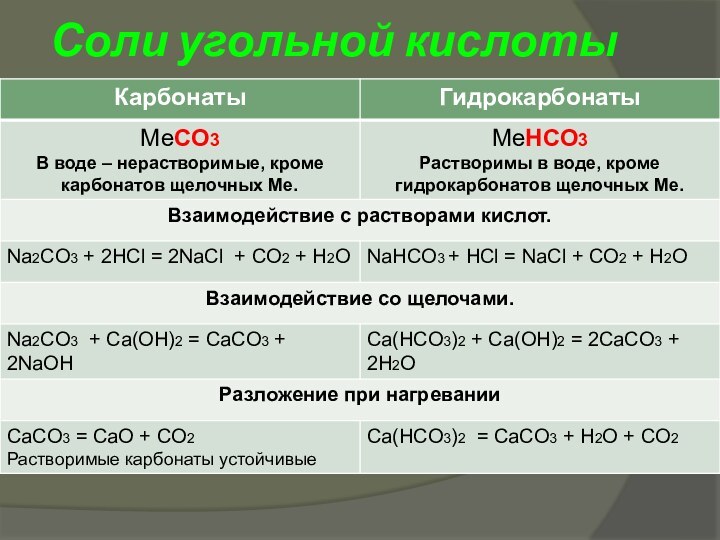
- 5. Соли угольной кислоты
- 6. Термическое разложение карбонатовА как относятся к нагреванию силикаты?
- 7. Разложение гидрокарбонатов
- 8. Образование карбонатов и гидрокарбонатов
- 9. Исследование.Выполните лабораторный опыт 35 на стр.201 учебника
- 10. Образование карбонатов и гидрокарбонатовСа(ОН)2 + СО2 =СаСО3
- 11. Скачать презентацию
- 12. Похожие презентации
Угольная кислотаСуществует в растворах;Является слабым электролитом;Неустойчива, легко разлагается.СО2 + Н2О → Н2О