бы не металлы, человек влачил бы самую жалкую жизнь
среди диких зверей»Г. Агрикола
XVI век.
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть















Каменный топор первобытного человека содержал алюминий. Дома из кирпича содержат алюминий. Любуясь драгоценными камнями - синим сапфиром, красным рубином - многие не догадываются,что это просто алюминий с кислородом.
Узнали об этом металле в 1825 г. Первоначально он ценился выше золота и применялся для изготовления ювелирных изделий. Члены царской семьи были удостоены чести пользоваться алюминиевыми вилками и ложками на банкете, устроенном императором Франции Наполеоном III.
Сегодня его называют «крылатым металлом».
Царь-Пу́шка — отлита из бронзы — отлита из бронзы в 1586 году — отлита из бронзы в 1586 году русским мастером Андреем Чоховым — отлита из бронзы в 1586 году русским мастером Андреем Чоховым на Пушечном дворе — отлита из бронзы в 1586 году русским мастером Андреем Чоховым на Пушечном дворе во времена правления царя — отлита из бронзы в 1586 году русским мастером Андреем Чоховым на Пушечном дворе во времена правления царя Фёдора Ивановича. Масса 40 тонн, длина 5.3 метра, калибр 89 см. В боях пушка не участвовала и осталась памятником высокого мастерства русских оружейников на территории Московского Кремля.
натрий
калий
II этап урока: Проверка усвоения пройденного материала
НОМЕР ГУППЫ
НОМЕР ПЕРИОДА
СЕМЕЙСТВО d-ЭЛЕМЕНТОВ
СЕМЕЙСТВО p-ЭЛЕМЕНТОВ
НОМЕР ГУППЫ
НОМЕР ПЕРИОДА
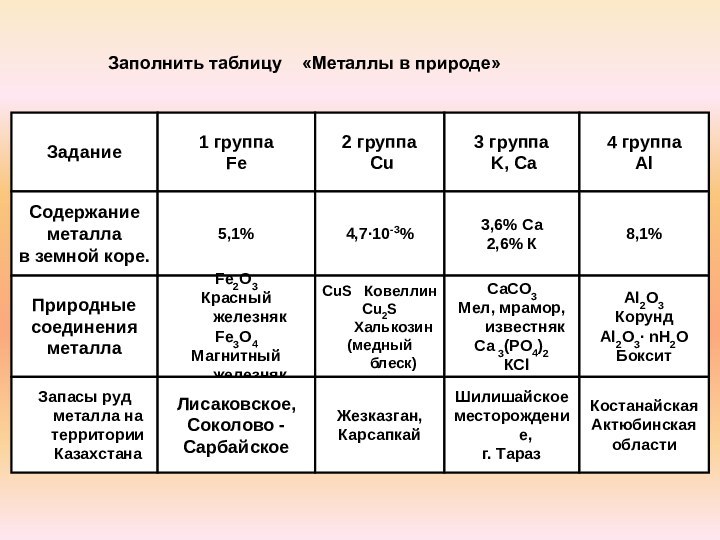
5,1%
Fe2O3
Красный железняк
Fe3O4
Магнитный железняк
Лисаковское,
Соколово -
Сарбайское
4,7∙10-3%
СuS Ковеллин
Сu2S Халькозин
(медный блеск)
Жезказган,
Карсапкай
3,6% Са
2,6% К
СаСО3
Мел, мрамор, известняк
Са 3(РО4)2
КСl
Шилишайское
месторождение,
г. Тараз
8,1%
Аl2О3
Корунд
Аl2О3∙ nН2О
Боксит
Костанайская Актюбинская области
Заполнить таблицу «Металлы в природе»
2 группа
Cu
3 группа
Zn
4 группа
Mn
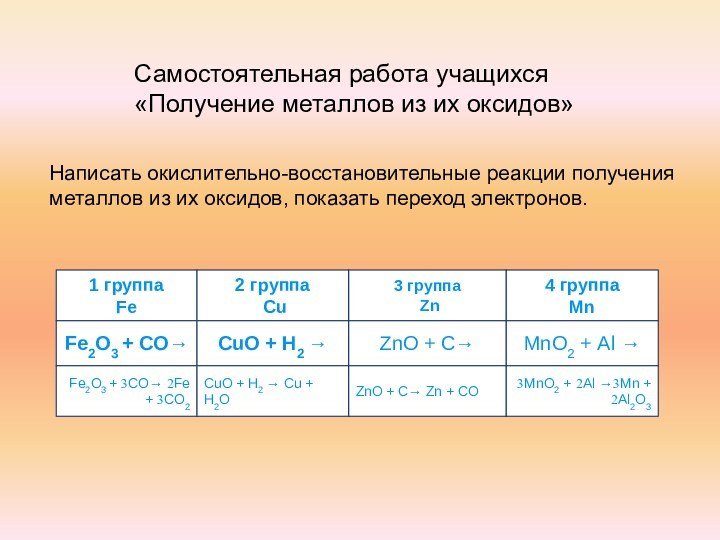
Fe2O3 + СО→
CuO + Н2 →
ZnO + C→
МnО2 + Аl →
Fe2O3 + 3СО→ 2Fe + 3СО2
CuO + Н2 → Cu + Н2О
ZnO + C→ Zn + CО
3МnО2 + 2Аl →3Мn + 2Аl2O3