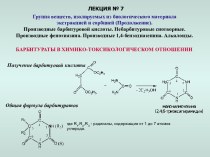
по химическим уравнениям:
находить количество, массу и объём продуктов
реакции по количеству, массе или объёму исходных веществ, продолжить формирование умения составлять уравнения химических реакций.
Никитина Н.Н., учитель химии, МАОУ "Средняя общеобразовательная школа №1" г.Нурлат