Слайд 3
Краткие сведение
История развития
Физиология : главные функции
ЦНС :
1- ВНД (восприятие , мышление , память ,
сон , речь , эмоция ….. итг)
2- моторная (движение , эфферентная)
3-сенсорная (чувствительная , афферентная )
4- вегетативная (автономная) (рефлексы , регуляции функции внутренних органов )
5- трофическая (регуляция питания клеток)
Анатомия (структуры , кровоснабжение , проводящие пути )
Гистология (нервная ткань , клетки )
Слайд 4
Продолжения кратких сведении
Продолговатый мозг :
1- защитные рефлексы

(мигание , слезоотделение , чихание , кашлевой и рвотный
рефлексы) .
2- установочные рефлексы (тонус мышц для позы и актов)
3- лабиринтные рефлексы (правильное распределение тонуса мышц)
4- рефлексы внутренних органов(ссс , дс , пс)
5- проводниковая функция
6- 5 по 8 черепно-мозговых нервов
Мост :
1- 9 по 12 черепно-мозговых нервов
2- проводниковая функция
Средний мозг :
1- красные ядра (правильное положение тела в пространстве )
2- черное вещество (жевание , глотание , АД , дыхание , )
3- ориентировочные рефлексы на звуковые и слуховые раздражения
4- 3 и 4 черепно-мозговые нервы
5- водопровод
Промежуточный мозг :
1- таламус (чувствительность , сон , мимическая эмоция )
2- гипоталамус (симпа , парасимп , все обмены , гормоны , темпир)
Базальные ядра :
1-полосатое тело (бег , плавание , прыжки , инстинкт )
2- бледный шар (сложные двигательные реакции )
ретикулярная формация (восходяшее влияние на кору и нисходяшее на мотонейроны )
Мозжечок (координация движения )
Кора :
1- правое полушари (познова.процессы , конкре.мышление , эмоция , зрительная память)
2- левое полушари (абстракное мышление , память , слух , письмо , счета)
3- лобная (письмо , речь)
4- височная (слух , речь)
5- затылочная (зрение , чтение , письмо ,узнавание предметов )
6- теменная (познавательные процессы (положение объектов , значимость раздражитель , произвольные движения))
Слайд 5
ЭТИОЛОГИЯ
Экзогенные факторы:
Физические
дефицит кислорода
ионизирующая радиация
электрический ток
вибрация
механическая травма
высокая/низкая температура
шум
Химические
- нейротропные яды (свинец, ванадий,
кураре, наркотики, этиловый и метиловый спирты, лекарства)
Биологические
- микробы- возбудители столбняка, ботулизма, менингококки, вирусы – бешенства, полиомиелита, гриппа)
Социальные
дефицит белка, витаминов
психогенные
Эндогенные факторы:
Врожденные:
наследственно обусловленные нарушения обмена веществ (гликогеноз II типа, липидозы, фенилкетонурия)
наследственные болезни (болезнь Дауна)
пороки развития, родовые травмы
Приобретенные:
ишемия мозга
гипогликемия
нарушения кислотно-основного равновесия
нарушения электролитного обмена
повреждение нейронов при почечной, печеночной недостаточности.
опухоли и др. патологические процессы
Слайд 6
МЕХАНИЗМЫ ЗАЩИТЫ НЕРВНОЙ СИСТЕМЫ
оболочки мозга, окружающие нейрон глиальные
и шванновские клетки
микроглия (система мононуклеарных фагоцитов)
гематоэнцефалический барьер
антисистемы ,
специальные регуляционные «уравновешивающие» (по И.П. Павлову) механизмы, направленные на предупреждение и ликвидацию возникающих изменений. Антисистема активируется или формируется вместе с образованием патологической системы, ограничивая развитие последней и подавляя ее деятельность. Например, при возникновении чрезмерной боли активируется антиноцицептивная система, регулирующая болевую чувствительность. Активация антиноцицептивной системы купирует возникновение болевого синдрома. Антиэпилептическая система контролирует уровень возбуждения в различных отделах ЦНС. Электрическая стимуляция каудального ядра моста, относящегося к антиэпилептической системе, подавляет активность в эпилептическом очаге в коре головного мозга.
высокая степень надежности функционирования нервных образований.
Слайд 7
ОСОБЕННОСТИ ДЕЙСТВИЯ ЭТИОЛОГИЧЕСКИХ ФАКТОРОВ
чем сильнее и дольше воздействие,

тем значительней его эффект
Однако даже слабые патогенные воздействия, если
они продолжительны и постоянны, могут вызывать глубокие и устойчивые изменения нервной системы. Например, при дробном, повторяющемся введении нейротропных токсинов (столбнячный, ботулинический и др.) их суммарная доза, вызывающая патологический эффект и гибель животного, может быть меньше той, которая вызывает аналогичный эффект при однократном введении всей дозы токсина (феномен Беринга).
Ежедневная электрическая стимуляция структур мозга током подпороговой силы, не сопровождающаяся видимой реакцией, обусловливает нарастание судорожной готовности мозга. С течением времени на те же подпороговые воздействия животное отвечает уже судорогами (феномен «раскачки», или киндлинг).
степень нарушения функций зависит не только от количества поврежденных нейронов, но и от формирования зоны торможения, которая увеличивает функциональный дефект, Вокруг очага поражения в мозговой ткани возникает зона обратимо поврежденных и заторможенных нейронов. Торможение играет роль охранительного механизма («охранительное торможение» по И.П. Павлову), предохраняя нейроны, обратимо поврежденные, от функциональной нагрузки, которая может способствовать их гибели. В связи с выключением этих нейронов из выполнения функции увеличивается степень функционального дефекта; такая ситуация имеет место при полиомиелите, травмах ЦНС и др.
Слайд 8
Пути поступления патогенных агентов в нервную систему
Гематогенное ,

В этом случае патогенный агент (токсическое вещество, вирусы, микробы
и др.) должен преодолеть гематоэнцефалический барьер (ГЭБ), который образуется сосудистой стенкой (эндотелиоцитами), а также глиальными элементами (астроцитами). ГЭБ осуществляет активный и избирательный транспорт из крови в мозг питательных и других биологически активных веществ, необходимых для деятельности мозга. Одновременно он защищает мозг от непосредственного действия находящихся в крови патогенных агентов. У плодов и новорожденных ГЭБ более проходим. Ряд токсических агентов (стрихнин, спирты, некоторые фармакологические препараты) сравнительно хорошо проходят ГЭБ. Для биологических возбудителей (вирусы, микробы) в норме ГЭБ практически непроницаем. Однако в условиях патологии при действии ряда физических и химических факторов усиливается проницаемость ГЭБ, что утяжеляет патологический процесс. Так, сильный длительный стресс способствует поступлению вируса гриппа в мозг.
по нервным стволам , Невральный путь характерен для столбнячного токсина, вирусов полиомиелита, бешенства и др. Входными воротами для столбнячного токсина является мионевральный синапс, откуда токсин поступает по двигательным волокнам в спинной и продолговатый мозг . В ЦНС токсины (столбнячный), вирусы, антитела к нервной ткани могут распространяться от нейрона к нейрону внутри нервных отростков (с аксотоком) и по межнейрональным пространствам.
Нарушения деятельности нервной системы и нервной регуляции функций могут быть вызваны условно - рефлекторно.
Слайд 9
Важно знать
Выпадение функции при возникновении структурных дефектов проявляется
не сразу. Оно происходит, когда повреждение достигло такого размера,
что уже стали недостаточными механизмы компенсации и перекрытия нарушенной функции. Иначе говоря, на этой стадии патологический процесс достиг значительного развития, а не начинается, как принято думать. В таких случаях врач имеет дело с уже довольно запущенной болезнью. Вот почему терапия бывает не всегда эффективна даже на этой, ранней стадии и столь важна диагностика патологических изменений на доклинической стадии процесса.
Слайд 10
феномена «второго удара»
восстановления признаков исчезнувшего патологического процесса
на базе следовых реакций при новом патогенном воздействии получил
название феномена «второго удара»
На поздних стадиях, когда происходит восстановление функций в необходимом объеме и полностью исчезают клинические признаки патологического процесса, могут сохраняться скрытые структурно-функциональные изменения в виде следов от бывшего патологического процесса
Слайд 11
вторичные эндогенные этиологические факторы
Этиологические факторы при их
действии на ЦНС , формируют вторичные эндогенные этиологические факторы:
повреждение
нейронов
нарушение межнейрональных связей
формирование ГПУВ – генератора патологически усиленного возбуждения
формирование патологической детерминанты, доминанта и патологической системы
Слайд 12
ПОВРЕЖДЕНИЕ НЕЙРОНОВ
В патогенезе
1-повреждение тела нейрона
2-повреждение аксонов.
3-повреждение
дендритов.
4-нарушение функции синаптического аппарата
Слайд 13
В патогенезе повреждения тела нейронов имеют значение:
1-повреждение мембран
2-нарушение энергообеспечения (Мозг потребляет около 20% от всей находящейся
в крови глюкозы )
3-ионный дисбаланс
4-нарушение регуляции клетки
Слайд 14
1-Патогенез повреждения мембран нейронов
1-активация ПОЛ.
2-активация мембранных фосфолипаз
и других гидролаз
3-осмотическое повреждение
4-иммунное повреждение.
Вследствие
увеличения проницаемости мембран происходит выход из нейрона различных веществ, в том числе антигенов, которые вызывают образование антинейрональных антител, что приводит к развитию аутоиммунного процесса. Нарушение барьерных свойств мембран обусловливает возрастание тока ионов Са2+ и Na+ в нейрон и К+ - из нейрона; эти процессы в сочетании с недостаточностью энергозависимых Na+-, K+- и Са2+-насосов (их деятельность изменяется также под влиянием усиленного ПОЛ) приводят к частичной деполяризации мембраны. Увеличенный вход Ca2+ не только вызывает гиперактивацию нейрона, но и при чрезмерном его содержании в клетке ведет к патологическим изменениям метаболизма и внутриклеточным повреждениям
Слайд 16
Весьма чувствительны к гипоксии тормозные механизмы. Одним из

следствий этого является растормаживание неповрежденных структур ЦНС. На ранних
стадиях ишемии, когда нейроны мозга еще способны давать реакцию, они могут гиперактивироваться. На поздних стадиях ишемии гиперактивация нейронов сменяется их инактивацией.
С поступлением Na+ в нейрон связана первая, острая фаза поражения нейрона. Возрастание концентрации Na+ в цитозоле нейрона приводит к повышению осмолярности, что обусловливает вход воды в нейрон и его набухание. В дальнейшем повышение осмолярности нейрона связано также с накоплением в нем Са2+, молочной кислоты, неорганического фосфора. С входом Са2+ в нейрон связана вторая фаза повреждения нейрона. Увеличение количества Са2+, поступающего в нейрон, обусловливается активацией глутаматных рецепторов в связи с усиленным выделением глутамата нервными окончаниями при ишемии. Антагонисты глутаматных рецепторов и антагонисты Са2+ (блокаторы Са2+-каналов) способны предотвратить ишемическую дегенерацию нейронов и оказать лечебный эффект.
Слайд 17
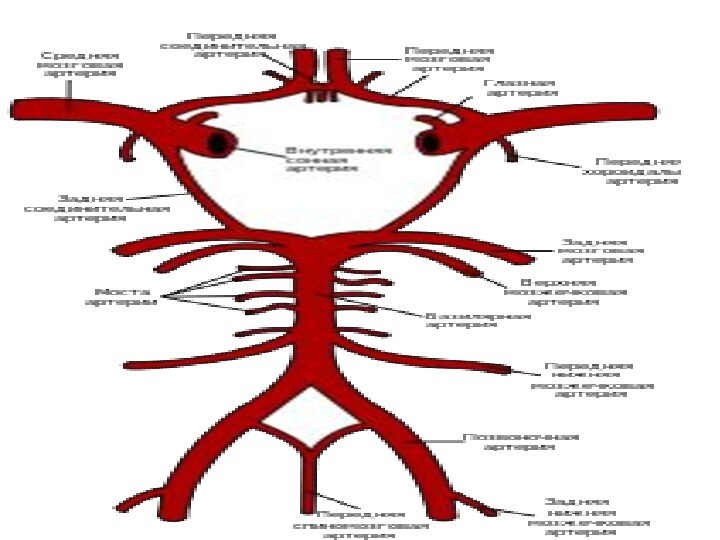
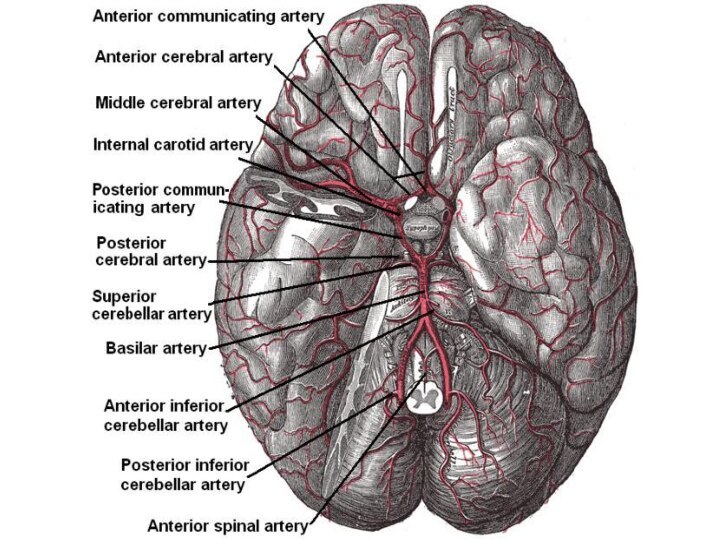
И раз мы говорим об ишемии мозга ,
значит необходимо коснуться с механизмами нарушения мозгового кровообращения
Для этого нужно повторить анатомию мозгового кровообращения
Слайд 20
Нарушение мозгового кровообращения
Нарушения мозгового кровообращения могут быть :
1-
острыми (преходящие нарушения, инсульты, острая гипертоническая энцефалопатия)
2- хроническими
Слайд 21
Причинами нарушений мозгового кровообращения могут быть следующие заболевания:
Атеросклероз
эссенциальная гипертензия
Васкулиты
пороки сердца
болезни крови
и др.
Слайд 22
В патогенезе нарушений мозгового кровообращения лежат:
1- Изменения системного
кровообращения (артериальные гипер- и гипотензии)
Артериальная гипертензия → гипертензия в
сосудах мозга → кровоизлияние в ткань мозга (при патологически измененных стенках сосудов), отек мозга, спазмы мозговых артерий
Артериальная гипотензия → ослабление мозгового кровотока, дефицит кровоснабжения тканей мозга →гипоксическое повреждение структур мозга
2- Патологические изменения в сосудистой системе самого мозга: ишемия, венозная гиперемия, артериальная гиперемия ткани мозга
Слайд 23
Ишемия мозга может быть связана с ангиоспазмом, тромбозом

или эмболией, стенозирующим атеросклерозом сосудов мозга, воспалительными заболеваниями сосудов
мозга (системная красная волчанка и др.), изменениями реологических свойств крови.
Ангиоспазм имеет типичную локализацию – крупные артериальные стволы в области основания мозга, спазм мелких пиальных артерий наступает редко.
Изменения реологических свойств крови обусловлены внутрисосудистой агрегацией эритроцитов, нарушением их эластичности, повышением гематокритного показателя и изменением траектории движения эритроцитов в просвете сосудов (тромбоцитоз, полицитемия, серповидно-клеточная анемия, ДВС-синдром).
Венозная гиперемия мозга → повышение внутричерепного давления и сдавление мозга→нарушение кровоснабжения мозга и функции мозга. Компенсаторно происходит сужение магистральных артерий мозга, при этом ограничивается приток крови в мозг и снижается степень венозного застоя, но при этом усугубляется гипоксия мозга.
Артериальная гиперемия возникает при резком расширении ветвлений пиальных артерий при повышении интенсивности обмена веществ, судорожной активности, при резком понижении общего артериального давления, после ишемии.
Артериальная гиперемия → повышение внутричерепного давления, активация ПОЛ, отек мозга
Слайд 24
Основные симптомы при нарушении мозгового кровообращения:
двигательные нарушения (парезы,
параличи, экстрапирамидные расстройства, расстройства координации, гиперкинезы)
расстройства чувствительности (снижение
чувствительности, иногда боли)
очаговые нарушения высших корковых функций (афазия(нарушение речи), аграфия (потеря способность писать ), алексия(нарушения чтения))
эпилептиморфные припадки, изменения интеллекта, памяти, эмоционально-волевой сферы, психопатологическая симптоматика
Слайд 25
ИНСУЛЬТ
Инсульт – это острое нарушение мозгового кровообращения, клинический
синдром, характеризующийся внезапным появлением неврологических расстройств, которые сохраняются в
течение 24 часов и обусловлены нарушением мозгового кровообращения.
Факторы риска:
1- генетическая предрасположенность к сосудистым заболеваниям
2- гиперлипидемия,
3- артериальная гипертензия,
4- гипергликемия,
5- гиподинамия,
6- ожирение
7- курение,
8- злоупотребление алкоголем.
Слайд 26
По патогенезу различают :
ишемический и геморрагический инсульты
Ишемический инсульт
является результатом тромбоза или эмболии сосудов мозга. Чаще всего
наблюдается тромбоз внутренней сонной артерии, средней мозговой или базилярной артерий. Источником эмболов чаще являются измененные клапаны сердце, дуга аорты, сонные артерии. Иногда происхождение эмбола связано с венами большого круга кровообращения. Наиболее часто эмболы обнаруживаются в бассейне среднемозговой артерии, реже позвоночной и базилярной.
Величина инфаркта зависит от возможностей коллатерального кровообращения.
Слайд 27
Геморрагический инсульт
развивается в результате разрыва сосуда, разрыва
аневризмы, или как следствие вазомоторных нарушений (дистонии сосудов).
Неврологические симптомы
при инсультах зависят от повреждения участка ткани, кровоснабжаемой поврежденным сосудом. При геморрагическом инсульте к очаговой симптоматике присоединяются симптомы, являющиеся следствием кровоизлияния в мозг, – повышение внутричерепного давления, отек мозга, сдавление тканей мозга.
Слайд 28
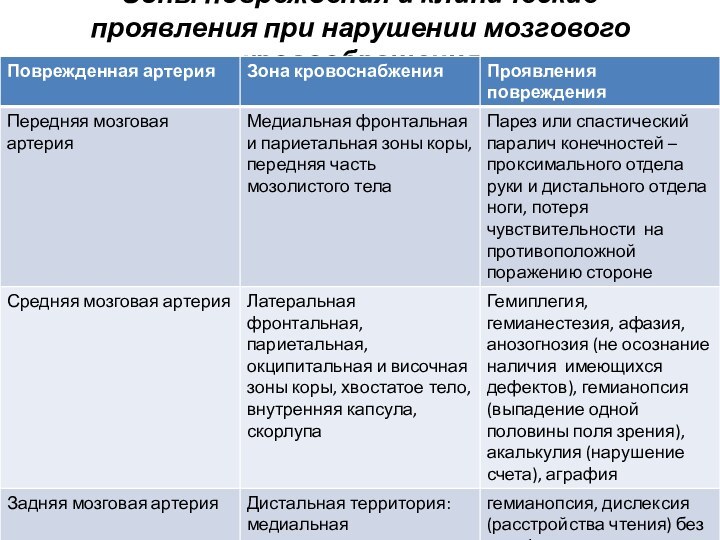
Зоны повреждения и клинические проявления при нарушении мозгового
кровообращения
Слайд 31
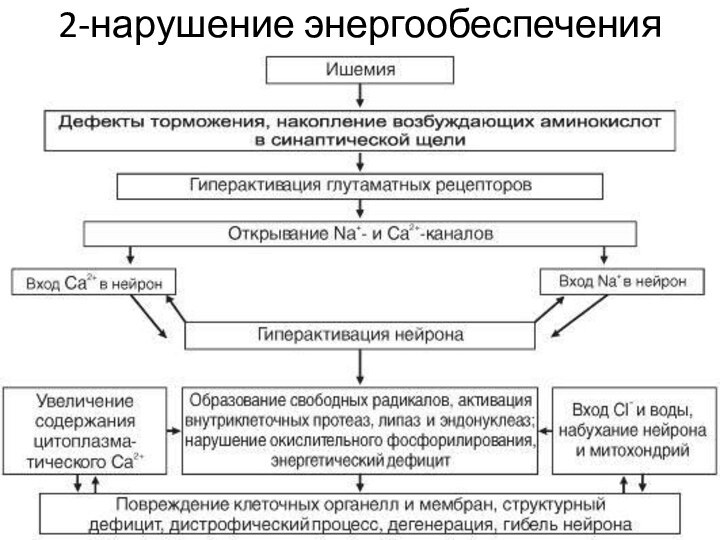
Патогенез повреждения нейронов при нарушении мозгового кровообращения
Нарушение кровоснабжения

участка ткани → гипоксическое повреждение нейронов.
Потребность нейронов в энергообеспечении
– самая высокая из всех клеток организма. Нейрон коры головного мозга потребляет 250-450 мкл О2 в мин (гепатоцит – 60 мкл), мозг потребляет около 20% от всей глюкозы, находящейся в крови. Мозг не имеет собственных запасов кислорода, снижение его поступления в мозг сопровождается немедленным расстройством функций, а затем и гибелью нейронов. Нарушение психики выявляется уже тогда, когда напряжение кислорода в артериальной крови падает до 40-50 мм рт.ст. При снижении рО2 до 30 мм.рт.ст. через 20 сек. наступает потеря сознания, а еще через 20 сек прекращается нормальная электрическая активность мозга. Полное восстановление функций мозга возможно в тех случаях, когда остановка кровообращения не превышает 5-6-мин.
На ранних этапах острой ишемии возникает гиперактивация нейронов. Она связана с их растормаживанием вследствие ослабления или выпадения чувствительных к гипоксии тормозных механизмов и с прямой деполяризацией нейронов вследствие входа натрия и кальция. Поступление этих ионов связано с раскрытием кальциево - натриевых каналов, недостаточностью натрий-калиевого насоса, действием возбуждающих аминокислот – глутамата. Накопление глютамата при ишемии обусловлено увеличением внутриклеточной концентрации натрия, при этом нарушается захват глютамата из синаптической щели. Кроме того, вследствие дефицита энергии нарушается метаболизм глютамата. Избыток глютамата приводит к стимуляции глютаматных рецепторов, что увеличивает поступление в нейрон кальция и натрия. Вхождение этих ионов деполяризует нейроны, стимулирует дополнительных вход кальция. Перегрузка нейронов кальцием способствует растормаживанию и гиперактивации нейронов, активирует кальций-зависимые ферментные системы, включая протеазы, фосфолипазы и эндонуклеазы, что приводит к гибели клетки. Эксперименты на животных показали уменьшение зоны ишемического повреждения при применении ингибиторов глютаматных рецепторов.
Слайд 32
Мы где сейчас
В патогенезе повреждения
нейрона :
1-повреждение тела нейрона
2-повреждение аксонов.
3-повреждение дендритов.
4-нарушение
функции синаптического аппарата
Слайд 33
ПОВРЕЖДЕНИЕ АКСОНОВ
1. Нарушение проведения возбуждения
при воспалении, рубцовых изменениях
нерва,
при сдавлении нервных волокон,
при демиелинизации нервных волокон,
дегенерации
аксона,
при ингибировании Na+/К+ - АТФ-азы Специфическим блокатором Na+-каналов является тетродотоксин - яд, вырабатывающийся во внутренних органах рыбы фугу, или местными анестетиками (новокаин, лидокаин и др.) , дифецит АТФ
2. Нарушение аксонального транспорта
при разрушении микротрубочек и нейрофиламентов (колхицин, винбластин),
при дефиците АТФ,
при дегенерации аксона (дефицит вит. В1 и В6, промышленные яды- гексахлороформ, алкоголь)
↓
дистрофия нейронов и иннервируемых ими тканей.
Слайд 34
ПОВРЕЖДЕНИЕ ДЕНДРИТОВ
Дендриты и их шипики являются самыми ранимыми
структурами нейрона. При старении шипики и ветви дендритов редуцируются,
при некоторых дегенеративных и атрофических заболеваниях мозга (старческое слабоумие, болезнь Альцгеймера) они исчезают. Дендрошипиковый аппарат страдает при гипоксии, ишемии, сотрясении мозга, стрессорных и невротизирующих воздействиях.
↓
- нарушение интегративной функции нервной системы
-уменьшение площади синаптических контактов
-возникновение эпилептической активности.
Слайд 35
СИНАПТИЧЕСКИЙ АППАРАТ
1-синтез медиатора →2- транспорт медиатора к синаптической
щели → 3-депонирование в пресинаптической области → 4-выброс в
синаптическую щель → 5-взаимодействие с рецепторами → распад нейромедиаторов →6- обратный захват.
Слайд 36
ПОВРЕЖДЕНИЕ СИНАПТИЧЕСКОГО АППАРАТА
1. нарушении синтеза медиатора
2. нарушение транспорта
медиатора
3. нарушение депонирования медиатора в нервных окончаниях.
4. нарушение
секреции медиатора в синаптическую щель
5. нарушение взаимодействия медиатора с рецептором
6. нарушение обратного захвата медиатора из синаптической щели.
Слайд 37
Синаптическая стимуляция и повреждение нейронов
Возбуждающая синаптическая стимуляция

может играть важную роль в развитии патологии нейрона. Усиленная
и длительная синаптическая стимуляция сама по себе вызывает функциональное перенапряжение нейрона, которое может завершиться дегенерацией внутриклеточных структур. Эти повреждения усиливаются при нарушениях микроциркуляции и мозгового кровообращения, действии токсических факторов.
Первостепенное значение синаптическая стимуляция имеет при развитии аноксических (ишемических) повреждений. Культура тканей нейронов становится чувствительной к аноксии лишь после установления синаптических контактов между нейронами. Синаптическая стимуляция реализуется через действие возбуждающих аминокислот (глутамат, аспартат, L-гомоцистеинат), причем эти повреждения подобны тем, которые возникают при ишемии и связаны с увеличенным содержанием внутриклеточного Са2+. Этот эффект известен как нейротоксическое (или цитотоксическое) действие возбуждающих аминокислот. С синаптической гиперактивацией, действием возбуждающих аминокислот и гипоксией связаны повреждение и гибель нейронов при эпилептическом статусе и в постишемическом периоде. При этом к патогенному действию указанных факторов присоединяется энергетический дефицит.
Слайд 38
Для жизнедеятельности нейрона, который как высокодифференцированная клетка не
способен митотически делиться, внутриклеточная регенерация является единственным способом структурного
обновления нейронов и поддержания их целостности. К ней относятся синтез белков, образование внутриклеточных органелл, митохондрий, мембранных структур, рецепторов, рост нервных отростков (аксоны, дендриты, дендритные шипики) и др.
Процессы внутриклеточной регенерации требуют высокого энергетического и трофического обеспечения и полноценного метаболизма клетки. При повреждениях нейрона, возникновении энергетического и трофического дефицита, нарушениях деятельности генома страдает внутриклеточная регенерация, падает пластический потенциал клетки, распад внутриклеточных структур не уравновешивается ими.
Слайд 39
Мы где сейчас
Этиологические факторы при их действии на
ЦНС , формируют вторичные эндогенные этиологические факторы:
повреждение нейронов
нарушение
межнейрональных связей
формирование ГПУВ – генератора патологически усиленного возбуждения
формирование патологической детерминанты, доминанта и патологической системы
Слайд 40
ГЕНЕРАТОР ПАТОЛОГИЧЕСКИ УСИЛЕННОГО ВОЗБУЖДЕНИЯ (ГПУВ)
это агрегат гиперактивных
нейронов, продуцирующий интенсивный, неконтролируемый поток импульсов.
Механизмы формирования:
1-устойчивая значительная деполяризация нейронов (возбуждающие нейромедиаторы и АК (глутамат), гипоксия и т.д. , ишемия)
2-дефицит торможения нейронов (снижение синтеза ГАМК или блокада рецепторов ,действие столбнячного токсина, стрихнина, пенициллина и других конвульсантов )
3-деафферентация нейронов (отсутствие тормозящего эффекта из периферических органов)
4-повреждение нейронов и изменения их окружения.
ГПУВ → патологическая детерминанта → патологическая система → нейропатологические синдромы.
Слайд 41
Патогенетическое значение ГПУВ
Основное патогенетическое значение генератора заключается
в том, что он гиперактивирует тот отдел ЦНС, в
котором он возник или с которым он непосредственно связан, вследствие чего этот отдел приобретает значение патологической детерминанты , формирующей патологическую систему. Поскольку патологические системы лежат в основе соответствующих нервных расстройств (нейропатологических синдромов), образование генератора является начальным звеном этих расстройств.
Слайд 42
ПАТОЛОГИЧЕСКАЯ ДЕТЕРМИНАНТА
Патологическая детерминанта является формирующим, ключевым и

управляющим звеном патологической системы. Возникновение детерминанты относится к разряду
типовых патологических процессов, реализующихся на системном уровне.
Примером патологической детерминанты в коре головного мозга является мощный эпилептический очаг, под влиянием которого формируется комплекс из разрозненных, более слабых очагов эпилептической активности. Такой очаг формирует эпилептический комплекс, представляющий собой патологическую (эпилептическую) систему. Если подавить с помощью фармакологических средств или хирургически удалить детерминантный очаг, то комплекс распадается и вместо него вновь возникают отдельные эпилептические очаги.
Отделы ЦНС, испытывающие длительное влияние патологической детерминанты, с течением времени могут сами становиться детерминантами. Вначале такая вторичная детерминанта зависима от первичной: она исчезает, если ликвидируется первичная детерминанта. В дальнейшем вторичная детерминанта может приобрести самостоятельное патогенетическое значение
Патологическая детерминанта является наиболее резистентной частью патологической системы. При подавлении патологической системы или при ее естественной ликвидации , детерминантная структура сохраняется еще тогда, когда другие образования системы уже нормализовались и вышли из ее состава («детерминанта умирает последней»). При восстановлении патологической системы под влиянием новых воздействий, раньше других активируется детерминантная структура («детерминанта воскресает первой»).
Слайд 43
ПАТОЛОГИЧЕСКАЯ СИСТЕМА
новая патодинамическая организация, возникающая в ЦНС

в условиях повреждения, деятельность которой имеет биологически отрицательное значение
(Г.Н. Крыжановский). Главным признаком патологической системы является ее дезадаптивное или прямое патогенное значение для организма. Этот признак отличает патологическую систему от физиологической, деятельность которой имеет адаптивное значение и направлена на достижение полезного для организма результата.
Наглядным примером деятельности патологической системы является патологический чесательный рефлекс. Он возникает при создании генератора в брахиальном отделе спинального аппарата чесательного рефлекса. Аппарат чесательного рефлекса становится патологической детерминантой, которая превращает физиологический чесательный рефлекс в патологический. Животное начинает расчесывать задней лапой зону проекции рефлекса. Эти расчесывания возникают спонтанно. С течением времени, по мере развития патологической системы, они становятся все более частыми, продолжительными и ожесточенными и могут завершаться раздиранием тканей. Животное не в состоянии прекратить эти расчесывания, несмотря на их бесполезность и вредящий эффект. Подобного рода неукротимое насильственное поведение наблюдается при многих формах патологии нервной системы у человека
Слайд 44
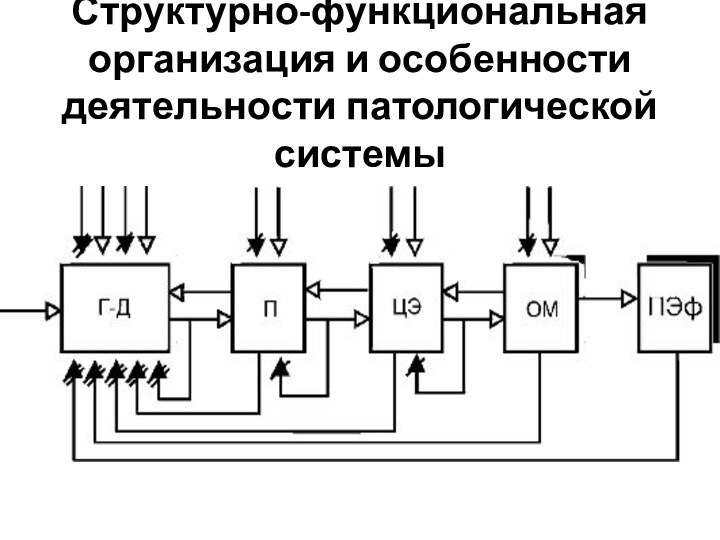
Структурно-функциональная организация и особенности деятельности патологической системы
Слайд 45
Патогенетическое значение патологической системы
Патологические системы лежат в
основе разнообразных нервных расстройств, относящихся к различным сферам деятельности
нервной системы, поэтому их образование имеет значение практически универсального патогенетического фактора.
В качестве примера таких патологических систем можно привести паркинсонизм, эмоционально-поведенческие расстройства, фотогенной эпилепсии (генератор в системе зрительного анализатора - в латеральном коленчатом теле); патологически удлиненного сна (генератор в сомногенной системе) и др
Ликвидируется патологическая система : естественно под действием антисистемы или с врачебным вмешательством
Доминанта является механизмом межсистемных отношений, а детерминанта - механизмом внутрисистемных отношений.
Слайд 46
ОСНОВНЫЕ ПРОЯВЛЕНИЯ НАРУШЕНИЙ НЕРВНОЙ СИСТЕМЫ
дефицит торможения, синдром
растормаживания
синдром денервации
синдром деафферентации
нарушение трофики.
Слайд 47
ДЕФИЦИТ ТОРМОЖЕНИЯ. СИНДРОМ РАСТОРМАЖИВАНИЯ -
выход нижележащих отделов
ЦНС из под контролирующего влияния вышележащих отделов.
первичный -
вследствие прямого повреждения тормозных механизмов (столбнячный токсин, стрихнин, конвульсанты, нарушающие ГАМК-ергические механизмы торможения)
вторичный вследствие действия деполяризующих агентов (возбуждающих аминокислот), приводящих к чрезмерной активности нейронов.
Дефицит торможения и растормаживание встречаются практически при всех формах патологии нервной системы, поэтому они относятся к типовым патологическим процессам нервной системы. Дефицит торможения играет существенную роль в формировании и деятельности ГПУВ.
↓
гиперактивность нейрона и формирование ГПУВ
Слайд 48
децеребрационная ригидность
Характерным экспериментальным синдромом растормаживания является децеребрационная ригидность.

Она вызывается, по Шеррингтону, перерезкой ствола мозга между передним
и задним четверохолмием. В этих условиях происходит выпадение тормозных влияний со стороны супраспинальных структур и особенно красных ядер, и проявляются возбуждающие тонические влияния вестибулярных ядер Дейтерса на мотонейроны спинного мозга, особенно γ-мотонейроны, которые в норме находятся под тормозным контролем со стороны красных ядер. Перерыв (например, путем перерезки задних корешков) расторможенной, патологически усиленной γ-петли на уровне спинного мозга ведет к исчезновению ригидности соответствующих мышц. Поэтому данный вид децеребрационной ригидности называют также γ-ригидностью (Р. Гранит).
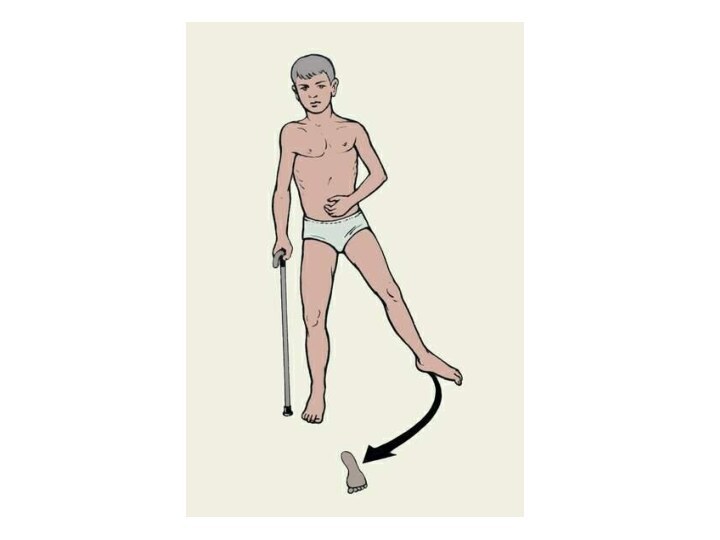
У человека при выпадении моторных корковых влияний (например, после геморрагического инсульта) возникает спастическая флексорная установка верхней и экстензорная установка нижней конечностей (поза Вернике-Манна).
Целый ряд патологических рефлексов возникает в условиях выпадения влияний со стороны коры и подкорковых образований; эти рефлексы являются результатом растормаживания центров спинного или продолговатого мозга. Они представляют собой гиперболизированные неконтролируемые реакции, которые являлись нормальными в раннем постнатальном периоде и затем были подавлены при развитии регулирующих влияний со стороны высших отделов ЦНС. К ним относятся рефлекс Бабинского (растопыривание пальцев ноги вместо их сгибания при раздражении подошвы), хватательный, сосательный и другие рефлексы.
Слайд 50
СИНДРОМ ДЕНЕРВАЦИИ
это комплекс изменений, возникающих в постсинаптических нейронах,
органах и тканях в связи с выпадением нервных влияний
на эти структуры.
↓
исчезновение концевой пластинки на мышечном волокне, и появление ацетилхолиновых рецепторов на всем протяжении мышечного волокна
↓
повышение чувствительности к ацетилхолину и др. БАВ
↓
фибриллярные подергивания мышцы
Слайд 51
СИНДРОМ ДЕАФФЕРЕНТАЦИИ
выключение импульсации, поступающей в нейрон –
афферентной импульсации
↓
повышение возбудимости нейрона и нарушение тормозных механизмов
↓
формирование ГПУВ
Слайд 52
Спинальный шок
Спинальный шок возникает после перерыва спинного
мозга и представляет собой глубокое, но обратимое угнетение двигательных
и вегетативных рефлексов, осуществляющихся ниже перерыва. Угнетение рефлексов связано с выпадением активирующей стимуляции со стороны головного мозга. У лягушек, у которых зависимость спинного мозга от головного значительно меньше, чем у высших животных, спинальный шок длится несколько минут, у человекообразных обезьян и человека - несколько месяцев.
У человека полная арефлексия после перерыва спинного мозга является начальной стадией полной параплегии. В дальнейшем происходит постепенное восстановление двигательных и вегетативных рефлексов. Вначале появляются сгибательные рефлексы пальцев, имеющие характер патологических рефлексов (рефлекс Бабинского и др.), после этого осуществляются более значительные и затем генерализованные спинальные рефлексы и движения типа спинальных автоматизмов.
Слайд 53
НАРУШЕНИЕ ТРОФИКИ ТКАНЕЙ И ОРГАНОВ
под нервной трофикой понимают
трофические влияния нейрона, которые обеспечивают нормальную жизнедеятельность иннервируемых им
структур – других нейронов и тканей.
Трофогены (трофические факторы), нейропептиды - эндорфины, энкефалины, медиаторы, факторы роста нервов, др. факторы роста.
Патотрофогены – вещества, образующиеся поврежденными нейронами.
Нарушение образования трофогенов,
↓
нарушение аксонального транспорта трофогенов,
образование патотрофогенов
↓
дистрофические изменения:
нарушение обмена веществ, растормаживание генетического аппарата → синтез аномальных белков, которые являются аутоантигенами, → активация аутоиммунных процессов, присоединение вторичной инфекции, атрофия
Слайд 54
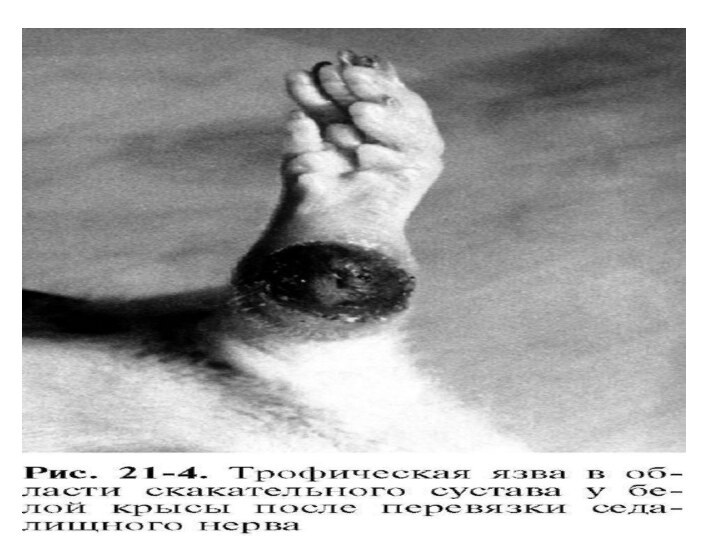
Классический опыт Ф. Мажанди (1824), послуживший началом разработки
всей проблемы нервной трофики, заключается в перерезке у кролика
первой ветви тройничного нерва. В результате операции развивается язвенный кератит(воспаление роговицы глаз), вокруг язвы возникает воспаление, и со стороны лимба в роговицу врастают сосуды, которые в ней в норме отсутствуют. Врастание сосудов является выражением патологического растормаживания сосудистых элементов - в дистрофически измененной роговице исчезает фактор, который тормозит в норме рост в нее сосудов, и появляется фактор, который активирует этот рост.
Слайд 56
Мы где?
Физиология : главные функции ЦНС :
1- ВНД
(восприятие , мышление , память , сон , речь
, эмоция ….. итг)
2- моторная (движение , эфферентная)
3-сенсорная (чувствительная , афферентная )
4- вегетативная (автономная) (рефлексы , регуляции функции внутренних органов )
5- трофическая (регуляция питания клеток)
Слайд 57
Нарушения движения
Нейрогенные расстройства движений характеризуются патологическими изменениями
количества движений, их темпа и координации.
Классы нейрогенных расстройств движений:
Выделены следующие классы типовых форм нейрогенных расстройств движения:
1- Гипокинезии — ограничение объёма и скорости произвольных движений.
2- Гиперкинезии — выполнение избыточных непроизвольных движений.
3- Гиподинамии — снижение двигательной активности и силы мышечных сокращений при движении.
4- Атаксии — нарушение координации движений.
Слайд 58
Анатомические системы регуляции движений
К системам, осуществляющим регуляцию движений,
относятся
1- пирамидная
2- экстрапирамидная системы
3- а также структуры, ответственные
за регуляцию координации движений.
Аксоны всех нисходящих путей заканчиваются исключительно на мотонейронах спинного мозга.
Слайд 59
Гиперкинезии
Гиперкинезы — увеличение объёма и количества непроизвольных движений
— развиваются вследствие поражения нейронов различных структур головного мозга
(экстрапирамидной системы, таламуса, субталамического ядра, зубчатого ядра мозжечка, красного ядра, коры и их систем связи).
Ведушое звено развития Гиперкинезы это
ГПУВ
Слайд 60
выделяют несколько типов гиперкинезий :
1- В зависимости
от локализации поражённых структур мозга выделяют
корковые
подкорковые
стволовые
2-В зависимости от распространённости процесса различают
. общие (генерализованные, с вовлечением нескольких или большинства групп мышц)
. местные (локальные, характеризующиеся непроизвольным сокращением отдельных мышц или их волокон)
3- В зависимости от преобладания фазных (быстро сменяющихся) или тонических (медленных) компонентов сокращения различают :
. быстрые
. медленные
Слайд 61
Быстрые гиперкинезии.
К быстрым гиперкинезам относят судороги, хорею, дрожания
(тремор) и тики.
Судороги — внезапно возникающие, приступообразные или
постоянные непроизвольные сокращения мышц различной интенсивности, продолжительности и распространённости. Выделяют клонические, тонические и смешанные судороги.
Клонические : Кратковременные и нерегулярные сокращения отдельных групп мышц, следующие друг за другом через сравнительно небольшие промежутки времени. Возникают чаще всего в результате чрезмерного возбуждения коры больших полушарий или поражения структур пирамидной системы. Распространённые выраженные клонические судороги обозначают как конвульсии.(вторая фаза эпелипсии , )
Слайд 62
Тонические
Длительные (до нескольких десятков секунд) мышечные сокращения, в
результате которых происходит «застывание» туловища или конечностей в различных
вынужденных положениях. Развиваются при чрезмерном возбуждении подкорковых структур и некоторых видах интоксикации (например, алкогольной, столбнячной, окисью углерода , первая фаза эпилепсия ). При столбняке может развиться опистотонус.
Смешанные (клонико‑тонические, тонико‑клонические). Наблюдаются при коматозных и шоковых состояниях (например, при диабетической, печёночной или уремической коме; ожоговом или анафилактическом шоке).
Слайд 63
Хорея
беспорядочные, быстрые, неритмичные, насильственные сокращения
различных групп мышц. Наблюдается при длительной ишемии мозга (например,
его сосудов), атеросклеротическом поражении, ревматическом энцефалите, черепно‑мозговых травмах. Может иметь наследственное происхождение (например, хорея Хантингтона).
Тремор
гиперкинез дрожательного типа. Характеризуется непроизвольными, стереотипными ритмическими колебательными движениями тела или его частей в результате повторяющихся сокращений и расслаблений мышц. Возникает преимущественно при поражении ствола мозга. Наблюдается при органических поражениях головного мозга (рассеянном склерозе, болезни Уилсона–Коновалова, энцефалите, расстройстве кровоснабжения), экзогенной интоксикации организма (алкоголем, ртутью, морфином , паркинсон).
Бывает 1- паркинсоновские (мало дофамина )
2- интенционные (истерии )
Отлечаются держанием чашку чайа
Слайд 64
Тик
— быстрые непроизвольные стереотипные сокращения мышцы или групп
мышц, обусловливающие насильственные движения (например, мигание, прищуривание глаз, жестикуляция).
Наблюдаются в основном при поражении экстрапирамидной системы в результате энцефалита, интоксикаций, в том числе ЛС (например, при употреблении психофармакологических средств), а также при некоторых психических расстройствах.
Медленные гиперкинезии.
Медленные гиперкинезы представлены :
атетозом
спастической кривошеей.
Слайд 65
Атетоз
непроизвольные стереотипные, медленные червеобразные вычурные движения, возникающие в
результате одновременной длительной активации мышц агонистов и антагонистов. Чаще
всего поражаются дистальные отделы конечностей пальцев рук и стоп. Развиваются при поражении стриарной системы (хвостатого ядра, скорлупы) при энцефалите, нарушениях мозгового кровообращения, черепно‑мозговых травмах, опухолях подкорковых отделов головного мозга.
Слайд 66
ЭПИЛЕПСИЯ
Эпилепсия представляет собой хроническое заболевание головного мозга, характеризующееся

повторными приступами нарушений двигательных, чувствительных, вегетативных, мыслительных или психических
функций Эти приступообразные нарушения функции мозга, вызваны синхронной деполяризацией группы нейронов мозга (ГПУВ).
Все виды эпилептических приступов подразделяются на парциальные (очаговые, фокальные, локальные, локализационно-обусловленные), генерализованные и неклассифицируемые.
Парциальные приступы диагностируются в том случае, когда в начале пароксизма имеются четкие клинические и электрофизиологические критерии вовлечения определенных структур головного мозга. Например, клонические судороги одной половины лица и руки (фациобрахиальные приступы) обычно указывают на наличие эпилептического очага в средне-нижних отделах передней центральной извилины; обонятельные галлюцинации – в области крючка; фотопсии – (появления беспредметных образов , точек , пятен , фигур )в коре затылочной доли и т.д. В том случае, если приступ начинается как парциальный, а затем происходит вовлечение всей мускулатуры туловища и конечностей и признаки вовлечения обеих гемисфер на ЭЭГ, то его следует классифицировать как очаговый с вторичной генерализацией. Простые приступы – без потери сознания, сложные приступы - пароксизмы с полным выключением сознания.
Абсансы – разновидность генерализованных бессудорожных приступов, характеризующаяся высокой частотой и короткой продолжительностью пароксизмов с выключением сознания и наличием на ЭЭГ специфического паттерна – генерализованной пик-волновой активности с частотой 3 Гц. Абсансы – один из наиболее частых видов эпилептических приступов у детей и подростков.
Слайд 67
По этиологии различают
идиопатическую эпилепсию, которая развивается вследствие
наследственно обусловленной повышенной возбудимости нейронов
симптоматическую эпилепсию (вторичную), развивающуюся вследствие
патологических процессов в ЦНС (травмы, инсульты, воспаление, опухоли, рубцы и др.)
Слайд 68
Патогенез:
1- Фаза. Инициации.
Формирование группы гиперактивных
нейронов и их синхронная деполяризация. Гиперактивность нейронов
обусловлена относительно продолжительной деполяризацией нейрональной мембраны, обусловленной входом внеклеточного кальция (Ca2+)
→открываются вольтажные натриевые каналы, входит Na+, и генерируется повторный потенциал действия.
2 - Фаза. Распространение волны возбуждения. При повторяющейся перезарядке мембраны происходит:
увеличение внеклеточного калия K+, который снижает гиперполяризацию деполяризации соседних нейронов
аккумуляция Ca2+ в пресинаптической терминали → увеличение высвобождения нейротрансмиттеров
активация возбуждающих аспартатных рецепторов, которые активируются при деполяризации → вход Ca2+ в нейрон и его активация
снижение действия тормозных синапсов, что обусловлено снижением чувствительности ГАМК рецепторов
Слайд 69
Травмы мозга, инсульты, инфекции, экзогенные и эндогенные интоксикации,
нарушения обмена - гипогликемия, нарушения КОС или электролитного обмена,
наследственные дефекты рецепторов и ионных каналов
нарушение деятельности ионных насосов, усиление входа натрия и кальция, усилен выход калия, изменение состава ионов в межнейрональной среде с повышением калия и уменьшением кальция и магния, повышенное действие возбуждающих нейромедиаторов, ослабление тормозных
гиперактивация нейрона → ГПУВ→ судороги
Слайд 70
Гипокенезии
ограничение объёма и скорости произвольных движений.
Бывает
1-
парезы : снижение амплитуды и силы
2- параличи
Отсутствие
произвольных движении
Периферические центральные
(вялые) (спастические )
1- атрофия мышц 1- Отсутствие атрофии мышц
2- снижение тонуса 2- повышение тонуса
3- отсуствие рефлексов 3- сохранение и появления
патологических рефлексов
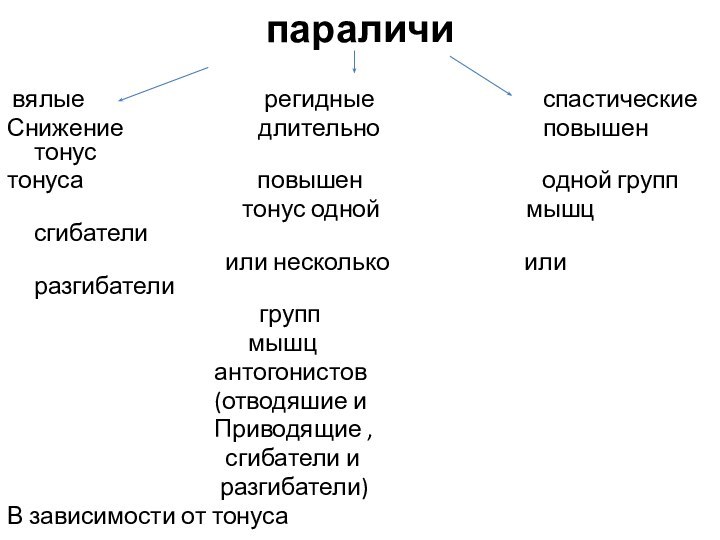
регидные спастические
Снижение длительно повышен тонус
тонуса повышен одной групп
тонус одной мышц сгибатели
или несколько или разгибатели
групп
мышц
антогонистов
(отводяшие и
Приводящие ,
сгибатели и
разгибатели)
В зависимости от тонуса
Слайд 72
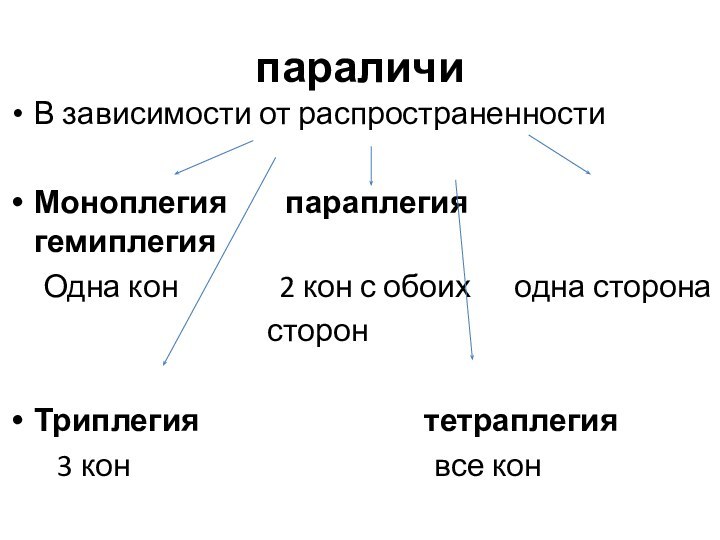
параличи
В зависимости от распространенности
Моноплегия
параплегия гемиплегия
Одна кон 2 кон с обоих одна сторона
сторон
Триплегия тетраплегия
3 кон все кон
Слайд 73
Нарушение чувствительности
В зависимости от уровня повреждения бывают:
Рецепторные проводниковые
центральные
В зави-ости от уровня потеря чувствительности :
Полная потеря пониженная повышения
(анестезия ) (гипестезия ) (гиперстезия )
В зави-сти от вида утраченной чувствительности :
Тактильная слуховая болевая темпират
Анестезия анестезия аналгезия анастезия
Топоаналгезия
(потеря воспр-и места воздествии раздражителя )
Астереогнозия
(нару-ие целостного объемного воспра-ия свойств ошупаемого предмета )
Слайд 74
Боль
Боль представляет собой сложное психоэмоциональное неприятное ощущение,
реализующееся специальной системой болевой чувствительности и высшими отделами мозга
Систему восприятия и передачи болевого сигнала называют также ноцицептивной системой
Люди с врожденной или приобретенной (например, при травмах, инфекционных поражениях) патологией ноцицептивной системы, лишенные болевой чувствительности, не замечают повреждений, что может привести к тяжелым последствиям.
Слайд 75
Виды боли
Боль бывает
1- физиологическая : сигнализирует
о наличей повреждения в организме (адаптивное значение)
2- патологическая :
Патологическая боль имеет дезадаптивное и патогенное значение. Различные виды патологической боли проявляются в качестве характерных для нее синдромов и симптомов, которые отсутствуют при физиологической боли. Сюда относятся каузалгия, гиперпатия, первичная и вторичная гипералгезия, расширение и появление новых алгогенных рецептивных зон, персистирующая боль, спонтанные приступы боли, сохранение боли после прекращения действия провоцирующего раздражителя и другие феномены
Слайд 76
А еще бывает
1- первичная боль : острая,
локализованная , поверхностная , быстрая , проводится через
тонкие немиелизированные нервы (эпекритическая)
2- вторичная боль : глубокая , тупая , проводится через толстые миелезированные нервы (протопотическая)
Слайд 77
Медиаторы боли
Простагландин , брадекинин , гистамин , (серотанин
+ -) , субстанция Р , ионы К+ ,
лизосомальные ферменты … все они раздражают нервные окончании и вызывают боль
Почему когда трем или ложем что то холодное на месте боли , боль утихает ?? И как объяснить фантомную боль ??
Слайд 78
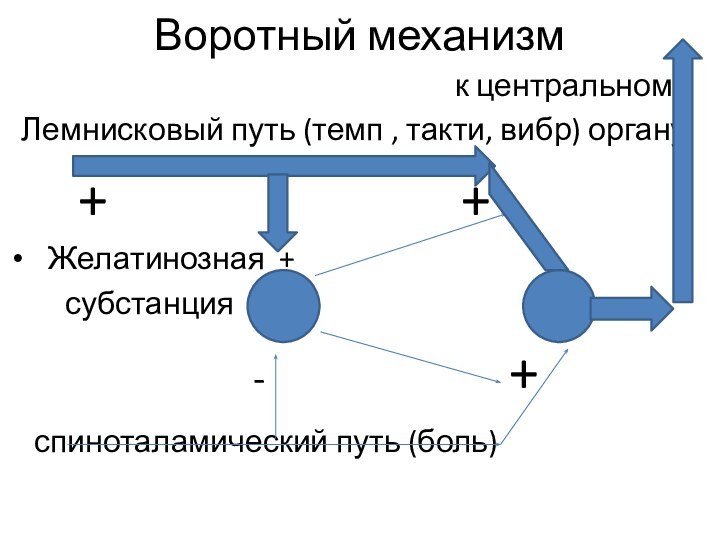
Воротный механизм
к центральному
Лемнисковый путь (темп , такти, вибр) органу
+ +
Желатинозная +
субстанция
- +
спиноталамический путь (боль)
Слайд 79
Каузалгия
Это боль возникшая из поврежденного нерва
Фантомная боль
это боль сохранившиеся на месте удаленного нерва (обычно конечность)
Слайд 80
Антиноцицептивная система
опиоидные нейропептиды (энкефалины, эндорфин , нейротензин,
холецистокинин, бомбезин, ангиотензин, вазопрессин и др. )
неопиоидные нейропептиды
(серотонин, норадреналин, допамин, ГАМК )
Вазопрессин : актевезирует желатинозную субстанцию
Слайд 81
нейроинфекций
Основные возбудители нейроинфекций: менингококки, пневмококки, гемофильная палочка инфлюэнцы,
стафилококки, синегнойная палочка, ишерихия коли, бета стрептококк (у новорожденных),
возбудители столбняка, ботулизма, менингококки, вирусы – бешенства, полиомиелита, гриппа герпес-вирусы, арбовирусы, цитомегаловирусы и др.; простейшие, прионы.
Слайд 82
Пути поступления инфекционных агентов в ЦНС
Гематогенный
Наиболее распространенный, агенты
попадают через артериальные сосуды или ретроградно через анастомозы вен
лица и церебральных сосудов
Прямое поступление
При открытых травмах черепа, при люмбальной пункции, при врожденных аномалиях развития (менингомиелоцеле)
Распространение из очага инфекций
Гайморит, фронтит, мастоидит, кариес зубов, остеомиелит костей черепа
По нервным проводникам
Возбудители столбняка, герпес-вирусы
Слайд 83
Патогенез повреждения нервной системы при нейроинфекциях:
1- Прямое повреждение
нейронов, микроглии
2- Опосредованное повреждение токсинами микроорганизмов, БАВ, высвобождаемых
при воспалительном ответе
3- Аутоиммунное повреждение
Слайд 84
Менингиты
воспаление оболочек головного и спинного мозга
Лептоменингит
– воспаление мягкой и паутинной оболочки
Пахименингит –
воспаление твердой мозговой оболочки
Возбудители менингита: менингококки- Neisseria meningitidis (30-74%), пневмококки (Streptococcus pneumoniae), гемофильная палочка инфлюэнцы (Haemophilis influenzae), стафилококки, синегнойная палочка, микобактерия туберкулеза (хронический менингит); у новорожденных- ишерихия коли, бета-гемолитический стрептококк
Слайд 85
Патогенез менингита при бактериальной инфекции
Бактерии
↓
колонизация бактерий в носоглотке
и инвазия слизистой оболочки (многие бактерии выделяют протеазы, разрушающие
IgА и преодолевают защитный барьер)
↓
Поступление бактерий в кровоток (покрытые капсулой бактерии устойчивы к фагоцитозу и комплемент-зависимому цитолизу; дефицит компонентов комплемента, спленэктомия способствуют бактериемии)
↓
Бактериемия и повреждение эндотелия капилляров мозга→ повышение проницаемости гематоэнцефалического барьера и проникновение бактерий в субарахноидальное пространство
↓
Развитие воспаления
↓
Отек мозга, повышение внутричерепного давления, сдавление сосудов мозга и нарушение кровообращения
Слайд 86
В развитии отека мозга при менингите имеют значение
: увеличение проницаемости сосудов под действием медиаторов воспаления, токсическое
воздействие на структуры мозга продуктов бактерий и лизосомальные ферменты нейтрофилов, затруднение оттока цереброспинальной жидкости, развитие васкулита сосудов мозга с последующим затруднением оттока крови.
(я) а еще , усиление выработки АДГ
Слайд 87
для всех форм менингита характерно наличие симптомов,
объединяемых в менингеальный синдром – синдром раздражения мозговых оболочек