Слайд 2
СТАРЫЕ И НОВЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ МОЧИ. НЕДОСТАТКИ И

ПРЕИМУЩЕСТВА (обзор) В последние десятилетия достигнуты значительные успехи в
развитии нефрологии. Во многом это связано с прогрессом базисных наук - биологии, физики, химии. Внедрение в нефрологию достижений физиологии, генетики, иммунологии, электронной микроскопии привело к пересмотру сохранявшихся многие годы этиологических и патогенетических концепций, классификаций и т. д. Основным принципом диагностической тактики в нефрологии должна стать оптимизация соотношения информативности исследования, его своевременности, безопасности, экономической целесообразности и реальной роли в выборе терапевтического подхода. Желание как можно быстрее установить диагноз не должно становиться поводом для избыточной диагностической активности, сильно удорожающей обследование, но не повышающей его практическую ценность. В то же время должны быть выполнены основные исследования, предусмотренные протоколами, существующими в отношении наиболее распространенных заболеваний, подозреваемых у данного больного. Обилие новой информации в диагностике заболеваний почек требует обобщения, доступной не только специалисту-нефрологу, но и врачам широкого профиля, представителям смежных клинических дисциплин 1-4. Поэтому цель данной статьи: помочь студентам, практическому врачу быстро ориентироваться в сложных вопросах нефрологии. Одним из наиболее важных исследований при подозрении на заболевание почек является общий анализ мочи
Слайд 3
При клиническом исследовании мочи изучают ее физические свойства,

химический состав, производят микроскопические исследования осадка и бактериологический состав.
Это – достаточно простые и информативные методы. Также следует знать современные дорогостоящие методы с высокими диагностическими возможностями, используемые в последние годы в развитых странах (протеомика мочи) 1-4,6. Общий анализ мочи (ОАМ) – наиболее часто используемый метод. В настоящее время количественные (Аддиса-Каковского, Амбурже) и полуколичественные (Нечипоренко) пробы признаны неудобными и не имеют преимуществ перед ОАМ. Суточный сбор мочи показан только для оценки суточной протеинурии при невозможности определения протеин/креатининового коэффициента. Для проведения ОАМ необходимо исследование утренней свежевыпущенной мочи после туалета наружных половых органов, без применения стабилизаторов с целью уменьшения вероятности ошибок, связанных с бактериальным разложением и другими факторами. Можно исследовать вторую и последующие порции мочи, полученные в течение дня. Экономичным и точным методом скринингового исследования мочи является применение тест-полосок (качественный анализ).
Слайд 4
В случае отсутствия гематурии/ гемоглобинурии или лейкоцитурии, протеинурии,

глюкозурии, необходимость в микроскопическом исследовании мочи отпадает. При обнаружении
хотя бы одной из вышеуказанных патологических находок необходимы дальнейшие количественные биохимические и микроскопические исследования. Исследование мочи начинается с изучения ее физических свойств: прозрачность, цвет, запах, реакция, относительная плотность. В норме моча прозрачная. Помутнение мочи может быть вызвано солями, клеточными элементами, слизью, бактериями и т. д. Цвет нормальной мочи зависит от ее концентрации и колеблется от соломенно-желтого до янтарно-желтого. Нормальная окраска мочи зависит от присутствия в ней пигментов (урохрома и других веществ). Бледный, почти бесцветный вид моча приобретает при сильном разведении или низкой относительной плотности, при хронической почечной недостаточности, после инфузионной терапии или приема диуретиков. Наиболее яркие изменения окраски мочи связаны с появлением в ней билирубина (от зеленоватого до зеленовато-бурого цвета), эритроцитов в большом количестве (от цвета мясных помоев до красного), измененных в кислой и гиперосмолярной среде мочи. Мутной моча может быть вследствие присутствия в ней лейкоцитов, бактерии, солей, липидов.
Слайд 5
Молочно-белый цвет отмечается при хилурии – массивной лимфоцитурии

при аномальном дренировании лимфатических сосудов в мочевыводящий тракт. Определенную
окраску моче могут придавать пищевые ингредиенты. Так, например, свекла окрашивает мочу в красный цвет, что иногда ложно трактуется как гематурия. При необычной окраске мочи следует проанализировать влияние на ее цвет медикаментозных препаратов. Запах мочи обычно нерезкий, специфический. При разложении мочи бактериями появляется аммиачный запах. При наличии кетоновых тел (ацетонемический криз, сахарный диабет) моча приобретает запах ацетона. При врожденных нарушениях метаболизма запах мочи может быть очень специфическим (мышиным, кленового сиропа, хмеля, кошачьей мочи, гниющей рыбы и т. д.). Реакция мочи в норме кислая или слабокислая, колеблется в пределах 5,5 до 8,0 и зависит от степени разведения мочи. Она может быть щелочной из-за преобладания в рационе овощной диеты, приема щелочных минеральных вод, после обильной рвоты, воспаления почек, при заболеваниях мочевыводящих путей, гипокалиемии. Постоянно щелочная реакция бывает при наличии фосфатных камней. рН мочи имеет клиническое значение при нарушениях кислотно-щелочного равновесия и механизмах камнеобразования.
Слайд 6
Относительная плотность мочи отображает активность процессов концентрирования мочи

и варьирует в зависимости от количества принимаемой жидкости в
пределах 105-1035. Наличие постоянно низкой относительной плотности мочи (1006-1010) является значимым отклонением и может быть первым признаком серьезного заболевания, к примеру нефронофтиза, хронической почечной недостаточности. Раннее проводимый тест на разведение мочи (водная нагрузка) сейчас не используется из-за опасности водной интоксикации. Но его применение оправдано при подозрении на несахарный диабет. Рутинным образом относительная плотность мочи может быть измерен непосредственно урометром, либо более просто, рефрактометром (охватывает значения до 1032). Ложно завышенные результаты наблюдаются, если моча содержит белок, глюкозу или рентгенконтрастные средства. Определение концентрационной функции канальцев зачастую требует повторных исследований, иногда с ограничением жидкости, однако если изначально хотя бы в одной порции мочи относительная плотность превышает 1020, нет необходимости в повторном исследовании или назначения пробы Зимницкого.
Слайд 7
Наиболее точным методом является измерение осмоляльности мочи криоскопическим

методом. Осмоляльность мочи колеблется в пределах 800-1400мосм/кг, тогда как
плазмы – 280-300 мосм/кг. Определение осмоляльности является точным методом оценки концентрационной функции, особенно важен при полиурически-полидипсическом синдроме. Химический состав мочи. В моче может находиться более 150 компонентов. Количественное определение нормальных составных частей мочи – экскреции мочевины, мочевой кислоты, креатинина, натрия, калия, хлора, магния, фосфора, глюкозы и аминокислот - важно для изучения функции проксимальных канальцев почек, что позволят выявить нарушений обмена веществ (тубулопатии). Протеинурия – один из главных признаков заболевания почек, маркер локализации и тяжести почечного повреждения. Однако следует помнить, что при таких состояниях, как лихорадка, значительная физическая нагрузка, длительная артериальная гипертония (гипертоническая нефропатия), диабетическая нефропатия, сердечная недостаточности, может иметь место транзиторное (преходящее) повышение альбумина в моче (до 0,033 г/л белка в разовых порциях мочи или 30-50 мг/сут в суточной). Патологическая протеинурия может колебаться от слабо выраженной (150-500 мг/сут), характерной для гломерулопатии до выраженной (более 2000 мг/сут или 3,0 г/с) – для гломерулопатии с нефротическим синдромом. В норме с мочой выделяются различные белки (альбумин, глобулин и др.), количество которых незначительно.
Слайд 8
Суточная протеинурия в норме не превышает 150 мг/сут.

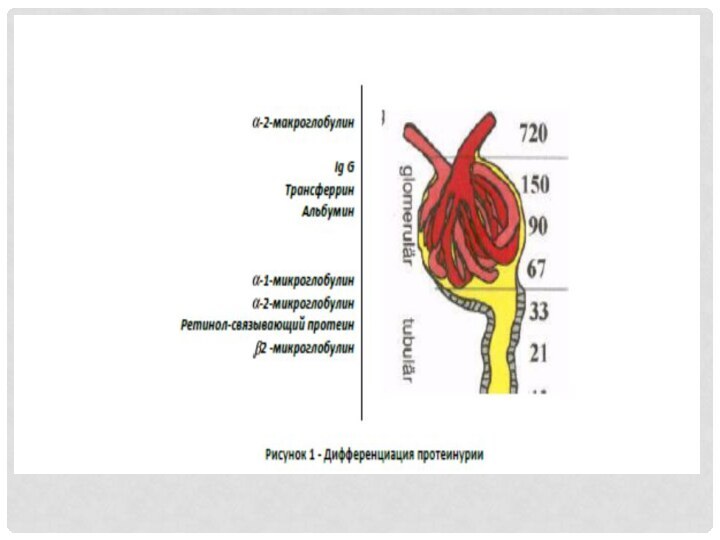
Рутинные методы исследования (тест-полоски, проба с сульфосалициловой кислотой) не
выявляют выделяющиеся в норме белки. При патологии уровень протеинурии растет. Поэтому диагностическое значение имеет определение суточного количества белка в моче, а также электрофоретическая дифференциация видов белка (альбумин, α1, α2 -микроглобулин, β2-микроглобулин, белок Тамма-Хорсфаля и др.). Для определения суточной протеинурии собирают суточную мочу и производят пересчет концентрации белка в моче (г/л) на суточный диурез (г/сут). Более удобен новый метод вычисления протеин/креатининового коэффициента, который позволяет определить суточную экскрецию белка без сбора 24-часовой мочи. Принцип основан на том, что креатинин выделяется путем клубочковой фильтрации и экскреция его постоянна в течение суток. С помощью вычисления отношения концентрации любого вещества (включая белок) в моче к уровню креатинина в моче, можно определить суточную экскрецию этих веществ (Na, K, Ca и др., табл.2). Концентрация веществ и креатинина может выражаться в ммоль, мг или г/л. При расчете суточной протеинурии чаще белок определяют в мг или г, а креатинин в ммоль. Оба вещества могут определяться в г/л. В зависимости от этого протеин/ креатининовый коэффициент в норме равен: у взрослых < 11 мг/ммоль или < 0,2 (при расчете в г/л). Альбумин/креатининовый коэффициент у взрослых < 2,3 мг/ммоль 3-8. Нормы протеинурии у детей представлены в таблице 1.
Слайд 11
В моче содержатся белки и неплазменного происхождения. 50%
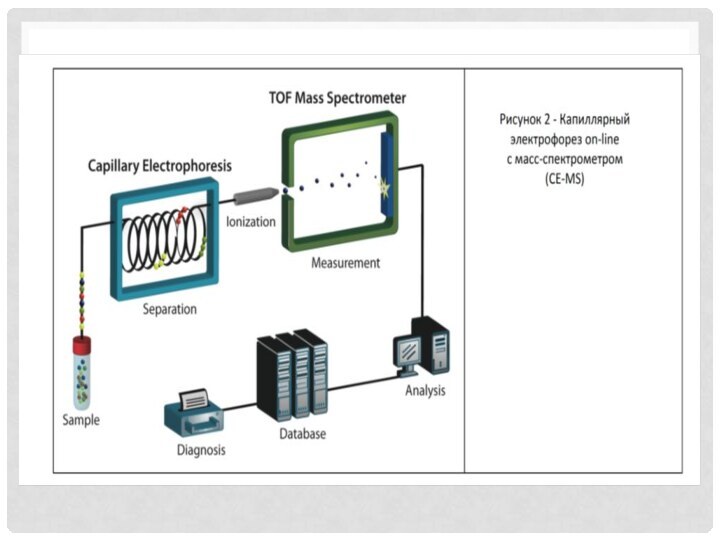
всех белков мочи образуется в мочевыводящем тракте, основным из
которых является белок Тамма-Хорсфалля. Наиболее точными являются новые технологии электрофореза - нефелометрические методы определения белков-маркеров (альбумин, α1-микроглобулин и др.). Этот, пока малодоступный и дорогой метод, позволяет быстро дифференцировать гломерулярную и тубулярную дисфункции, отдельно выявляя альбумин и α-микроглобулин. С недавнего времени, используемый в развитых странах протеомный анализ мочи (протеомика), предоставил возможность дальнейшего совершенствования неинвазивных методов диагностики заболеваний почек (рисунок 2) 3-4 .
Слайд 13
Внедрение этого дорогостоящего метода в будущем позволит дифференцировать

такие болезни, как Ig A нефропатия, фокально-сегментарный гломерулосклероз без
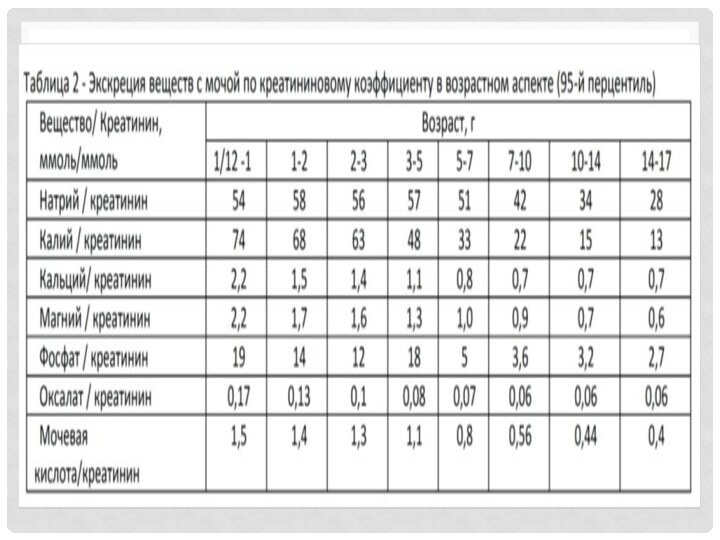
биопсии почек. При заболеваниях почек, связанных с гематологическими, онкологическими болезнями, увеличивается экскреция парапротеинов с мочой. Парапротеины появляются в избыточном количестве при множественной миеломе, амилоидозе, макроглобулинемии Вальденстрема (протеинурия переполнения). Одним из них является белок Бенс-Джонса. Он не определяется обычными тест-полосками и требует специального исследования легких цепей иммуноглобулинов. Свойством белка Бенс-Джонса является осаждение при термической обработке сульфосалициловой кислотой. Экскреция химических веществ в моче. Также определяется с использованием креатининового коэффициента (КК). Уровень экскреции химических веществ с мочой зависит от возраста детей и для правильной оценки рекомендуется руководствоваться нормативами (таблица 2). Большинство детей старше 2-х лет при нормальном питьевом режиме имеют уровень креатинина мочи 5±4 ммоль/л. Может быть ошибка «разведения мочи», когда креатинин мочи составляет около 2 ммоль/л или «концентрирования мочи» при концентрации около 12 ммоль/л. При концентрации альбумина в моче 1 г/л, то есть при 50-кратном его повышении, расчет КК не требуется. КК всех веществ у грудных детей выше, чем у старших детей. Это связано не с повышенной их экскрецией, а со сниженной экскрецией креатинина из-за малой мышечной массы. Норма КК у новорожденных детей в 4 раза выше, чем у старших детей. При определении КК необходимость в определении суточной экскреции веществ отпадает.
Слайд 15
Для правильной интерпретации экскреции электролитов (Na, K, Ca,

Mg, Cl, P) с мочой важно знать их уровни
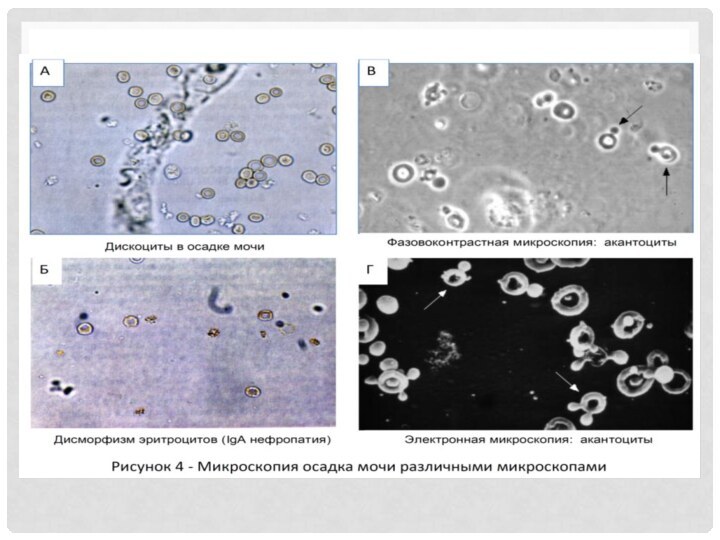
в сыворотке крови и суточный прием. Глюкозурия обычно свидетельствует о гипергликемии, однако может носить и изолированный характер (почечная глюкозурия) или сочетаться с нарушениями других функций проксимальных почечных канальцев (синдром Фанкони). Глюкозурия иногда встречается при нефротическом синдроме и на фоне стероидной терапии. Микроскопия мочи. Микроскопия мочи позволяет дифференцировать эритроцитурию от гемо,- миоглобинурии. Гематурия – частый симптом и может встречаться при многих заболеваниях: от тяжелых (гломерулонефрит) до доброкачественной гематурии у детей. В норме эритроциты в моче отсутствуют или могут быть не более 3-5 в поле зрения. Различают следующие клинические варианты гематурии: бессимптомная микрогематурия, макрогематурия, микрогематурия с протеинурией >0,5 г/л. Немаловажное практическое значение имеет дифференцирование ренальной (гломерулярной) и экстраренальной гематурии. Помимо клинических симптомов, для этого исследуется морфология эритроцитов мочи с использованием фазово-контрастной микроскопии. Наличие дисморфных эритроцитов характерно для гломерулярной гематурии. Выявление так называемых акантоцитов, клеток Шнуллера (более 10%) безусловно свидетельствует о гломерулярной патологии (рис.3,4). Опытный нефролог может распознать дисморфные эритроциты с помощью обычного светового микроскопа при увеличении в 400 раз. Дальнейшая дифференциация дисморфных эритроцитов на подгруппы проводится в редких случаях по показаниям из-за дороговизны 4-8 .
Слайд 18
Гломерулярная гематурия диагностируется при достаточном количестве дисморфных эритроцитов

(напр. 200 эр/мл). Обнаружение эритроцитарных цилиндров в осадке мочи
свидетельствует о гломерулярной патологии и исследуется только в неясных случаях. Количественный подсчет клеток в суточной моче по методу Аддиса не удобен, не информативен вследствие ошибок сбора мочи и спонтанного разрушения клеток. Главным показателем бактериальной инфекции мочевой системы (ИМС) является лейкоцитурия. Допустимо наличие 4-6 лейкоцитов в поле зрения. Однако лейкоцитурия не всегда является следствием бактериальной ИМС. Например, стерильная лейкоцитурия может быть при тубулоинтерстициальном нефрите, нефролитиазе. При кандидозе или аденовирусной ИМС лейкоцитурия может отсутствовать. Проба Нечипоренко в данное время уже не используется, в виду того, что она не может считаться количественной, так как не учитывается время, за которое собрана моча и к тому же не имеет преимуществ перед общим анализом мочи. При микроскопическом исследовании мочи можно при необходимости дифференцировать лейкоциты по морфологии (напр. эозинофилы при интерстициальном нефрите). При бактериурии микробиологическое исследование дает более точные данные о количестве и свойствах микроорганизмов. Степень бактериурии определяют методом Гоулда. Диагностическое значение имеет бактериурия 105 м.т. в 1 мл мочи и выше. Выявление в моче грибковой флоры является основанием для постановки диагноза кандидозной ИМС.
Слайд 19
Использование дип-слайдов (Uricult) со свежевыпущенной мочой способствует правильной

диагностики инфекции в короткий срок – моча часто загрязняется,
елси ее немедленно не поместить в холодиьник или не доставить в лабораторию. Цилиндры. Гиалиновые цилиндры образуются в почечных канальцах из белка Тамма-Хорсфаля. Они быстро растворяются в щелочной среде и иногда встречаются в нормальной моче. Их количество возрастает при приеме диуретических средств, повышении температуры тела и физической нагрузке, но особенно значительно при почечной патологии. Наличие в моче зернистых и клеточных цилиндров свидетельствует о патологических изменениях в почечной паренхиме. Эритроцитарные цилиндры указывают на поражение клубочков (гломерулонефрит). Лейкоцитарные цилиндры – признак острого пиелонефрита. Количество гиалиновых цилиндров увеличивается при протеинурии. При СКВ характерен «телескопический» осадок с широким набором клеток и цилиндров. Жировые цилиндры встречаются при нефротическом синдроме, восковидные – признак ХПН (формируются при расширении канальцев почек). Скорость клубочковой фильтрации и клиренс креатинина. Наиболее точным показателем, отражающим функциональное состояние почек, является СКФ. СКФ может измеряться с применением эндогенных (инулин) и экзогенных маркеров фильтрации, рассчитываться по клиренсу эндогенных маркеров фильтрации (Cr) или по формулам, основанным на сывороточном уровне эндогенных маркеров (Cr, цистатин С) (таблица 3).
Слайд 21
Определение клиренса эндогенных и экзогенных маркеров фильтрации. Золотым

стандартом измерения СКФ является клиренс инулина, который в стабильной
концентрации присутствует в плазме, физиологически инертен, свободно фильтруется в клубочках, не секретируется, не реабсорбируется, не синтезируется, не метаболизируется в почках. Определение клиренса инулина, также как и клиренса экзогенных радиоактивных меток (125I-иоталамата и 99mTc-DTPA) дорогостояще и труднодоступно в рутинной практике. Разработан ряд альтернативных методов оценки СКФ. Проба Реберга-Тареева. Измерение 24-часового клиренса Cr (проба Реберга-Тареева) требует сбора мочи за определенный промежуток времени, что часто сопровождается ошибками и обременительно для пациента. Кроме того, данный метод оценки СКФ не имеет преимуществ в сравнении с расчетом СКФ по формуле. Исключением является определение СКФ у лиц с необычной диетой или отклонениями в мышечной массе, поскольку эти факторы не принимались во внимание при разработке формул. Кроме того, использование Cr сыворотки для оценки СКФ предполагает наличие стабильного состояния пациента. Поэтому результаты будут ненадежными, если уровень СКФ быстро меняется (при острой почечной недостаточности), если мышечная масса необычно велика или мала (у атлетов или истощенных лиц), или если потребление креатина с пищей необычно велико или мало (у лиц, употребляющих пищевые добавки с креатином или у вегетарианцев).
Слайд 22
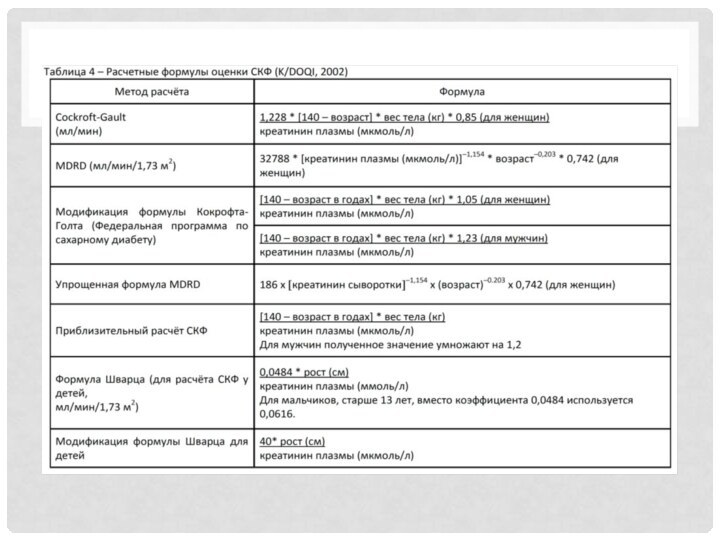
Расчётные формулы оценки СКФ. Расчет СКФ являются лучшим

общим показателем уровня функции почек. Формулы для расчета СКФ
учитывают различные влияния на продукцию Cr, они просты в применении, валидированы. Стандартизация СКФ по площади поверхности тела полезна у детей и является общепринятой практикой у взрослых. Точность всех измерений СКФ, основанных на сборе мочи зависит от его точности. Неточности могут быть связаны с неполным опорожнением мочевого пузыря перед началом периода сбора мочи, неполным сбором мочи за весь период и отклонениями в продолжительности сбора. В теории ошибки можно минимизировать, если тщательно проинструктировать больного и повторить сбор дважды. Для того чтобы избежать этих трудностей на практике, разработаны формулы для оценки СКФ или клиренса креатинина по уровню креатинина плазмы, возрасту, полу и массе тела. На сегодняшний день широкое распространение получили простые расчётные методы оценки СКФ: у взрослых - формула из исследования MDRD и формула Кокрофта-Голта (Cockcroft-Gault), у детей - формулы Шварца (Schwartz) и Кунаха-Барра (Counahan-Barratt), норма СКФ 90-130 мл/мин (таблица 4).
Слайд 24
Креатинин так и не был замещен другим показателям

для оценки СКФ. К сожалению, методики и нормальные значения
существенно варьируют от лаборатории к лаборатории. Альтернативой является анализ на содержание цистатина С. В качестве альтернативного маркера функционального состояния почек и сердечно-сосудистого риска в последние годы рассматривается цистатин С, белок с низкой молекулярной массой, ингибитор протеаз. Цистатин С характеризуется свободной клубочковой фильтрацией, не подвергается канальцевой секреции. Его преимущество в том, что значения не зависят от мышечной массы, как при определении уровня креатинина. На сегодняшний день разрабатываются формулы для расчета СКФ на основании уровня цистатина С. Таким образом, путь к точному диагнозу - это не простое проведение серии обследований и констатация их результатов, а создание диагностической концепции, включающей этиологические и патогенетические особенности заболевания у конкретного больного. Несмотря на значительное развитие диагностических тестов, и исследований, очень многое может быть достигнуто с помощью простых методов, при условии их правильного применения, однако в определенных случаях необходимо применять самые современные и технологические методики. Важен учет таких факторов, как наибольшая информативность, современность, безопасность и стоимость предполагаемого метода исследования. В каждом конкретном случае поэтапное применение методов исследования с использованием алгоритмов облегчает диагностику того или другого заболевания.