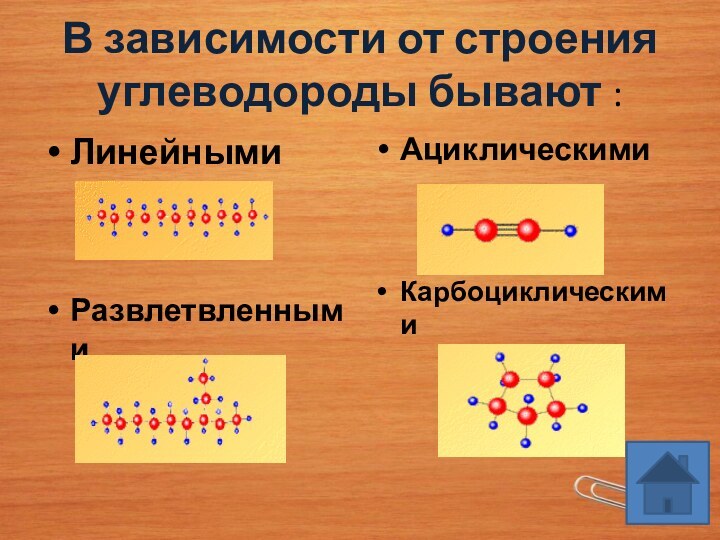
Уже название этого класса веществ является описанием их качественного состава:
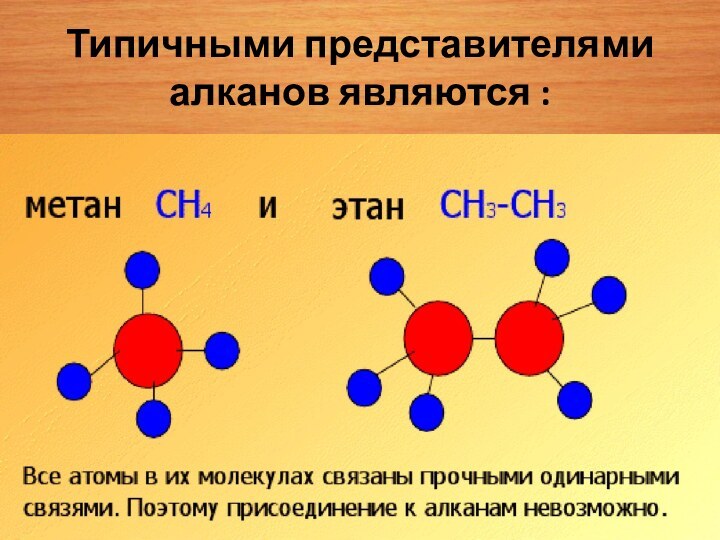
Углеводороды – вещества, состоящие из атомов углерода и атомов водорода.
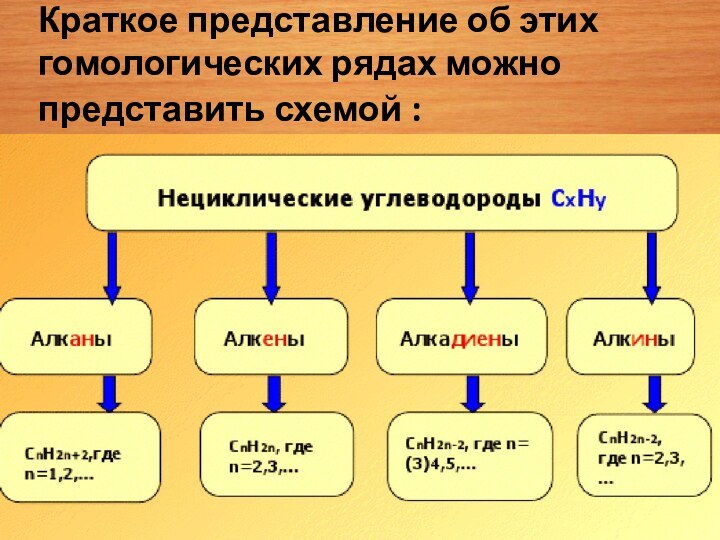
Общая формула : СxHY
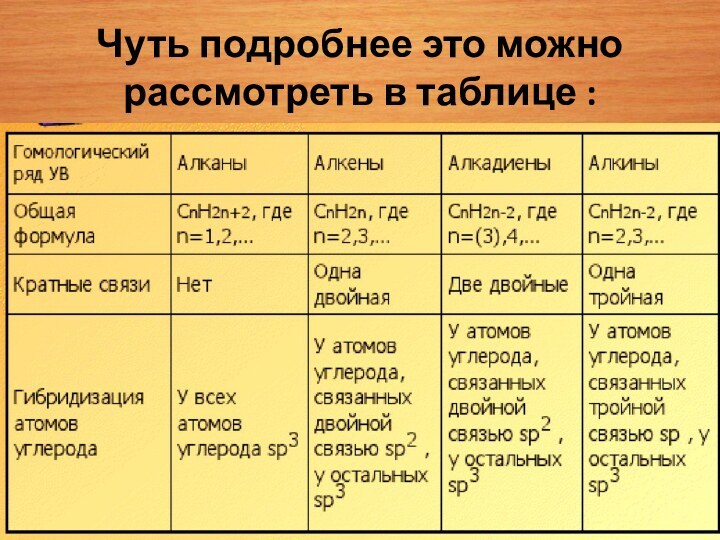
Соотношение между количеством атомов углерода и количеством атомов водорода разное в разных гомологических рядах углеводородов.