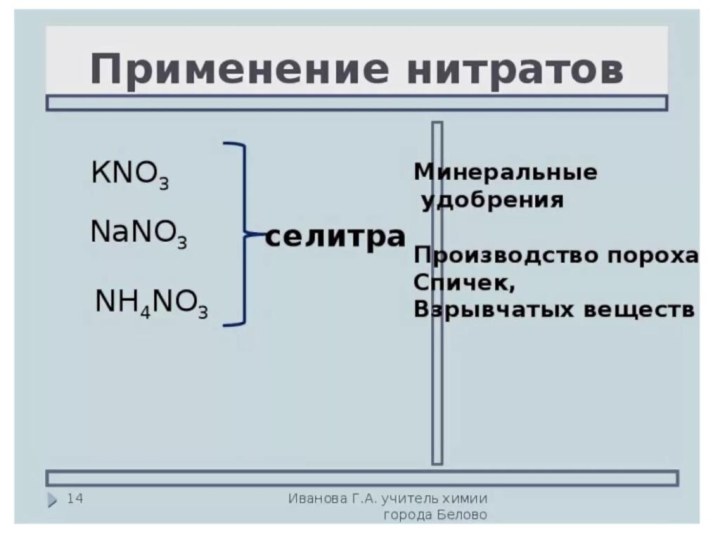
NaNO3 – натриевая селитра (чилийская), KNO3 – калийная селитра
(индийская), Са(NO3)2 – кальциевая селитра (норвежская),NH4NO3 – аммиачная селитра.)
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть







2HNO3 + Na2CO3 = 2NaNO3 + H2O + CO2 ↑
6) Оксид азота (IV) + щёлочь
2NO2 + NaOH = NaNO2 + NaNO3 + H2O
в присутствии кислорода -
4NO2 + O2 + 4NaOH = 4NaNO3 + 2H2O