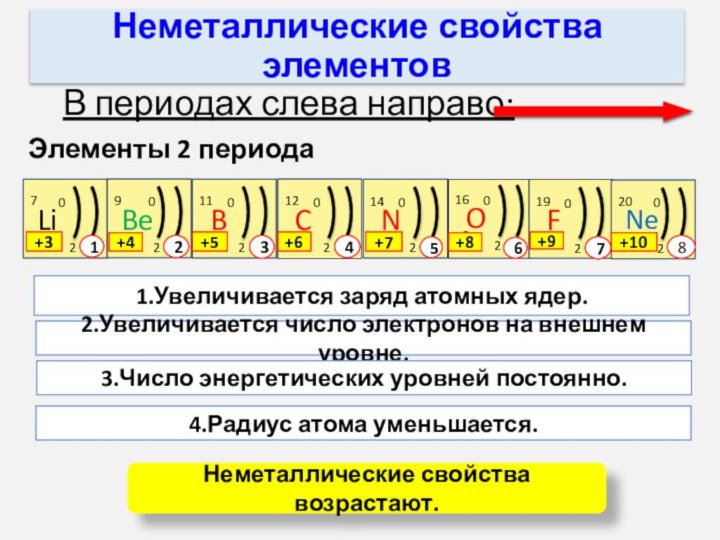
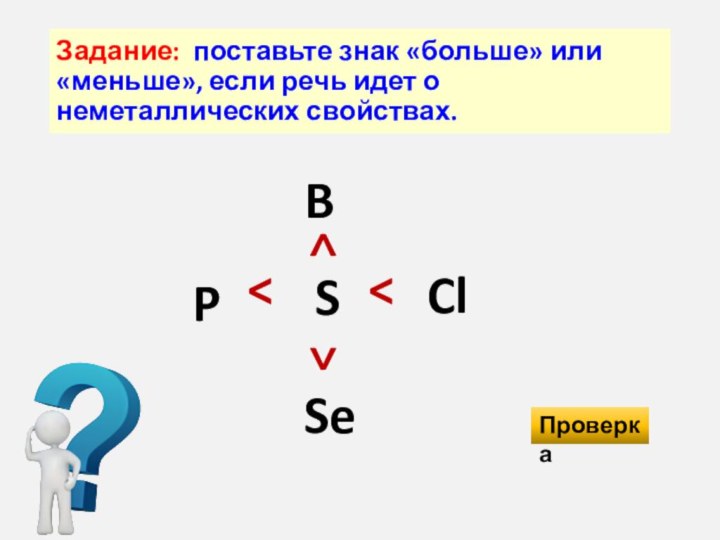
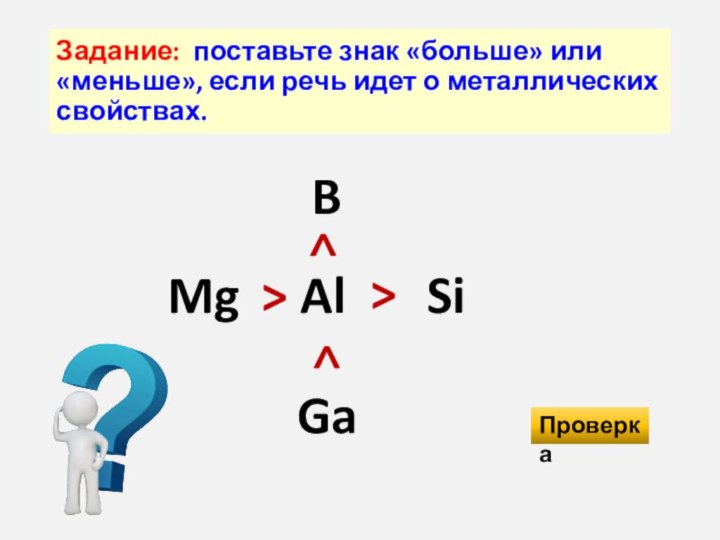
неметаллические свойства_________________, потому что:
а)_______________________________________
б)___________________________________________________
в)________________________________________
г)________________________________________
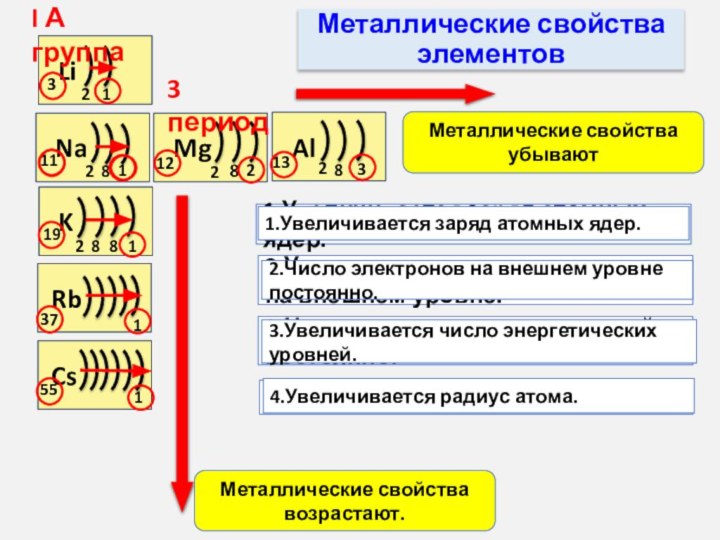
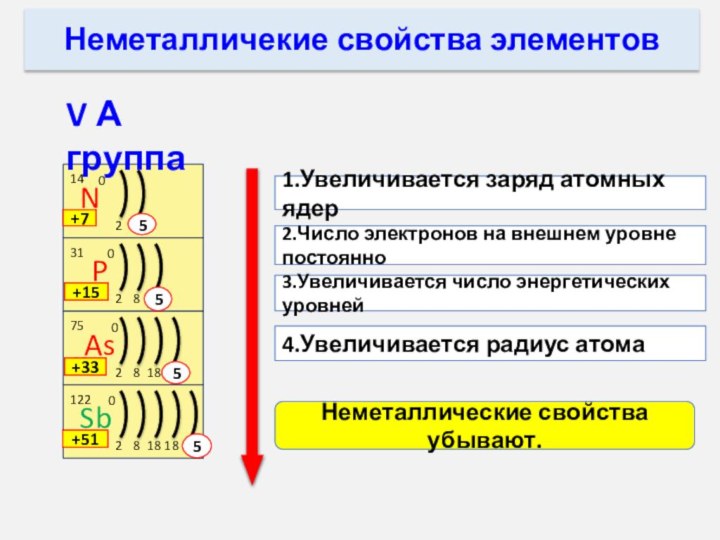
В А группе сверху вниз:
металлические свойства____________________
а
неметаллические свойства_________________, потому что:
а)___________________________________
б)____________________________________________________
в)____________________________________________________
г)_____________________________________
убывают
возрастают
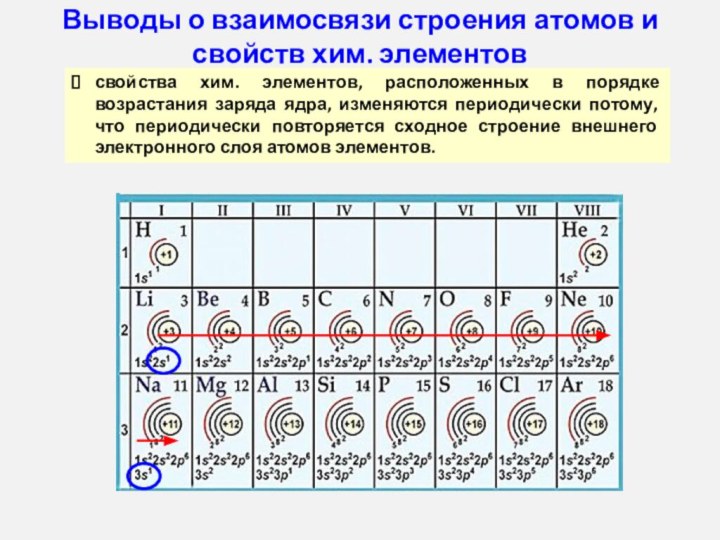
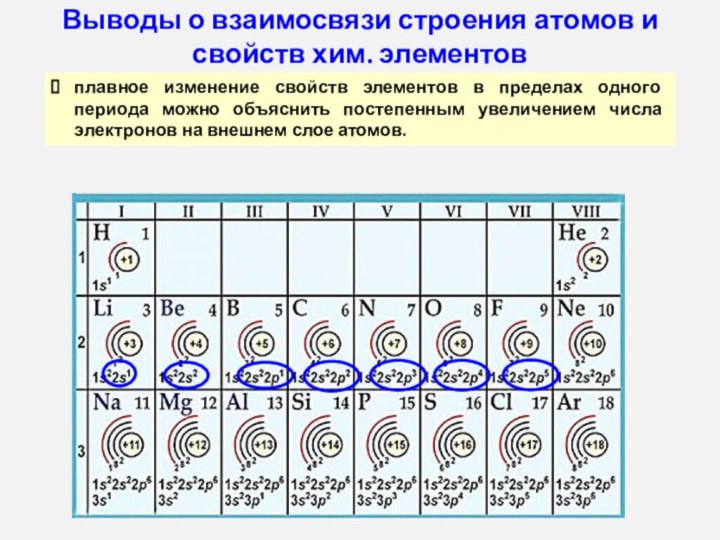
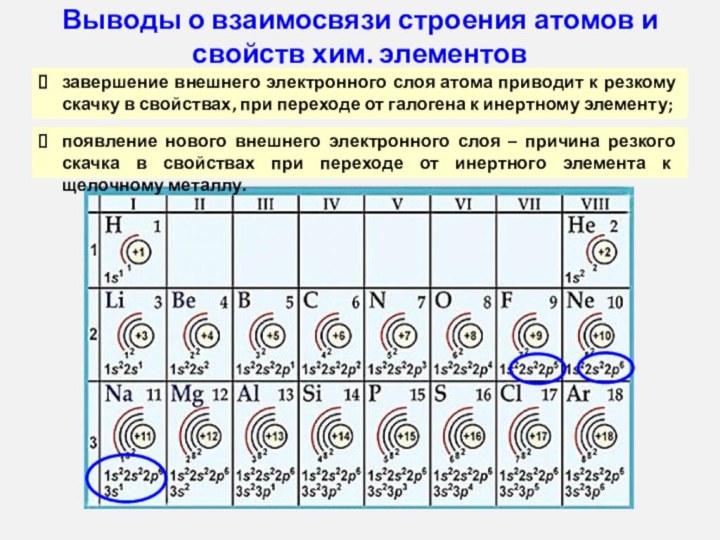
увеличивается заряд атомных ядер
увеличивается число электронов на внешнем уровне
число энергетических уровней постоянно
радиус атома уменьшается
возрастают
убывают
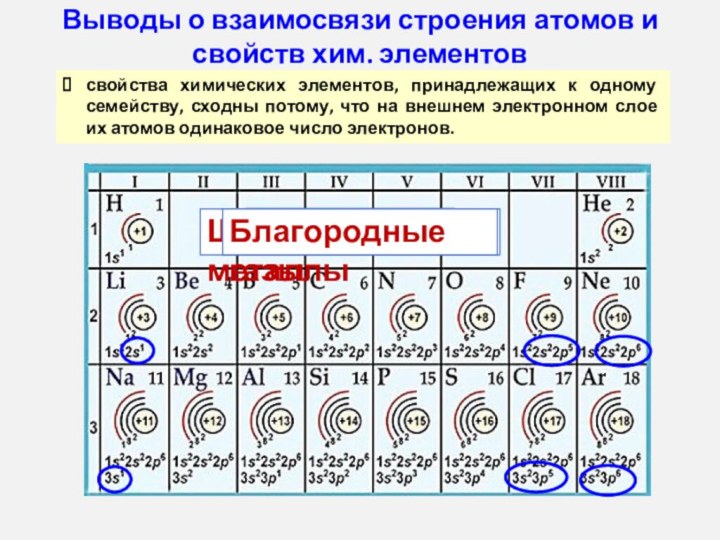
увеличивается заряд атомных ядер
число электронов на внешнем уровне постоянно
увеличивается число энергетических уровней
радиус атома увеличивается
Проверка