Слайд 2
Содержание:
Физические свойства
Строение
История открытия
Способы получения
Применение
Химические свойства
Номенклатура Номенклатура и изомерия Номенклатура и
изомерия, Классификация и состав
Вопросы для проверки
Использованная литература
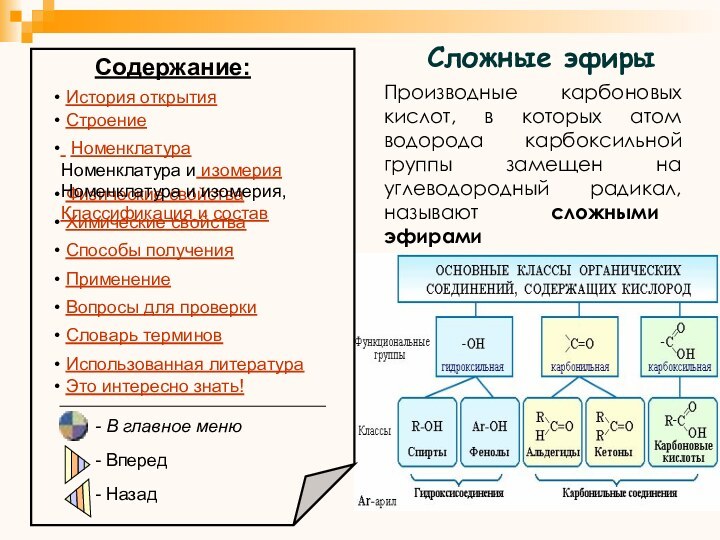
Сложные эфиры
Производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен на углеводородный радикал, называют сложными эфирами
- В главное меню
- Вперед
- Назад
Словарь терминов
Это интересно знать!
Слайд 3
Открытие сложных эфиров
Первооткрывателем сложных эфиров является русский академик
Тищенко Вячеслав Евгеньевич (1861-1941). В 1899 году разработал способ
получения алкоголята алюминия. В 1906 году открыл реакцию сложноэфирной конденсации, или диспропорционирование альдегидов с образованием сложных эфиров под воздействием алкоголятов алюминия.
Слайд 4
Тищенко Вячеслав Евгеньевич
Тищенко Вячеслав Евгеньевич (1861-1941). Советский химик-органик,
академик АН СССР(1935). Основная область его работы – органическая
химия и лесохимия. Написал труды по органическому синтезу, химии терпенов. Открыл реакцию конденсации альдегидов жирного ряда(1906), или реакция Тищенко. Предложил промышленный способ получения камфоры из скипидара. Также предложил новый тип склянок для промывания и просушки газов (склянки Тищенко) .
Участвовал в изучении Кольских апатитов. Под его руководством разработаны способы получения многих химически чистых реактивов. Также изучал состав нефти и отдельных нефтяных фракций (1890). Занимался Государственными проектами СССР (1945).
Слайд 5
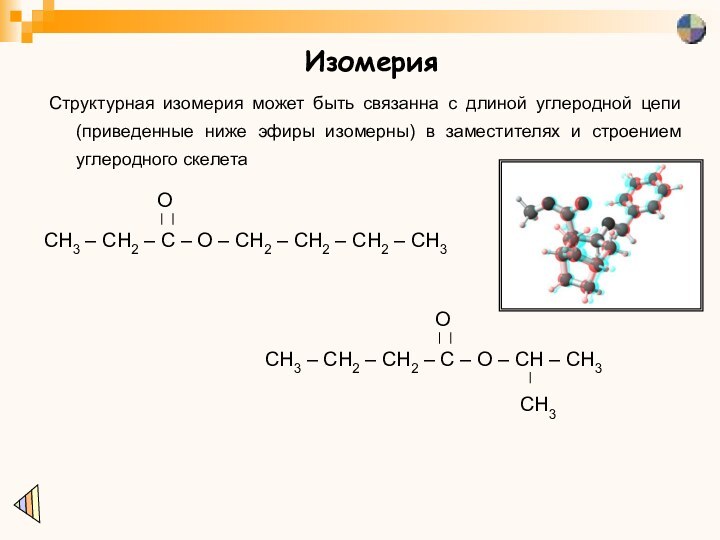
Изомерия
Структурная изомерия может быть связанна с длиной углеродной
цепи (приведенные ниже эфиры изомерны) в заместителях и строением
углеродного скелета
Слайд 6
Номенклатура
Общую формулу сложных эфиров можно представить в виде
RCOOR’, где R и R’ – углеводородные радикалы (для
эфиров муравьиной кислоты R – атом водорода). Широко используют несколько типов названий сложных эфиров. Самые длинные происходят от названия соответствующий кислоты с указанием углеводородного заместителя, например, бутиловый эфир уксусной кислоты, изопропиловый эфир масляной кислоты. В русском языке приняты названия, состоящие из двух слов: уксуснобутиловый эфир, масляноизопропиловый
Слайд 7
Классификация и состав сложных эфиров
Когда число атомов С
в исходных карбоновой кислоте и спирте не превышает 6–8,
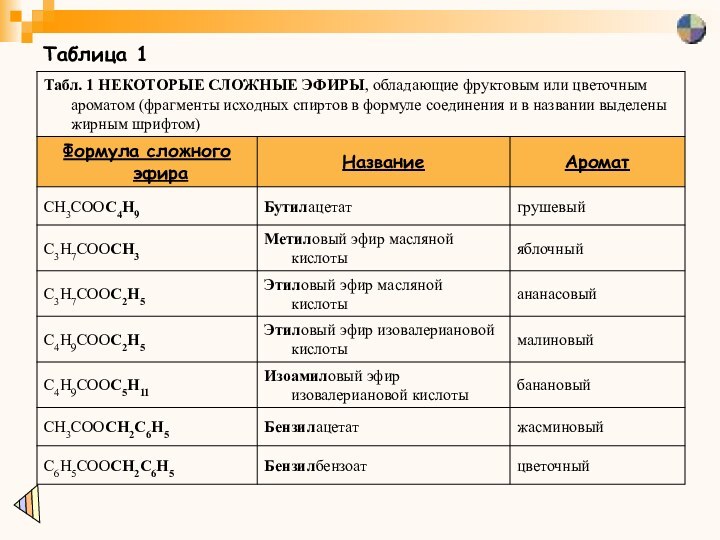
соответствующие сложные эфиры представляют собой бесцветные маслянистые жидкости, чаще всего с фруктовым запахом. Они составляют группу фруктовых эфиров. Если в образовании сложного эфира участвует ароматический спирт (содержащий ароматическое ядро), то такие соединения обладают, как правило, не фруктовым, а цветочным запахом. Все соединения этой группы практически нерастворимы в воде, но легко растворимы в большинстве органических растворителей. Интересны эти соединения широким спектром приятных ароматов (см. табл. 1), некоторые из них вначале были выделены из растений, а позже синтезированы искусственно.
Продолжение темы –
Слайд 8
При увеличении размеров органических групп, входящих в состав
сложных эфиров, до С15–30 соединения приобретают консистенцию пластичных, легко
размягчающихся веществ. Эту группу называют восками, они, как правило, не обладают запахом.
Классификация и состав сложных эфиров
Искусственный воск
Продолжение темы –
Слайд 9
Третья группа – жиры. В отличие от предыдущих
двух групп на основе одноатомных спиртов ROH, все жиры
представляют собой сложные эфиры, образованные из трехатомного спирта глицерина НОСН2–СН(ОН)–СН2ОН. Карбоновые кислоты, входящие в состав жиров, как правило, имеют углеводородную цепь с 9–19 атомами углерода.
Классификация и состав сложных эфиров
Слайд 10
Липиды
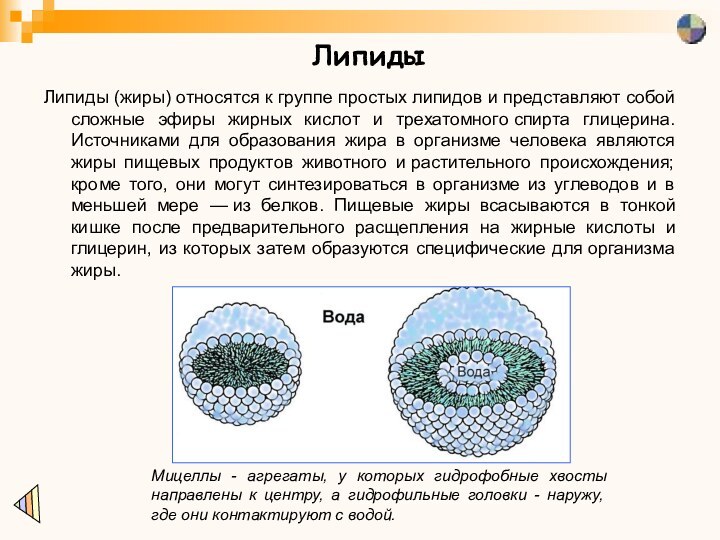
Липиды (жиры) относятся к группе простых липидов и
представляют собой сложные эфиры жирных кислот и трехатомного спирта глицерина.
Источниками для образования жира в организме человека являются жиры пищевых продуктов животного и растительного происхождения; кроме того, они могут синтезироваться в организме из углеводов и в меньшей мере — из белков. Пищевые жиры всасываются в тонкой кишке после предварительного расщепления на жирные кислоты и глицерин, из которых затем образуются специфические для организма жиры.
Мицеллы - агрегаты, у которых гидрофобные хвосты направлены к центру, а гидрофильные головки - наружу, где они контактируют с водой.
Слайд 11
Воска
Воска - сложные эфиры одиночных жирных кислот и
одноатомных спиртов с длинной углеводородной цепочкой.
Пчелиный воск содержит смесь
различных сложных эфиров, один из компонентов воска, который удалось выделить и определить его состав, представляет собой мирициловый эфир пальмитиновой кислоты C15H31COOC31H63. Китайский воск (продукт выделения кошенили – насекомых Восточной Азии) содержит цериловый эфир церотиновой кислоты C25H51COOC26H53. Кроме того, воски содержат и свободные карбоновые кислоты и спирты, включающие большие органические группы. Воски не смачиваются водой, растворимы в бензине, хлороформе, бензоле.
Молекула воска
Слайд 14
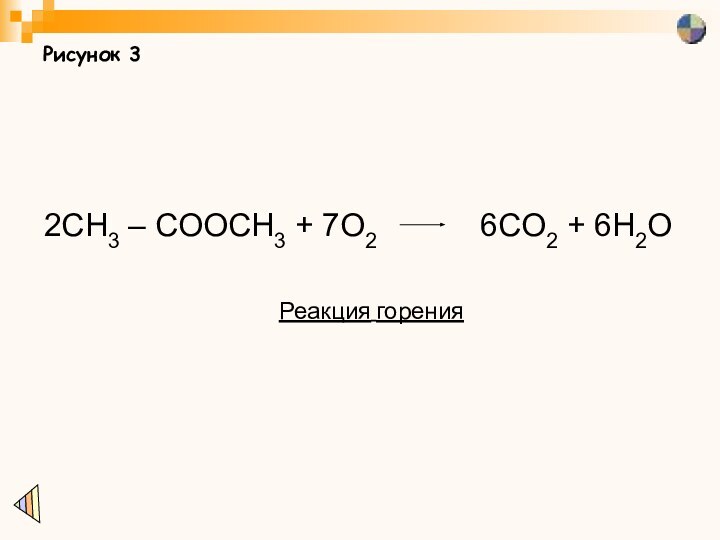
Рисунок 3
2CH3 – COOCH3 + 7O2
Реакция горения
Слайд 18
Применение сложных эфиров
Этилформиат НСООС2Н5 и этилацетат Н3СООС2Н5 используются
как растворители целлюлозных лаков.
Сложные эфиры на основе низших спиртов
и кислот (табл. 1) используют в пищевой промышленности при создании фруктовых эссенций, а сложные эфиры на основе ароматических спиртов – в парфюмерной промышленности.
Из восков изготавливают политуры, смазки, пропиточные составы для бумаги (вощеная бумага) и кожи, они входят и в состав косметических кремов и лекарственных мазей.
Продолжение темы –
Жиры вместе с углеводами и белками составляют набор необходимых для питания пищевых продуктов, они входят в состав всех растительных и животных клеток, кроме того, накапливаясь в организме, играют роль энергетического запаса. Входя в состав жиров, предохраняют от обморожения. Животные и растительные жиры представляют собой сырье для получения высших карбоновых кислот, моющих средств и глицерина, используемого в косметической промышленности и как компонент различных смазок.
Слайд 19
Нитроглицерин – известный лекарственный препарат и взрывчатое вещество,
основа динамита.
На основе растительных масел изготавливают олифы, составляющие
основу масляных красок.
Эфиры серной кислоты используют в органическом синтезе как вводящие в соединение алкильную группу реагенты, а эфиры фосфорной кислоты – как инсектициды, а также добавки к смазочным маслам.
Применение сложных эфиров
Продолжение темы –
Слайд 20
Применение сложных эфиров
Продолжение темы –
Машинное масло на
основе сложных эфиров. Разработано для 2-х тактных двигателей большой
мощности.
На основе жиров создаются медицинские препараты, а также тестостероны. Тестостерон «Энантат» - сложный эфир естественного тестостерона...
Слайд 21
Применение сложных эфиров
Новый антифог на основе сложных эфиров
глицерина разработан специально для пленок, которые применяются в производстве
упаковочных материалов. Степень полимеризации глицерина может варьироваться, а фракции с заданным молекулярным весом отделяются и направляются на этерификацию.
Одним из уникальных продуктов, применяемых нашей фирмой, являются метилметакрилатные смолы (ММА), основанные на акриловых и метакриловых сложных эфирах, активная группа которых имеет двойную композицию С=С.
Слайд 22
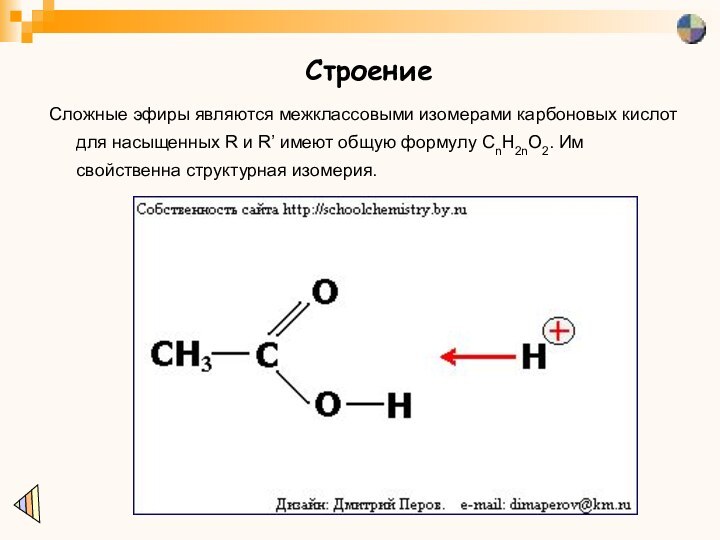
Строение
Сложные эфиры являются межклассовыми изомерами карбоновых кислот для
насыщенных R и R’ имеют общую формулу CnH2nO2. Им
свойственна структурная изомерия.
Слайд 23
Физические свойства
Сложные эфиры низших карбоновых кислот представляют собой
летучие жидкости, многие из которых обладают приятным цветочным или
фруктовым запахом (см. табл.1). Они практически нерастворимы в воде и имеют более низкие температуры кипения, чем изомерные им карбоновые кислоты. Это связанно с тем, что в молекулах сложных эфиров отсутствуют межмолекулярные водородные связи.
Свойства жиров
Свойства восков
Слайд 24
Химические свойства
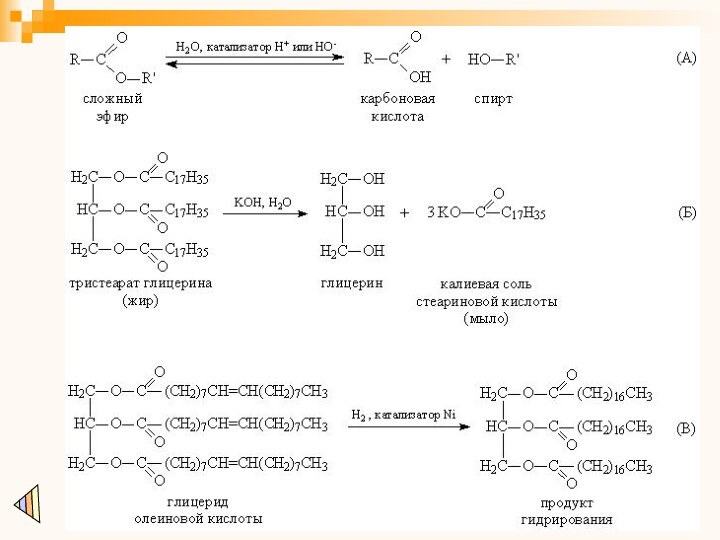
Наиболее характерно для эфиров карбоновых кислот гидролитическое
(под действием воды) расщепление сложноэфирной связи, в нейтральной среде
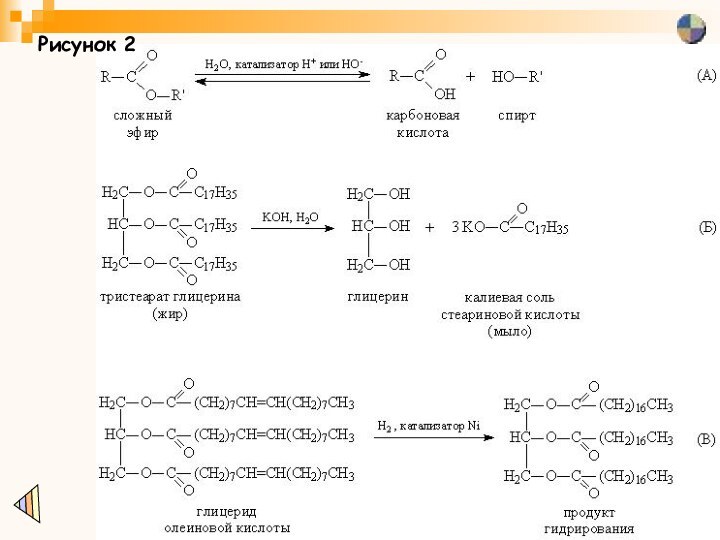
оно протекает медленно и заметно ускоряется в присутствии кислот или оснований, т.к. ионы Н+ и НО- катализируют этот процесс (рис. 2А), причем гидроксильные ионы действуют более эффективно. Гидролиз в присутствии щелочей называют омылением. Если взять количество щелочи, достаточное для нейтрализации всей образующейся кислоты, то происходит полное омыление сложного эфира. Такой процесс проводят в промышленном масштабе, при этом получают глицерин и высшие карбоновые кислоты (C15-19) в виде солей щелочных металлов, представляющих собой мыло (рис. 2Б).
Продолжение темы –
Слайд 25
Химические свойства
Содержащиеся в растительных маслах фрагменты ненасыщенных кислот,
как и любые ненасыщенные соединения, могут быть прогидрированы, водород
присоединяется к двойным связям и образуются соединения, близкие к животным жирам (рис. 2ВСодержащиеся в растительных маслах фрагменты ненасыщенных кислот, как и любые ненасыщенные соединения, могут быть прогидрированы, водород присоединяется к двойным связям и образуются соединения, близкие к животным жирам (рис. 2В). Этим способом в промышленности получают твердые жиры на основе подсолнечного, соевого или кукурузного масла. Из продуктов гидрирования растительных масел, смешанных с природными животными жирами и различными пищевыми добавками, изготавливают маргарин. Многие эфиры являются легковоспламеняющимися жидкостями и сгорают с образованием углекислого газа и воды (рис. 3)
Катализатор ГБФ-082 предназначен для гидрирования сложных эфиров жирных кислот, в частности бутилбутиратов – побочных продуктов оксосинтеза.
Слайд 26
Основной способ синтеза – взаимодействие карбоновой кислоты и

спирта, катализируемое кислотой и сопровождаемое выделением воды. Эта реакция
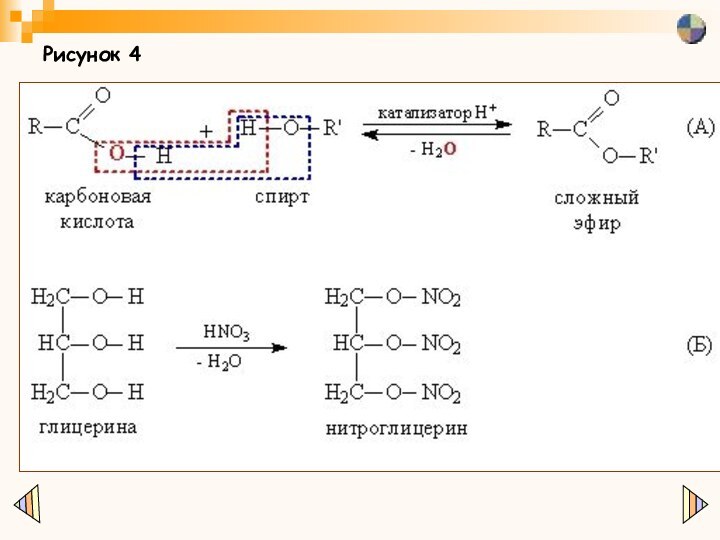
обратна показанной на рис. 4А. Чтобы процесс шел в нужном направлении (синтез сложного эфира), из реакционной смеси дистиллируют (отгоняют) воду. Специальными исследованиями с применением меченых атомов удалось установить, что в процессе синтеза атом О, входящий в состав образующейся воды, отрывается от кислоты (отмечено красной пунктирной рамкой), а не от спирта (нереализующийся вариант выделен синей пунктирной рамкой).
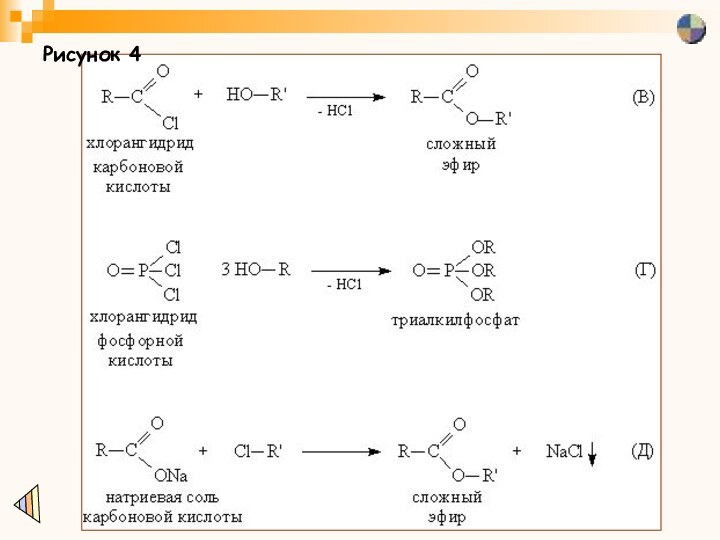
По такой же схеме получают сложные эфиры неорганических кислот, например, нитроглицерин (рис. 4БПо такой же схеме получают сложные эфиры неорганических кислот, например, нитроглицерин (рис. 4Б). Вместо кислот можно использовать хлорангидриды кислот, метод применим как для карбоновых (рис. 4ВПо такой же схеме получают сложные эфиры неорганических кислот, например, нитроглицерин (рис. 4Б). Вместо кислот можно использовать хлорангидриды кислот, метод применим как для карбоновых (рис. 4В), так и для неорганических кислот (рис. 4Г).
Взаимодействие солей карбоновых кислот с галоидалкилами RCl также приводит к сложным эфирам (рис. 4Д), реакция удобна тем, что она необратима – выделяющаяся неорганическая соль сразу удаляется из органической реакционной среды в виде осадка.
Получение сложных эфиров
Продолжение темы –
Слайд 27
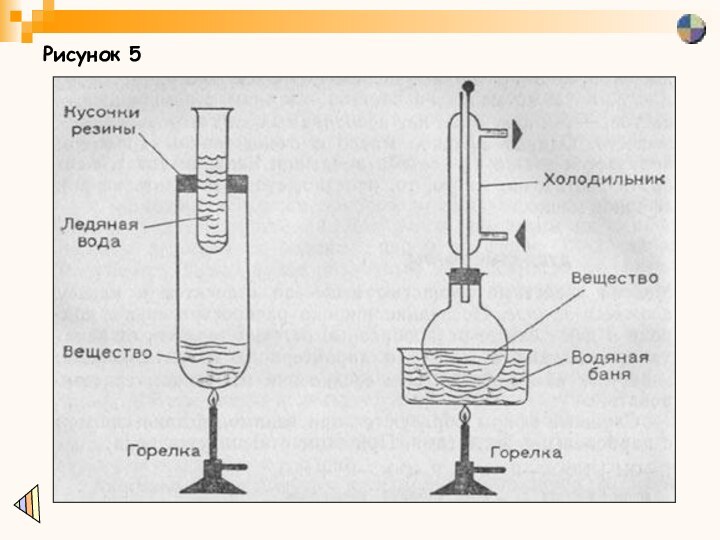
Опыт на получение сложного эфира
Чтобы получить сложные эфиры

в малых количествах, используем простой прибор (см. рис.5). В
широкую пробирку вставим узкую пробирку таким образом, чтобы одна треть широкой пробирки в ее нижней части оставалась незаполненной. Проще всего можно укрепить узкую пробирку с помощью нескольких кусочков резины, вырезанной из шланга или пробки. При этом необходимо учесть, что вокруг узкой пробирки обязательно нужно оставить зазор величиной не менее 1,5—2 мм, чтобы исключить избыточное давление при нагревании. Теперь нальем в широкую пробирку 0,5—2 мл спирта и приблизительно столько же карбоновой кислоты, при тщательном охлаждении (в ледяной воде или холодной проточной воде) добавим 5—10 капель концентрированной серной кислоты и в некоторых случаях еще несколько крупинок поваренной соли. Вставим внутреннюю пробирку, заполним ее холодной водой или еще лучше кусочками льда и укрепим собранный прибор в обычном штативе или в штативе для пробирок. Прибор нужно поставить подальше от себя и не наклоняться над отверстием пробирки (как и при проведении любого другого опыта!), потому что при неосторожном нагревании возможно разбрызгивание кислоты. Затем на самом малом огне горелки Бунзена будем кипятить смесь по крайней мере 15 минут (добавить «кипелки»!).
Слайд 28
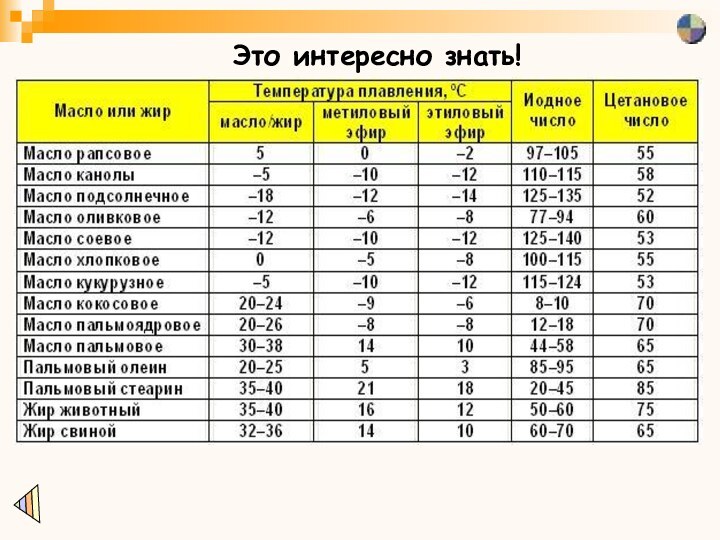
Свойства жиров
Жиры, образованные предельными кислотами, обычно имеют твердую
консистенцию, это жиры животного происхождения. С увеличением длины углеводородного
радикала температура плавления жира увеличивается. Если в составе жира содержатся остатки непредельных кислот, они представляют собой вязкие жидкости и часто называются маслами.
Слайд 29
Свойства восков
Воска обладают аморфностью, пластичностью, легко размягчаются и
плавятся обычно при более высоких температурах, чем твердые жиры
и жирные кислоты (в интервале 40-900C). Воски стойки к действию различных реагентов, многие годы сохраняются без изменений. Воски обладают химической устойчивостью, не подвержены окислению, водостойки, имеют достаточную твердость.
Воска сложных эфиров
Слайд 30
Масла – это жидкие жиры растительного происхождения (исключение
составляет твердое пальмовое масло
Слайд 32
Вопросы для проверки
Дайте понятие сложных эфиров?
Какими свойствами обладают
сложные эфиры на основе низших кислот и спиртов?
Дайте понятие
жиров?
Как образуются сложные эфиры, какова их общая формула?
Какой опыт на получение эфира можно провести собственными силами?
Какими химическими свойствами обладают сложные эфиры?
Какими физическими свойствами обладают сложные эфиры?
Какими физическими свойствами обладают жиры?
Какая изомерия присуща сложным эфиры?
Дайте понятие восков?
Кто является первооткрывателем сложных эфировКто является первооткрывателем сложных эфиров?
Слайд 33
Словарь основных терминов
Масла – это жидкие жиры растительного
происхождения (исключение составляет твердое пальмовое масло;
Сложные эфиры – производные
карбоновых кислот, в которых атом водорода карбоксильной группы замещен на углеводородный радикал;
Воска – сложные эфиры одиночных жирных кислот и одноатомных спиртов с длинной углеводородной цепочкой;
Нитроглицерин – известный лекарственный препарат и взрывчатое вещество, основа динамита;
Изомерия – существования веществ с одинаковым составом молекул, но обладающих различными свойствами;
Гидрирование – реакция присоединения молекулы водорода;
Дегидрирование – отщепление водорода;
Полимеризация – процесс соединения множества низкомолекулярного вещества в крупные молекулы полимера;
Диспропорционирование альдегида - получение сложного эфира из альдегида в присутствии алкоголята алюминия.
Слайд 34
Литература
О.С.Габриелян, И.Г.Остроумов – Химия(Пособие для школьников старших классов
и поступающих в вузы) издательство «Дрофа», 2006
А.А.Карцова – Покорение
вещества. Органическая химия. Издательство «Химиздат», 1999
Л.М.Пустовалова - Органическая химия. Издательство «Феникс», 2003
Слайд 35
Сложные эфиры – это производные карбоновых кислот, в
которых атом водорода карбоксильной группы замещен на углеводородный радикал
Слайд 36
Сложные эфиры низших кислот и спиртов составляют группу
фруктовых эфиров. Если в образовании сложного эфира участвует ароматический
спирт (содержащий ароматическое ядро), то такие соединения обладают, как правило, не фруктовым, а цветочным запахом. Все соединения этой группы практически нерастворимы в воде, но легко растворимы в большинстве органических растворителей.
Слайд 37
Липиды (жиры) представляют собой сложные эфиры жирных кислот
и трехатомного спирта глицерина.
Слайд 38
Сложные эфиры являются межклассовыми изомерами карбоновых кислот для
насыщенных R и R’ имеют общую формулу CnH2nO2. Им
свойственна структурная изомерия.
Слайд 39
Чтобы получить сложные эфиры в малых количествах, используем

простой прибор. В широкую пробирку вставим узкую пробирку таким
образом, чтобы одна треть широкой пробирки в ее нижней части оставалась незаполненной. Проще всего можно укрепить узкую пробирку с помощью нескольких кусочков резины, вырезанной из шланга или пробки. При этом необходимо учесть, что вокруг узкой пробирки обязательно нужно оставить зазор величиной не менее 1,5—2 мм, чтобы исключить избыточное давление при нагревании. Теперь нальем в широкую пробирку 0,5—2 мл спирта и приблизительно столько же карбоновой кислоты, при тщательном охлаждении (в ледяной воде или холодной проточной воде) добавим 5—10 капель концентрированной серной кислоты и в некоторых случаях еще несколько крупинок поваренной соли. Вставим внутреннюю пробирку, заполним ее холодной водой или еще лучше кусочками льда и укрепим собранный прибор в обычном штативе или в штативе для пробирок. Прибор нужно поставить подальше от себя и не наклоняться над отверстием пробирки (как и при проведении любого другого опыта!), потому что при неосторожном нагревании возможно разбрызгивание кислоты. Затем на самом малом огне горелки Бунзена будем кипятить смесь по крайней мере 15 минут (добавить «кипелки»!).
Слайд 41
Сложные эфиры низших карбоновых кислот представляют собой летучие
жидкости, многие из которых обладают приятным цветочным или фруктовым
запахом. Они практически нерастворимы в воде и имеют более низкие температуры кипения, чем изомерные им карбоновые кислоты. Это связанно с тем, что в молекулах сложных эфиров отсутствуют межмолекулярные водородные связи.
Слайд 42
Жиры, образованные предельными кислотами, обычно имеют твердую консистенцию,
это жиры животного происхождения. С увеличением длины углеводородного радикала
температура плавления жира увеличивается. Если в составе жира содержатся остатки непредельных кислот, они представляют собой вязкие жидкости и часто называются маслами.
Слайд 43
Структурная изомерия может быть связанна с длиной углеродной
цепи (приведенные ниже эфиры изомерны) в заместителях и строением
углеродного скелета.
Слайд 44
Воска - сложные эфиры одиночных жирных кислот и
одноатомных спиртов с длинной углеводородной цепочкой.