или несколько гидроксильных групп (групп –OH), соединенных с углеводородным
радикаломR
углеводородный радикал
-ОН
гидроксильная группа
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть







































R
углеводородный радикал
-ОН
гидроксильная группа
углеводородный радикал + ОЛ
СН3-СН-СН2-ОН
│
СН3
2- метилпропанол-1
СН3
│
СН3- С – СН3
│
ОН
Н
Н-С-О - Н
Н
При химических реакциях она может разрываться с отщеплением протона, т.е. спирты имеют слабые кислотные свойства.
Прогноз реакционной способности спиртов
Н
Н- С- ОН
Н
Спирты- амфотерные соединения
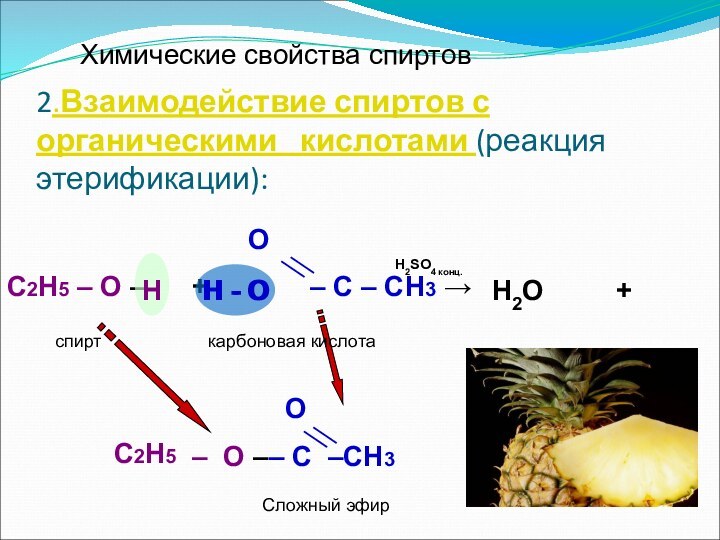
H - O
спирт
карбоновая кислота
H
Н2О
+
О
– O –– C –СН3
Сложный эфир
Н
Н - О
Н2SO4 конц.
С2Н5
Химические свойства спиртов