по распространенности элемент в земной коре, второй среди металлов
Это
элемент8 группы
побочной подгруппы
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть



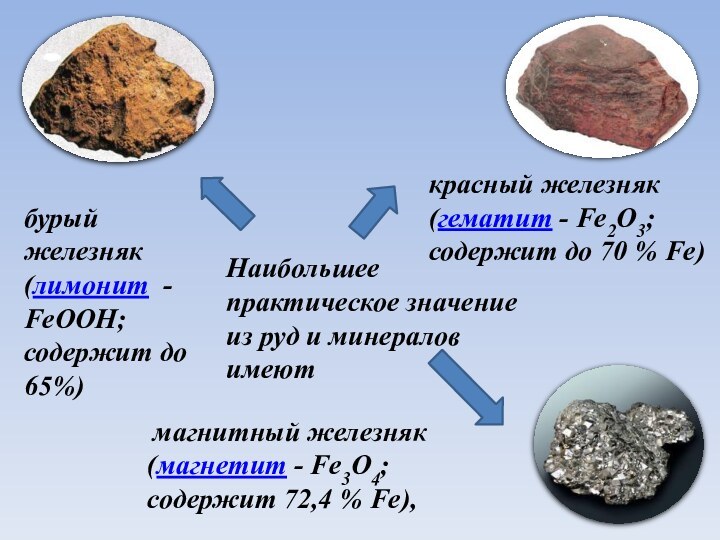









Встречается железо в виде различных соединений: оксидов, сульфидов, силикатов. В свободном виде железо находят в метеоритах, изредка встречается самородное железо (феррит) в земной коре как продукт застывания магмы.
бурый железняк (лимонит -
FeOOH;
содержит до 65%)
красный железняк (гематит - Fe2O3; содержит до 70 % Fe)
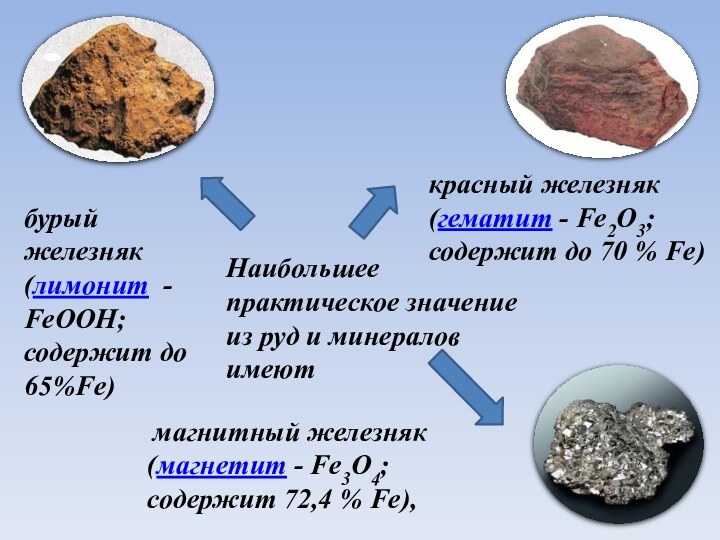
бурый железняк (лимонит -
FeOOH;
содержит до 65%Fe)
красный железняк (гематит - Fe2O3; содержит до 70 % Fe)
Реагирует с галогенами при нагревании:2Fe + 3CL2=2FeCL3
Первое железо на земле…….
История получения железа