негашеная известь,
жженка
Н2О
вода
Fe2O3
красный железняк
Al2O3 · nH2O
глинозем
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть
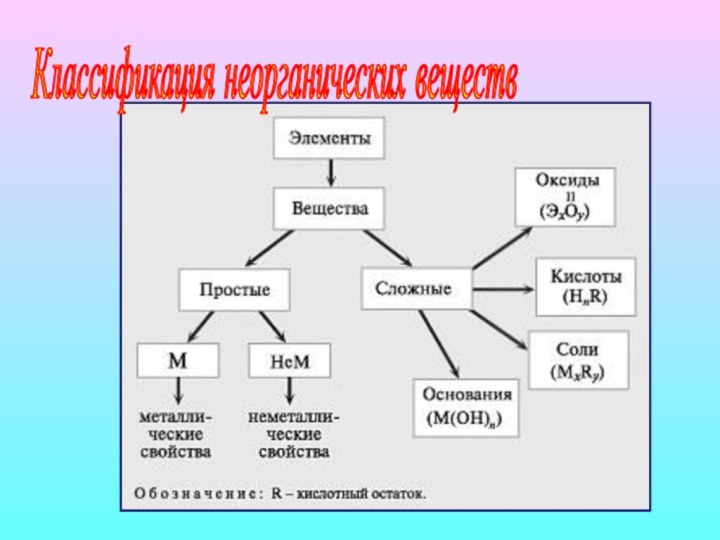











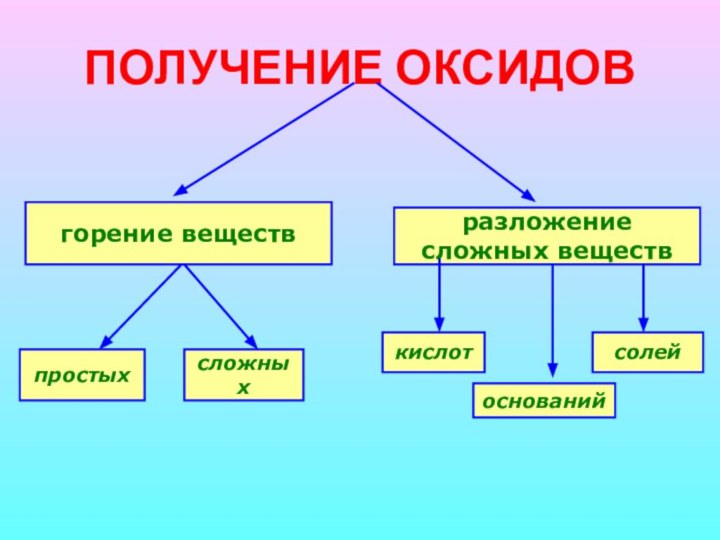



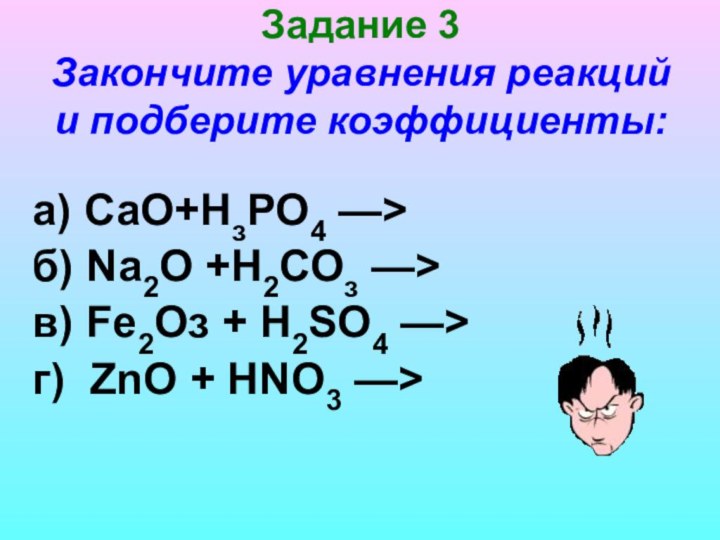






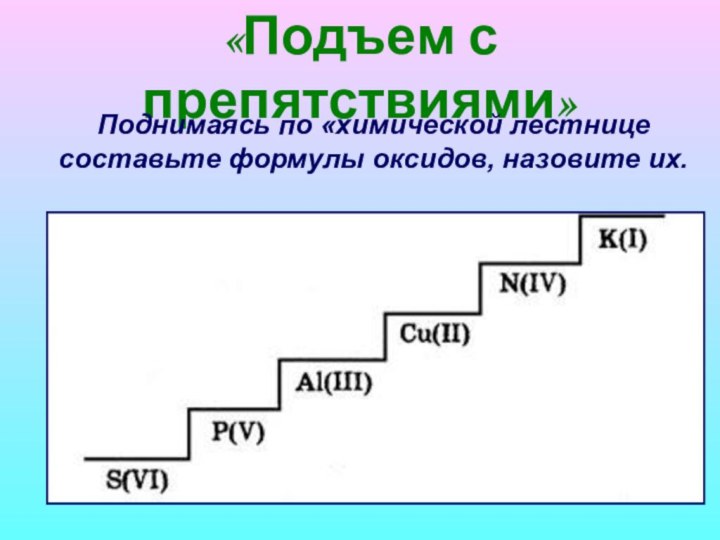
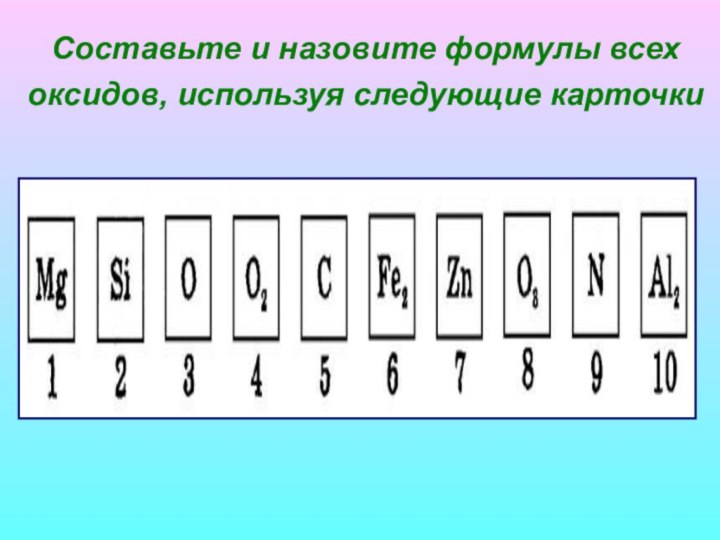
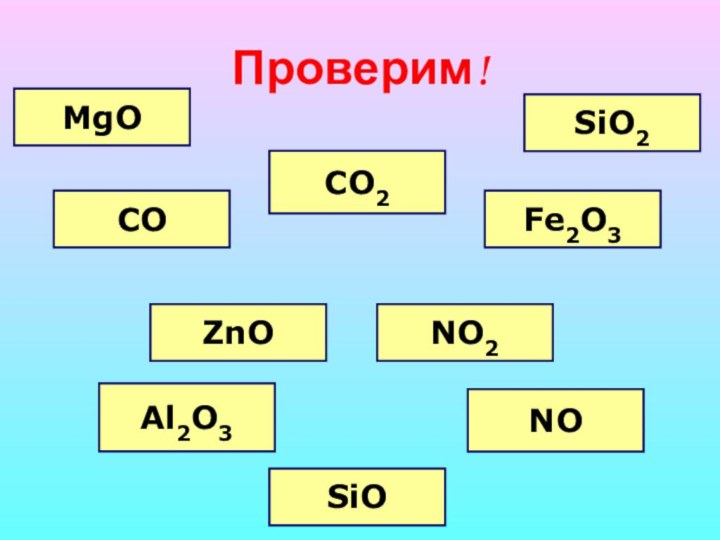

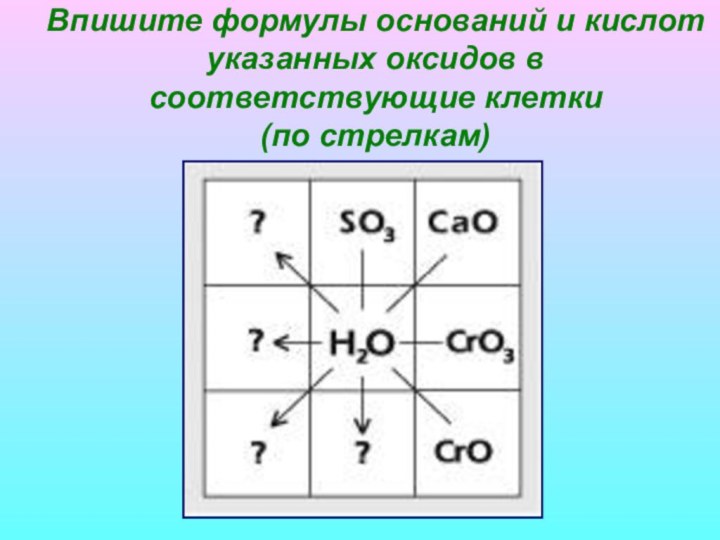
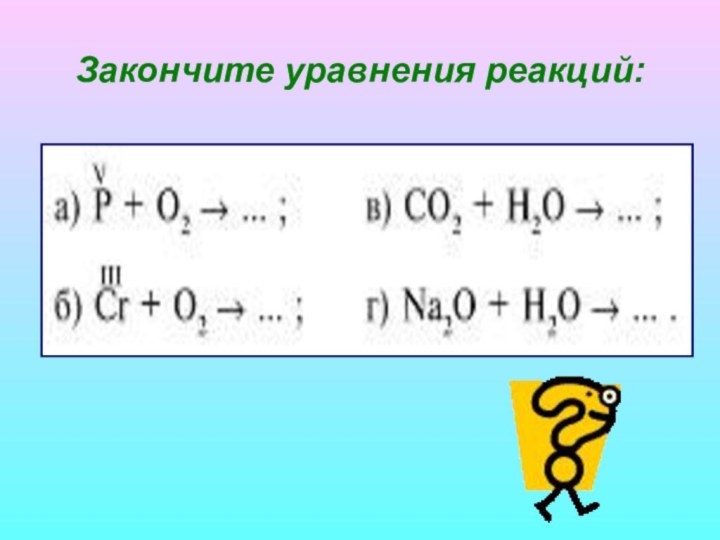

Классификация оксидов
ВаО, СО, N2О5, Fе2Оз, SO3, Na2O, N2O,
BeO, SiO2, SO2, Cs2O, Ag2O
Напишите уравнения осуществимых реакций.