Слайд 3
Болезнь Паркинсона - хроническое нейродегенеративное заболевание,
связанное с нарушением деятельности базальных ганглиев
головного мозга
Впервые описано в 1817 году английским врачом Джеймсом Паркинсоном в статье «Эссе о дрожательном параличе»
Но - описания аналогичного заболевания есть в «Аюрведе» и в китайском медицинском трактате «Nei Jing»
Слайд 4
«ДОРОЖНАЯ КАРТА»
ПРИ БОЛЕЗНИ ПАРКИНСОНА
Слайд 5
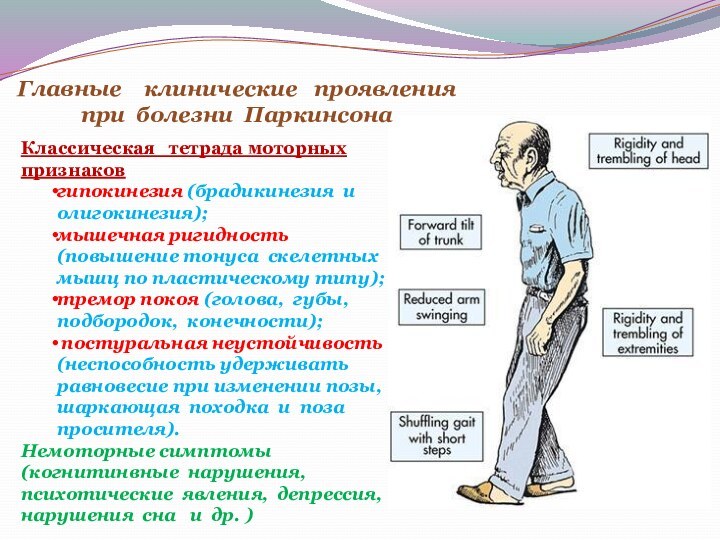
Главные клинические проявления
при болезни Паркинсона
Классическая
тетрада моторных признаков
гипокинезия (брадикинезия и олигокинезия);
мышечная
ригидность (повышение тонуса скелетных мышц по пластическому типу);
тремор покоя (голова, губы, подбородок, конечности);
постуральная неустойчивость (неспособность удерживать равновесие при изменении позы, шаркающая походка и поза просителя).
Немоторные симптомы (когнитинвные нарушения, психотические явления, депрессия, нарушения сна и др. )
Слайд 6
Эпидемиология болезни Паркинсона
В мире в целом
насчитывается около 6 миллионов пациентов с
болезнью Паркинсона
В России, по разным (и, скорее всего, неполным) данным, насчитывается от 117000 до 338000 больных БП
Второе по частоте встречаемости нейродегенеративное заболевание (после болезни Альцгеймера)
Этнические отличия в частоте заболевания (от 15\100000 в Китае до 100-250\100000 в Европе и США до 600\100000 в Аргентине)
В среднем в Европе идиопатическим паркинсонизмом страдает не менее 1% лиц в возрасте старше 50 лет и 2-4% лиц с возрасте старше 65 лет
Мужчины и женщины болеют с одинаковой частотой
Ожидается, что в следующие 50 лет число пациентов будет расти за счет повышения продолжительности жизни и «омоложения» заболевания
Но старение само по себе - не причина болезни Паркинсона
Слайд 7
«ДОРОЖНАЯ КАРТА»
ПРИ БОЛЕЗНИ ПАРКИНСОНА
Слайд 8
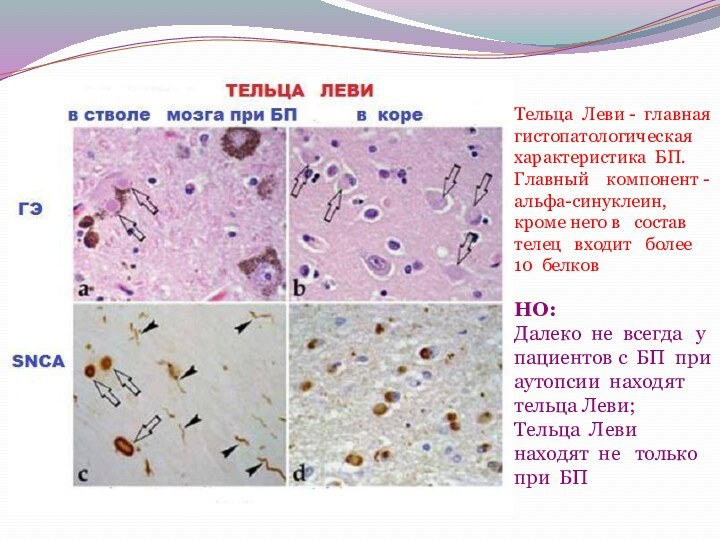
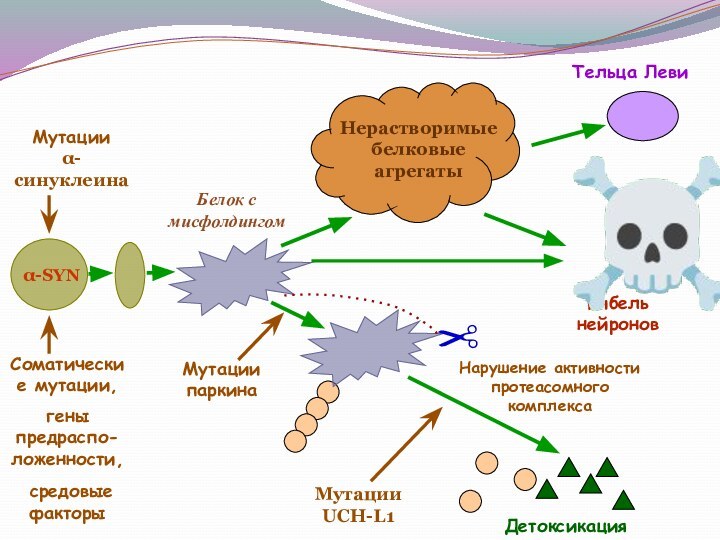
Тельца Леви - главная гистопатологическая
характеристика БП. Главный
компонент - альфа-синуклеин, кроме него в состав
телец входит более 10 белков
НО:
Далеко не всегда у пациентов с БП при аутопсии находят тельца Леви;
Тельца Леви находят не только при БП
Слайд 9
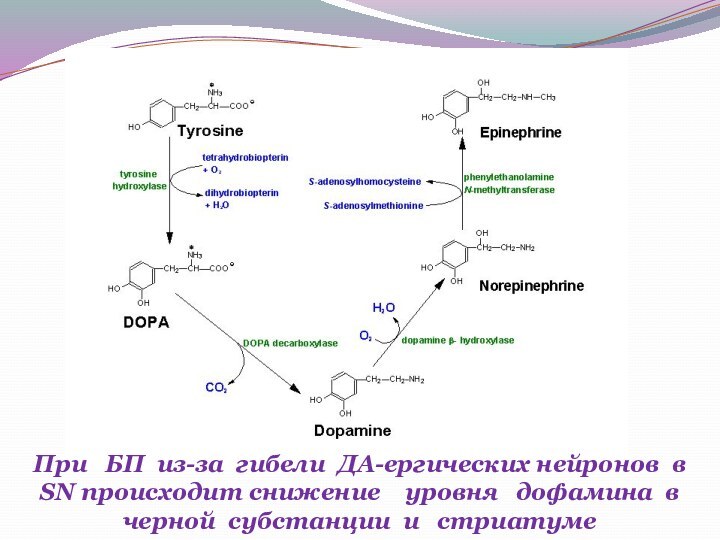
При БП из-за гибели ДА-ергических нейронов в
SN происходит снижение уровня дофамина в
черной субстанции и стриатуме
Слайд 10
Нигростриатная ДА система контролирует активность
ГАМК и глутаматергических синапсов
неостриатума, которые в свою очередь активируют таламокортикальные сети и
регулируют моторное поведение.
Слайд 11
При болезни Паркинсона тельца Леви в
первую очередь наблюдаются в области черной субстанции
- где они связаны с дегенерацией дофаминергических нейронов
Но процесс дегенерации не ограничивается ДА-ергическими нейронами в SN и других отделах мозга и распространяется со временем на НА-ергические нейроны в голубом пятне ствола мозга и НТ-ергические нейроны ядра шва, а также на нейроны периферической нервной системы в сердце, ЖКТ и других внутренних органах
Слайд 12
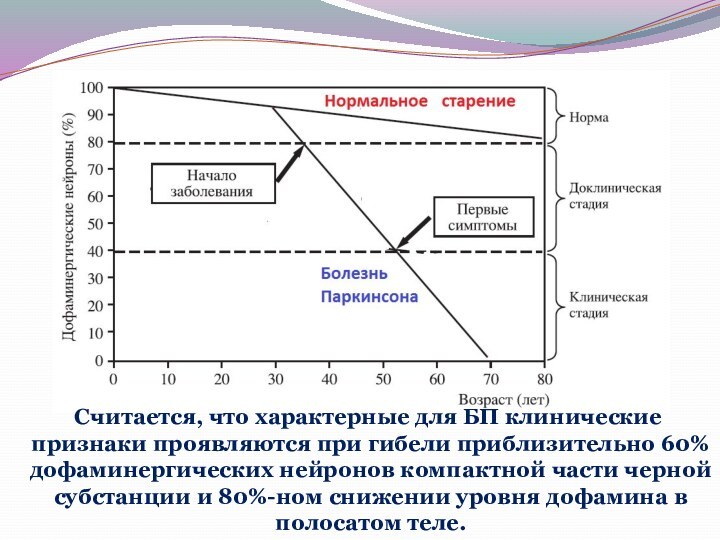
Cчитается, что характерные для БП клинические
признаки проявляются при гибели приблизительно 60% дофаминергических нейронов компактной
части черной субстанции и 80%-ном снижении уровня дофамина в полосатом теле.
Слайд 13
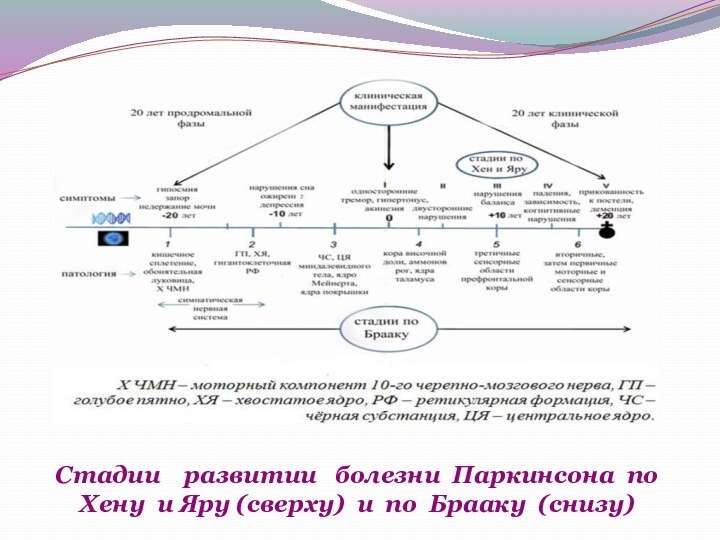
Стадии развитии болезни Паркинсона по
Хену и Яру (сверху) и по Брааку (снизу)
Слайд 14
«ДОРОЖНАЯ КАРТА»
ПРИ БОЛЕЗНИ ПАРКИНСОНА
Слайд 15
В большинстве случаев болезнь Паркинсона носит спорадический характер
и обусловлена взаимодействием генетической конституции организма и факторов внешней
среды
Семейные моногенные формы составляют не более 10-15% всех случаев заболевания - но именно они стали ключом к пониманию этиопатогенеза болезни Паркинсона
Слайд 16
Факторы среды в патогенезе
болезни Паркинсона
Риск
развития заболевания повышен при:
проживании в сельской местности;
употреблении сырой воды;
работе в сельском хозяйстве;
Скорее всего это эффект пестицидов и гербицидов
Риск развития заболевания снижен у
- курильщиков
- кофеманов и чаеманов
Слайд 17
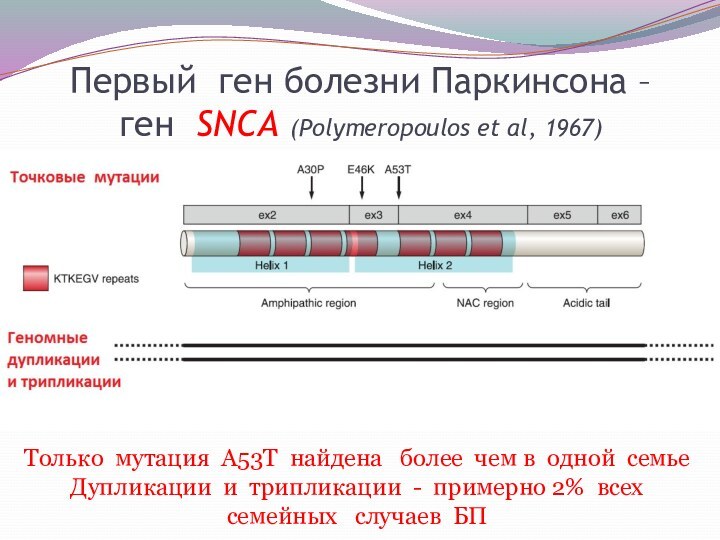
Первый ген болезни Паркинсона – ген SNCA (Polymeropoulos
et al, 1967)
Только мутация А53Т найдена более чем
в одной семье
Дупликации и трипликации - примерно 2% всех семейных случаев БП
Слайд 18
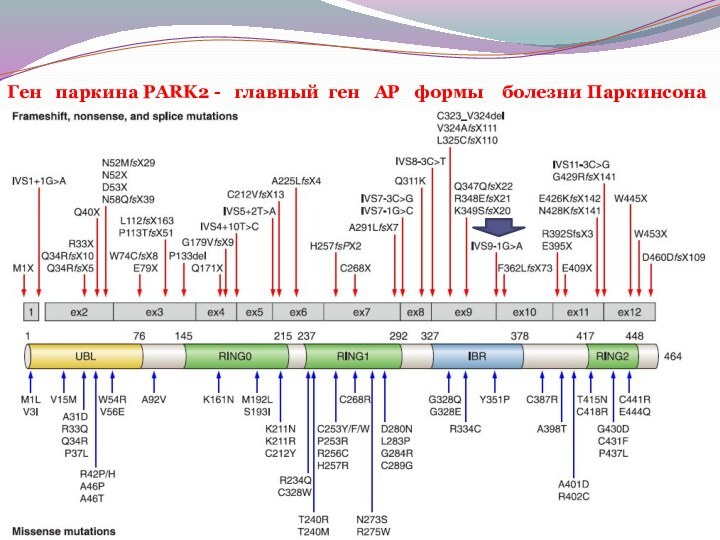
Ген паркина PARK2 - главный ген
АР формы болезни Паркинсона
Слайд 20
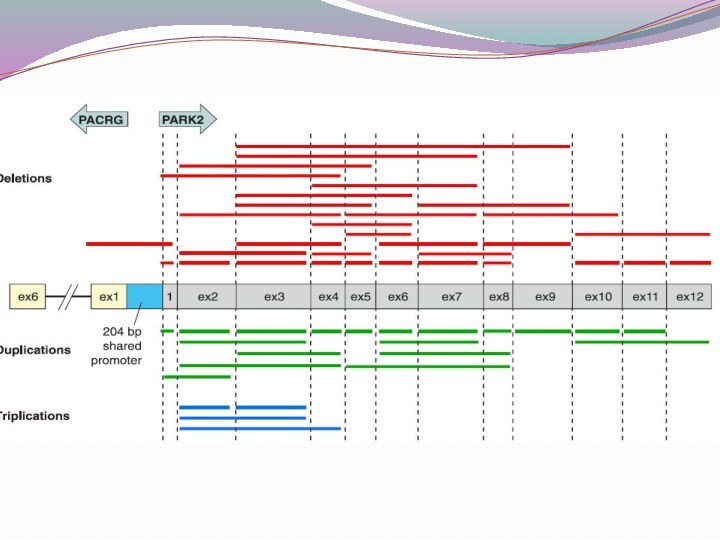
Распределение делеций и дупликаций в гене PARK2 у
спорадических больных БП из России с ранним (А) и
поздним (Б) началом развития заболевания.
А
Б
Слайд 22
Идентифицирован в 1997 г. (Tohru, et. al., Nature)
12
экзонов, 465 AA
E3 убиквитин лигаза
Непосредственной функцией паркина является
перенос убиквитина с убиквитин-конъюгирующего фермента (Е2) на специфичные субстраты.
Слайд 24
«ДОРОЖНАЯ КАРТА»
ПРИ БОЛЕЗНИ ПАРКИНСОНА
Слайд 25
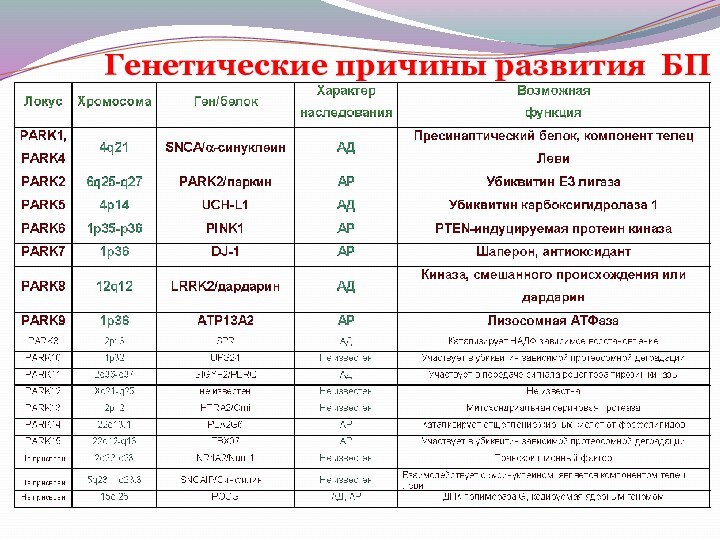
Генетические причины развития
БП
Слайд 26
Ген киназы с лейцин богатыми повторами
LRRK2 - основной ген AД формы
болезни Паркинсона
Слайд 27
Мультфункциональная серин-треонин киназа, может принимать участие в
контроле за обменом синаптических везикул, росте и ветвлении аксонов
и функционировании аппарата Гольджи, лизосом и митохондрий
Слайд 28
Еще одна cерин-треонин киназа с митохондриальной
локализацией - PINK1
Слайд 29
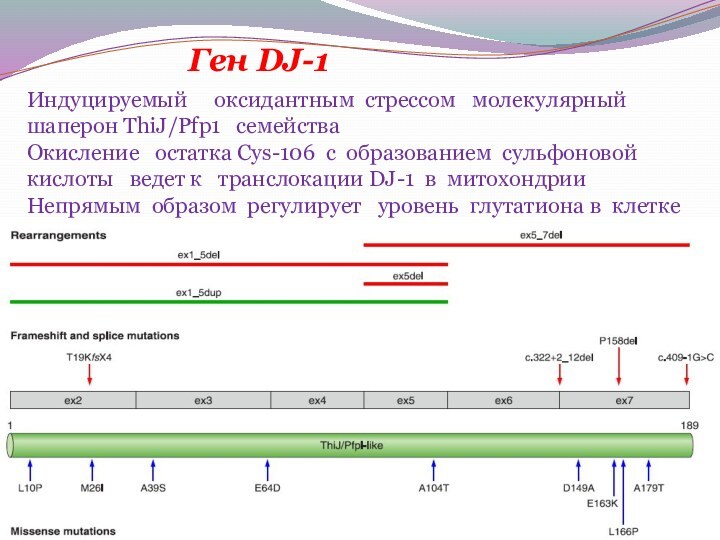
Ген DJ-1
Индуцируемый оксидантным стрессом
молекулярный шаперон ThiJ/Pfp1 семейства
Окисление
остатка Cys-106 с образованием сульфоновой кислоты ведет к транслокации DJ-1 в митохондрии
Непрямым образом регулирует уровень глутатиона в клетке
Слайд 30
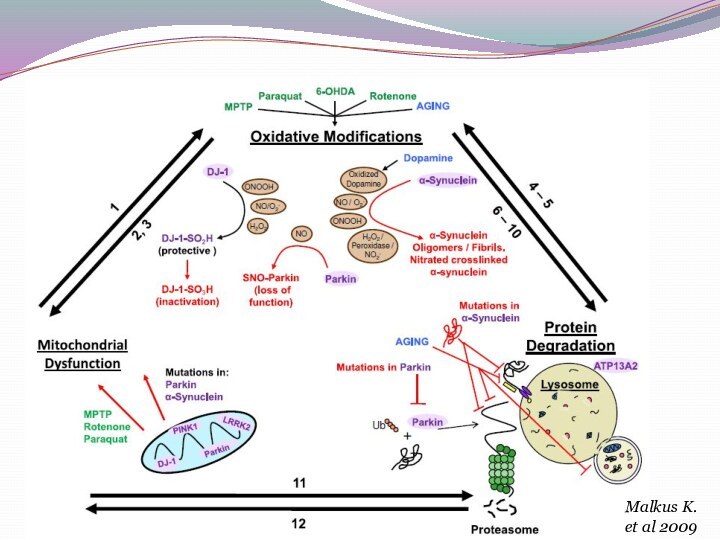
У дрозофилы белки паркин, PINK1 и DJ-1
необходимы для нормального функционирования митохондрий
Corti
О. et al 2011
Слайд 31
Паркин и PINK1 участвуют в регуляции процесса
митохондриальной аутофагии
Слайд 33
ВСЕ ЛИ ГЕНЫ БОЛЕЗНИ ПАРКИНСОНА
ВЫЯВЛЕНЫ ?
ОСНОВНЫЕ - ДА
НО ПОИСК ПРОДОЛЖАЕТСЯ
РЕДКИЕ
ГЕНЫ
СЕМЕЙНЫХ ФОРМ
ПОЛНОГЕНОМНЫЙ АССОЦИАТИВНЫЙ
АНАЛИЗ (GWAS) ПРИ СПОРАДИЧЕСКОЙ БП
Слайд 34
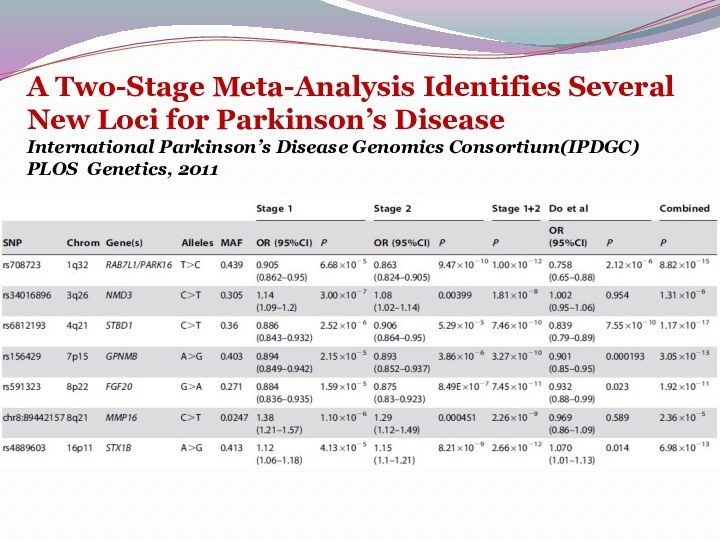
A Two-Stage Meta-Analysis Identifies Several New Loci for
Parkinson’s Disease
International Parkinson’s Disease Genomics Consortium(IPDGC)
PLOS Genetics, 2011
Слайд 35
ПЕРЕХОД К КОМПЛЕКСНОМУ АНАЛИЗУ
данные GWAS
дифференциальное
метилирование ДНК
транскриптом мозга
транскриптом периферической
крови
протеом мозга
протеом периферической
крови
Слайд 36
ШИРОКОЕ ИСПОЛЬЗОВАНИЕ МОДЕЛЕЙ БОЛЕЗНИ ПАРКИНСОНА
Генетические
модели
Получены трансгенные
мыши, дрозофилы, нематоды с различными вариантами генов SNCA, PARK2, DJ-1,
LRRK-2
Токсические модели
6-гидроксидофамин
Ротенон
МРТР
Слайд 37
Схема эксперимента по моделированию паркинсонизма с использование 6-ГДА
и последующего анализа изменения транскриптома в черной субстанции у
крыс паркинсон-подобным фенотипом.
Слайд 38
Проанализировано 24500 генов крысы.
131 ген, достоверно
изменивший экспрессию в черной субстанции через 2 недели после
введения токсина.
698 генов, достоверно изменивших экспрессию в черной субстанции через 4 недели после введения токсина.
Для дальнейшего анализа панели дифференциально экспрессирующихся генов была использована база данных DAVID
Слайд 39
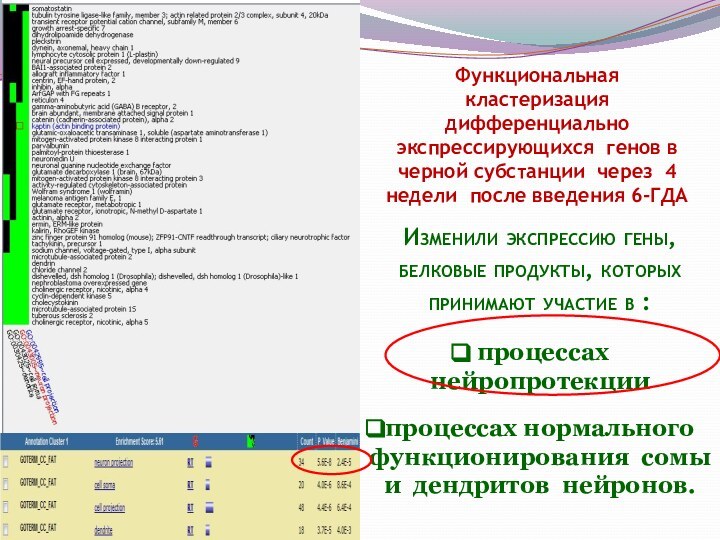
Функциональная кластеризация дифференциально экспрессирующихся генов в
черной субстанции через 4 недели после введения 6-ГДА
Изменили
экспрессию гены, белковые продукты, которых принимают участие в :
процессах нейропротекции
процессах нормального функционирования сомы и дендритов нейронов.
Слайд 40
Ген нейромедина (NMU), который является нейропептидом. Точная функция
белка не известна. Установлено, что он может играть важную
роль в энергетическом обмене, будучи вовлечен в процессы регуляции аппетита.
Ген PPT1 кодирует тиоэстеразу 1 пальмитоилированных белков, которая принимает непосредственное участие лизосомальной деградации белков
Ген GRM1 кодирует метаботропный рецептор глутамата, который является одним из участников глутаматэргической системы.
Ген PVALB, который кодирует парвальбумин, имеющий высокое сродство с кальций связывающими белками, такими как кальмодулин. Это сходство предполагает, его важную роль в гомеостазе кальция.
Ген WFS1 кодирует вольфрамин, который является мембранным гликопротеином эндоплазматического ретикулума и предположительно участвует в формировании синаптических везикул.
ОТОБРАННЫЕ ГЕНЫ
Слайд 41
«ДОРОЖНАЯ КАРТА»
ПРИ БОЛЕЗНИ ПАРКИНСОНА
Слайд 42
Современные лекарственные методы лечения БП:
мишени и препараты
Слайд 43
ПЕРСПЕКТИВЫ
Клеточная терапия
Эмбриональные стволовые
клетки
Фетальная нервная
ткань
ДА-нейроны на основе iPS
Трансгенные «кассеты» для синтеза ДА и\или введения генов нейротрофинов
Общая проблема - нет восстановления архитектоники ДА-ергической системы мозга
Слайд 44
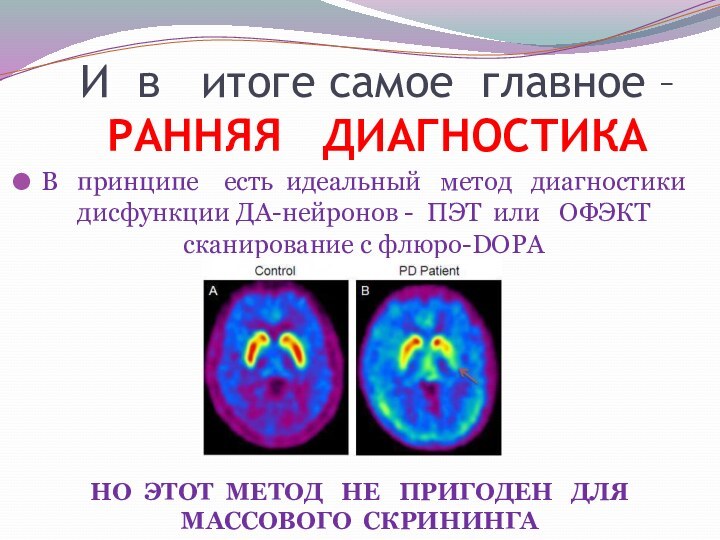
И в итоге самое главное – РАННЯЯ
ДИАГНОСТИКА
В принципе есть идеальный
метод диагностики дисфункции ДА-нейронов - ПЭТ или ОФЭКТ сканирование с флюро-DOPA
НО ЭТОТ МЕТОД НЕ ПРИГОДЕН ДЛЯ МАССОВОГО СКРИНИНГА
Слайд 45
Массовый скрининг:
быстро - просто - относительно
дешево
Нарушение обоняния
Обстипация (запоры)
Нарушения сна (парадоксальный сон без мышечной атонии)
Изменение ЭЭГ
Биохимические маркеры периферической крови (метаболиты дофамина, гормоны гипофиза, специфические белки (альфа-синуклеин)
Провокационные тесты (выявление латентного тремора, временное блокирование
тирозин гидроксилазы и др.)
Слайд 46
где (ΔΔCt)= =(Сt(x)-Ct(r))-(Сt(x0)-Ct(r0)), где Ct(х) и Ct(х0) -
пороговый цикл амплификации для гена-кандидата в исследуемой группе и
контрольной группе здоровых добровольцев соответственно, Ct(r) и Ct(r0) - то же для гена сравнения
R = 2 –(ΔΔCt)
БП - больные БП
ЦА- больные с церебральным атеросклерозом
НЗ – больные с различными неврологическими болезнями
За единицу принят уровень экспрессии анализируемых генов в группе неврологически здоровых добровольцев.
Слайд 48
Отдел молекулярных основ генетики человека Института
молекулярной генетики РАН
Шадрина М.И. , Семенова Е.С., Филатова
Е.В., Алиева А.Х., Сломинский П.А.
Отделение нейрогенетики ГУ Центр Неврологии РАМН
Иллариошкин С.Н., Иванова-Смоленская И.А.
СПАСИБО ЗА ВНИМАНИЕ